
|
|
הערות הרצאה, דפי רמאות
טיפול בבית חולים. הערות ההרצאה: בקצרה, החשוב ביותר
מדריך / הערות הרצאה, דפי רמאות תוכן העניינים
הרצאה מס' 1. מחלות של מערכת הלב וכלי הדם. שִׁגָרוֹן שיגרון (מחלת סוקולסקי-בויו) היא מחלה דלקתית מערכתית של רקמת החיבור עם לוקליזציה דומיננטית של התהליך במערכת הלב וכלי הדם, המתפתחת אצל אנשים הסובלים ממנה (ככלל, מדובר באנשים צעירים) עקב זיהום חריף עם סטרפטוקוקוס β-המוליטי מקבוצה A. הגדרה זו של המחלה ניתנה בשנת 1989 על ידי V. A. Nasonov. זה משקף את כל המאפיינים האופייניים של המחלה: 1) נזק דומיננטי למערכת הלב וכלי הדם; 2) תפקיד התורשה הפתולוגית; 3) המשמעות של זיהום סטרפטוקוקלי. מהות המחלה טמונה בתבוסה של כל ממברנות הלב, אך בעיקר שריר הלב והאנדוקרדיום עם התרחשות של דפורמציה של מנגנון המסתם - מחלת לב והתפתחות אי ספיקת לב לאחר מכן. התבוסה של איברים ומערכות אחרים בראומטיזם היא בעלת חשיבות משנית ואינה קובעת את חומרתה ואת הפרוגנוזה שלאחר מכן. אטיולוגיה. סטרפטוקוקים בטא המוליטיים מקבוצה A גורמים נזק לדרכי הנשימה העליונות. זו הסיבה שתחילתה של שיגרון, ככלל, קודמת לכאב גרון, החמרה של דלקת שקדים כרונית, וכמות מוגברת של אנטיגן סטרפטוקוקלי ונוגדנים אנטי סטרפטוקוקליים (ASL-O, ASG, ASA, antideoxyribonuclease B (אנטי דיאוקסיריבונוקלאז). -DNase B)) מתגלים בדם החולים. קשר כזה עם זיהום סטרפטוקוקלי קודם בולט במיוחד במהלך החריף של שיגרון, המלווה בפוליארתריטיס. בהתפתחות שיגרון, גיל וגורמים חברתיים משחקים תפקיד (תנאי חיים לא נוחים, תת תזונה), גם נטייה גנטית חשובה (שיגרון היא מחלה תורשתית פוליגנית, קיומן של משפחות "ראומטיות" ידוע), המורכבת ממחלה. תגובה היפראימונית לאנטיגנים של סטרפטוקוקוס, הנטייה של חולים לתהליכים אוטואימוניים ואימונוקומפלקסים. פתוגנזה. עם שיגרון, מתרחשת תגובה חיסונית מורכבת ומגוונת (תגובות רגישות יתר מיידיות ומושהות) לאנטיגנים רבים של סטרפטוקוקל. כאשר זיהום חודר לגוף נוצרים נוגדנים אנטי סטרפטוקוקלים ונוצרים קומפלקסים חיסוניים (אנטיגנים סטרפטוקוקלים + נוגדנים אליהם + משלים), שמסתובבים בדם ומתיישבים במיטה המיקרו-סירקולטורית. לרעלים ולאנזימים של סטרפטוקוק יש גם השפעה מזיקה על שריר הלב ורקמת החיבור. עקב פגם שנקבע גנטית במערכת החיסון, אנטיגנים ותסביכי חיסון של סטרפטוקוקלים אינם מסולקים לחלוטין ובמהירות מגוף החולים. לרקמות של חולים כאלה יש נטייה מוגברת לתקן קומפלקסים חיסוניים אלה. נוגדנים בעלי תגובה צולבת משחקים כאן גם תפקיד, אשר נוצרים על אנטיגנים סטרפטוקוקליים, מסוגלים להגיב עם רקמות, כולל אנטיגנים לבביים, של הגוף. בתגובה מתפתחת דלקת על בסיס חיסוני (לפי סוג רגישות היתר המיידית), בעוד שהגורמים המיישמים את התהליך הדלקתי הם אנזימים ליזוזומליים של נויטרופילים הפגוציטים קומפלקסים חיסוניים ונהרסים בו זמנית. תהליך דלקתי זה ממוקם ברקמת החיבור, בעיקר של מערכת הלב וכלי הדם, ומשנה את התכונות האנטיגניות שלה ושל שריר הלב. כתוצאה מכך, תהליכים אוטואימוניים מתפתחים בהתאם לסוג רגישות יתר מסוג מושהה, ולימפוציטים המגיבים עם רקמת לב נמצאים בדם של חולים. לתאים אלו חשיבות רבה במקורם של נגעי איברים (בעיקר הלב). ברקמת החיבור עם שיגרון מתרחשים שינויי פאזה: נפיחות רירית - שינויים פיברינואידים - נמק פיברינואידי. הביטוי המורפולוגי של הפרעות חיסוניות הן תגובות תאיות - חדירת לימפוציטים ופסמוציטים, היווצרות של גרנולומה ראומטית, או אשוף-טלאייבסקי. התהליך הפתולוגי מסתיים בטרשת. מצע מורפולוגי נוסף לפגיעה בלב במחלת לב ראומטית הוא תגובה דלקתית לא ספציפית הדומה לזו במפרקים ובממברנות הסרוסיות: נפיחות של רקמת החיבור הבין-שרירית, הזעה של פיברין, חדירת נויטרופילים ולימפוציטים. המחלה זורמת בגלים, מחמירה בהשפעת זיהום או גורמים לא ספציפיים (היפותרמיה, מתח פיזי, מתח וכו'), הקשורה לאופי האוטואימוני של התהליך הפתולוגי. כאשר הלב ניזוק, התהליך הדלקתי יכול להתפשט לכל ממברנות הלב (פנקרדיטיס) או בבידוד לכל אחד מהקרומים. שינויים מורפולוגיים בראומטיזם נמצאים בעיקר בשריר הלב, ולכן מיוקרדיטיס בשלבים המוקדמים היא שקובעת את התמונה הקלינית. שינויים דלקתיים באנדוקרדיום (דלקת מסתם, אנדוקרדיטיס ורוסית), פגיעה בחוטי הגיד ובטבעת הסיבית מתגלים קלינית 6-8 שבועות לאחר התקף השיגרון. השסתום המיטרלי מושפע לרוב, ואחריו מסתמי אבי העורקים והתלת-צדדיים. השסתום הריאתי בראומטיזם כמעט ואינו מושפע. סיווג של שיגרון. נכון להיום, אומץ הסיווג והמינוח של שיגרון, שאושרו בשנת 1990 על ידי האגודה המדעית של כל האיחוד לראומטולוגיה, המשקפים את שלב התהליך, המאפיינים הקליניים והאנטומיים של נזק לאיברים ומערכות, אופי הקורס. והמצב התפקודי של מערכת הלב וכלי הדם (ראה טבלה 1). תמונה קלינית. ניתן לחלק את כל ביטויי המחלה ללב ולחוץ לבבי. ניתן לתאר את התמונה הקלינית של המחלה מתוך עמדות אלו. שלב א': מתגלה הקשר של המחלה עם הזיהום המועבר. במקרים טיפוסיים, 1-2 שבועות לאחר כאב גרון או מחלה חריפה בדרכי הנשימה, טמפרטורת הגוף עולה, לעיתים עד 38-40 מעלות צלזיוס, עם תנודות במהלך היום בתוך 1-2 מעלות צלזיוס וזיעה חזקה (לרוב ללא צמרמורות). בהתקפים חוזרים ונשנים של שיגרון, לעיתים קרובות מתפתחת חזרה של המחלה בהשפעת גורמים לא ספציפיים (כגון היפותרמיה, עומס פיזי, ניתוח). לוח 1 סיווג של שיגרון
הביטוי השכיח ביותר של שיגרון הוא פגיעה בלב - מחלת לב ראומטית: פגיעה בו זמנית בשריר הלב ובאנדוקרדיום. אצל מבוגרים, מחלת לב ראומטית אינה חמורה. חולים מתלוננים על כאב קל או אי נוחות באזור הלב, קוצר נשימה קל במהלך פעילות גופנית, הפרעות או דפיקות לב שכיחות הרבה פחות. תסמינים אלו אינם ספציפיים למחלת לב ראומטית ועשויים להיראות במצבי לב אחרים. אופי התלונות הללו מצוין בשלבים הבאים של החיפוש האבחוני. Rheumocarditis בחולים צעירים, ככלל, היא חמורה: מתחילת המחלה, קוצר נשימה חמור במהלך פעילות גופנית ובמנוחה, כאב מתמיד בלב ודפיקות לב. ייתכנו תסמינים של אי ספיקת מחזור במעגל גדול בצורה של בצקת וכבדות בהיפוכונדריום הימני (עקב עלייה בכבד). כל התסמינים הללו מצביעים על דלקת שריר הלב מפוזרת חמורה. פריקרדיטיס, כמו גם ביטויים חוץ-לביים של שיגרון, הם נדירים. עם התפתחות פריקרדיטיס יבש, החולים מציינים רק כאב מתמיד באזור הלב. עם פריקרדיטיס exudative, המאופיינת בהצטברות של exudate serous-fibrinous בשק הלב, הכאב נעלם, כאשר שכבות קרום הלב הדלקתיות מופרדות על ידי exudate המצטבר. מופיע קוצר נשימה, שמתגבר עם המיקום האופקי של המטופל. עקב הקושי בזרימת הדם ללב הימני, מופיע גודש במעגל גדול (בצקת, כבדות בהיפוכונדריום הימני עקב עלייה בכבד). המאפיין ביותר של שיגרון הוא התבוסה של מערכת השרירים והשלד בצורה של דלקת מפרקים שגרונית. המטופלים מציינים כאב גובר במהירות במפרקים גדולים (ברך, מרפק, כתף, קרסול, פרק כף היד), חוסר האפשרות של תנועות פעילות, עלייה בנפח המפרקים. ישנה השפעה מהירה לאחר שימוש בחומצה אצטילסליצילית ובתרופות נוגדות דלקת שאינן סטרואידיות אחרות עם הקלה למשך מספר ימים, לרוב מספר שעות של כל הביטויים המפרקים. נגעים ראומטיים של הכליות הם גם נדירים ביותר, מתגלים רק במחקר של שתן. נגעים של מערכת העצבים בראומטיזם הם נדירים, בעיקר בילדים. התלונות דומות לאלו של דלקת המוח, דלקת קרום המוח, דלקת כלי דם במוח של אטיולוגיה שונה. רק "כוריאה קטנה" ראויה לתשומת לב, המופיעה בילדים (לעתים קרובות יותר בנות) ומתבטאת בשילוב של רגישות רגשית והיפרקינזיס אלים של תא המטען, הגפיים והשרירים המחקים. תסמונת בטן (דלקת הצפק) מופיעה כמעט אך ורק בילדים ובני נוער עם שיגרון ראשוני חריף. זה מאופיין בהתפרצות פתאומית, חום וסימנים של דיספאגיה (כאבי התכווצויות מפושטים או מקומיים, בחילות, הקאות, עצירות או צואה תכופה). בשלב השני של החיפוש האבחוני, אין חשיבות לגילוי סימני נזק ללב. במחלת לב ראומטית ראשונית, הלב בדרך כלל אינו מוגדל. אוסקולציה מגלה טונוס I עמום, לפעמים הופעה של טונוס III, אוושה סיסטולית רכה בקודקוד. סימפטומטולוגיה זו נובעת משינויים בשריר הלב. עם זאת, עלייה בעוצמת, משך והתמדה של הרעש עשויה להצביע על היווצרות של אי ספיקה של המסתם המיטרלי. ניתן לשפוט בביטחון את היווצרות הפגם 6 חודשים לאחר תחילת ההתקף, תוך שמירה על תמונת ההשמעה לעיל. במקרה של פגיעה במסתם אבי העורקים, עשויה להישמע אוושה פרוטו-דיאסטולית בנקודת בוטקין, ולהישמר הצליל של הטון II. רק שנים רבות לאחר מכן, לאחר היווצרות אי ספיקה חמורה של מסתם אבי העורקים, מצטרפת לסימן ההשמעה הזה היחלשות (או היעדר) של הטון II בחלל הבין-צלעי II מימין. בחולים עם polyarthritis, עיוות מפרק הוא ציין עקב דלקת של הממברנה הסינוביאלית ורקמות periarticular, כאב במישוש של המפרק. באזור המפרקים הפגועים עשויים להופיע גושים ראומטיים, הממוקמים על האמות והשוקים, מעל הבולטות הגרמיות. אלו תצורות קטנות, צפופות וללא כאבים שנעלמות בהשפעת הטיפול. Erythema annulare (סימן כמעט פתוגנומוני לראומטיזם) הם אלמנטים בצורת טבעת ורודים, לא מגרדים, הממוקמים על העור של המשטח הפנימי של הידיים והרגליים, הבטן, הצוואר והגזע. סימפטום זה נדיר ביותר (ב-1-2% מהחולים). לדלקת ריאות ראומטית ולדלקת צדר יש את אותם סימנים פיזיים כמו מחלות דומות של אטיולוגיה בנאלית. באופן כללי, נגעים שאינם לבביים נצפים כיום לעיתים רחוקות ביותר, בצעירים עם מהלך חריף של שיגרון (בנוכחות פעילות גבוהה - תואר III). הם מתבטאים בצורה לא חדה, ניתנים במהירות להפוך את ההתפתחות במהלך טיפול אנטי-ראומטי. בשלב III של החיפוש האבחוני, נתוני המחקרים המעבדתיים והאינסטרומנטליים מאפשרים לנו לבסס את פעילות התהליך הפתולוגי ולהבהיר את הנזק ללב ולאיברים אחרים. עם תהליך ראומטי פעיל, בדיקות מעבדה חושפות שלב חריף לא ספציפי ופרמטרים אימונולוגיים משתנים. אינדיקטורים לשלב חריף: נויטרופיליה עם הסטת נוסחת הדם של לויקוציטים שמאלה; עלייה בתכולת 2-גלובולינים, ולאחריה עלייה ברמת - גלובולינים; עלייה בתכולת הפיברינוגן; הופעת חלבון C-reactive; ESR עולה. בהתייחס לפרמטרים אימונולוגיים, הטיטרים של נוגדנים אנטי-סטרפטוקוקלים עולים (אנטי-hyaluronidase ו-antistreptokinase יותר מ-1:300, אנטי-O-streptolysin יותר מ-1:250). האק"ג מגלה לעיתים הפרעות בקצב והולכה: חסימה אטריו-חנטרית חולפת (לעתים קרובות יותר I grad - הארכה של מרווח P-Q, לעתים רחוקות יותר - II Grade), אקסטרה-סיסטולה, קצב פרוזדורוני. במספר חולים נרשמת ירידה באמפליטודה של גל T עד להופעת שיניים שליליות. הפרעות הקצב וההולכה הללו אינן יציבות ונעלמות במהירות במהלך הטיפול האנטי-ראומטי. אם השינויים ב-ECG מתמשכים ונשארים לאחר חיסול התקף ראומטי, אז יש לחשוב על נזק אורגני לשריר הלב. במהלך בדיקה פונוקרדיוגרפית, מצוינים נתוני האזנה: היחלשות של הטון הראשון, הופעת הטון השלישי, אוושה סיסטולית. במקרה של היווצרות מחלת לב מופיעים שינויים ב-PCG התואמים את אופי הנגע המסתם. צילום רנטגן בהתקף הראשון של שיגרון, לא מתגלים שינויים. רק במחלת לב ראומטית קשה בילדים ובצעירים ניתן לזהות עלייה בלב עקב הרחבת החדר השמאלי. עם התפתחות מחלת לב ראומטית על רקע מחלת לב קיימת, תמונת הרנטגן תתאים לפגם ספציפי. מחקר אקו-קרדיוגרפי במחלת לב ראומטית ראשונית אינו מגלה שינויים אופייניים כלשהם. רק במחלת לב ראומטית קשה עם סימני אי ספיקת לב בבדיקת האקו-לב מראים סימנים המעידים על ירידה בתפקוד ההתכווצות של שריר הלב והתרחבות חללי הלב. אבחון. זיהוי שיגרון ראשוני קשה מאוד, שכן הביטויים השכיחים ביותר שלו, כגון דלקת מפרקים ונזק לבבי, אינם ספציפיים. נכון לעכשיו, הקריטריונים העיקריים והקטנים לראומטיזם של איגוד הלב האמריקאי נמצאים בשימוש הנרחב ביותר. השילוב של שני קריטריונים עיקריים או עיקריים אחד ושני קריטריונים מינוריים מצביע על סבירות גדולה יותר לראומטיזם רק במקרים של זיהום סטרפטוקוקלי קודם. עם תחילתה ההדרגתית של שיגרון, האבחנה התסמונתית שהציע AI Nesterov בשנת 1973 (ראה טבלה 2) משנה: תסמונת קלינית ואפידמיולוגית (קשר עם זיהום סטרפטוקוקלי); תסמונת קלינית ואימונולוגית (סימנים של הבראה לא מלאה, ארתרלגיה, רמות גבוהות של נוגדנים אנטי-סטרפטוקוקליים, כמו גם זיהוי של דיספרוטינמיה ואינדיקטורים לשלב חריף); תסמונת קרדיווסקולרית (זיהוי של דלקת לב, כמו גם נגעים חוץ-לביים) (ראה טבלה 3). לוח 2 קריטריונים לראומטיזם
לוח 3 דרגות של שיגרון
אבחון דיפרנציאלי. יש להבדיל בין דלקת מפרקים שגרונית לבין דלקת לא ראומטית (ראה טבלה 4). לוח 4 דלקת מפרקים שגרונית ולא ראומטית
המחלות והתסמינים הבאים חשודים ביחס לראומטיזם: 1) אנדוקרדיטיס; 2) דלקת שריר הלב; 3) פריקרדיטיס; 4) מומי לב; 5) הפרעות קצב והולכה; 6) אי ספיקת לב חריפה וכרונית; 7) מצב subfebrile ממושך; 8) אריתמה נודוסום; 9) אריתמה טבעתית; 10) גושים תת עוריים; 11) דלקת מפרקים אלרגית חריפה; 12) כוריאה. אף אחת מהתסמונות הקליניות המפורטות לעיל אינה ספציפית למחלה זו. רק שילוב של פתולוגיית לב עם לפחות סימפטום עיקרי חוץ-לבי אחד של שיגרון נותן סיבה לחשוד בראומטיזם. זיהוי מחלת לב ראומטית עצמה מתבצע על בסיס תסמינים כמו קוצר נשימה ודפיקות לב, עייפות, כאבים בלב והפרעות בקצב הלב, רעשים, לעיתים קצב דהירה והיחלשות בטון ה-I. חשיבות רבה באבחון של מחלת לב ראומטית היא זיהוי הפתולוגיה ב-ECG. בראומטיזם זה נגרם על ידי דלקת שריר הלב, פריקרדיטיס ומומי לב. התבוננות דינמית מאפשרת להבחין בין שינויים בלתי הפיכים האופייניים להיפרטרופיה של חלקים שונים של הלב במקרה של פגמים, מפגמים חולפים, המעידים על התהליך הדלקתי הנוכחי. טיפול. השפעה חיובית בטיפול, כמו גם מניעת התפתחות מחלות לב, מתאפשרת על ידי אבחון מוקדם וטיפול פרטני, המבוסס על הערכה של סוג הקורס, פעילות התהליך הפתולוגי, חומרת הקרדיטיס, והגרסה של מחלת לב מסתמית. יש חשיבות למצב של שריר הלב, רקמות ואיברים אחרים, מקצוע המטופל וכו'. לפיכך, כל מכלול הטיפול בראומטיזם מורכב מטיפול אנטי מיקרוביאלי ואנטי דלקתי, אמצעים שמטרתם לשחזר הומאוסטזיס אימונולוגי. מומלץ להשתמש בתזונה מאוזנת רציונלית, להתמקד בהסתגלות לפעילות גופנית, הכנה לעבודה, טיפול כירורגי בזמן בחולים עם מומי לב מורכבים. לכל החולים במהלך השלב הפעיל של שיגרון מוצג פניצילין (1-200 IU עבור 000 מנות ליום, כל 1 שעות), בעל השפעה חיידקית על כל סוגי A-streptococcus. מהלך הטיפול הוא שבועיים במהלך השלב הפעיל של שיגרון, בעתיד נדרשת העברה לתרופה ממושכת bicillin-500 (000 יחידות). עם אי סבילות לפניצילין, ניתן לרשום אריתרומיצין 6 מ"ג 4 פעמים ביום. תרופות בעלות השפעה אנטי דלקתית, המשמשות בטיפול המודרני של השלב הפעיל של שיגרון, הן גלוקוקורטיקוסטרואידים, סליציליק, נגזרות אינדול, נגזרות של חומצה פנילאצטית וכו '. פרדניזולון משמש במינון של 20-30 מ"ג ליום (למשך שבועיים, ואז המינון מופחת ב-2-2,5 מ"ג כל 5-5 ימים, בסך הכל במהלך של 7-1,5 חודשים) עבור ראשוני וחוזר עם III ו-II דרגת פעילות של תהליך של מחלת לב ראומטית, עם polyserositis ו chorea, עם התפתחות של אי ספיקת לב עקב קרדיטיס פעיל. במקרה האחרון, עדיף טריאמצינולון במינון של 2-12 מ"ג ליום, שכן יש לו יכולת מועטה להפר את מאזן האלקטרוליטים. סוכני קורטיקואידים משפיעים על חילוף החומרים של מים-מלח, לכן, יש להשתמש באשלגן כלוריד 3-4 גרם ליום, panangin ואחרים בטיפול, עם אגירת נוזלים - אנטגוניסטים של אלדוסטרון (ורושפירון עד 6-8 טבליות ביום), משתנים (lasix). 40 -80 מ"ג ליום, פורוסמיד 40-80 מ"ג ליום וכו'), עם אופוריה - תרופות הרגעה וכו'. תרופות נוגדות דלקת לא סטרואידיות נמצאות בשימוש נרחב גם לראומטיזם: מינונים ממוצעים של חומצה אצטילסליצילית הם 3-4 גרם ליום, לעתים רחוקות יותר 5 גרם ליום או יותר. אינדיקציות לשימוש בסליצילטים: 1) דרגת פעילות מינימלית, חומרה קלה של קרדיטיס, בעיקר שריר הלב; 2) טיפול ארוך טווח בראומטיזם, חשד למהלך סמוי; 3) טיפול ממושך עם ירידה בפעילות מהלך התהליך והפסקת השימוש בקורטיקוסטרואידים וכן לאחר סיום הטיפול בבית חולים; 4) מחלת לב ראומטית חוזרת המופיעה על רקע מומי לב חמורים ואי ספיקת מחזור הדם, שכן הסליצילטים אינם מסוגלים לשמר נוזלים, למנוע היווצרות קרישי דם ומהווים ממריצים של מרכז הנשימה; 5) הפחתת הסבירות להחמרה של שיגרון בתקופות האביב והסתיו, כמו גם לאחר סבל מזיהומים אינטראקטיביים (יחד עם אנטיביוטיקה). חומצה אצטילסליצילית משמשת 1 גרם 3-4 פעמים ביום לאחר ארוחות במשך 1-3 חודשים או יותר עם סבילות רגילה ובכפוף לשליטה בתופעות הלוואי. השימוש המוצלח בנגזרת חומצה אינדולאצטית - אינדומתצין בראומטיזם במשך יותר מ-20 שנה. יש לו השפעה טיפולית בולטת: תסמינים סובייקטיביים של קרדיאלגיה (לב, דפיקות לב, קוצר נשימה) נעלמים ביום ה-8-10 של הטיפול, וסימנים אובייקטיביים - עד היום ה-14-16. היעלמותן של דלקת מפרקים ופוליסרוסיטיס מתרחשת אפילו מהר יותר. בטיפול בראומטיזם יש חשיבות לשילוב של שלושה שלבים עיקריים: בית חולים - מרפאה - נופש. בבית החולים מתבצע הטיפול בתרופות המפורטות לעיל. לאחר הפחתת פעילות השיגרון ונורמליזציה של מצב החולה, הם מועברים לשלב II - טיפול בסנטוריום ראומטולוגי. המטרה העיקרית של שלב זה היא המשך הטיפול בתרופות נוגדות דלקת לא סטרואידיות, הנבחרות באופן פרטני בבית החולים, נגזרות אמינוקינולין, ביצילין-5, שיקום. שלב III כולל תצפית מרפאה וטיפול מונע. זהו יישום אמצעים טיפוליים שמטרתם ביטול סופי של המהלך הפעיל של התהליך הראומטי; ביצוע טיפול סימפטומטי בהפרעות במחזור הדם בחולים עם מחלת לב; פתרון סוגיות של שיקום, כושר עבודה ותעסוקה; יישום מניעה ראשונית של שיגרון ומניעה משנית של הישנות המחלה. הרצאה מס' 2. מחלות של מערכת הלב וכלי הדם. קרדיומיופתיה. קרדיומיופתיה מורחבת 1. קרדיומיופתיה קרדיומיופתיה - נגעים ראשוניים מבודדים בשריר הלב בעלי אופי לא דלקתי של אטיולוגיה לא ידועה (אידיופתית), הם אינם קשורים לפגמים במסתמים או שאנטים תוך-לביים, יתר לחץ דם עורקי או ריאתי, מחלת לב כלילית או מחלות מערכתיות (כגון: קולגנוזות, עמילואידוזיס, המוכרומטוזיס, וכדומה), ובשלב הסופי של המחלה מתפתחים אי ספיקת לב חמורה והפרעות מורכבות בקצב הלב והסבלנות. הסיווג של קרדיומיופתיה הוא כדלקמן: 1) קרדיומיופתיה מורחבת: א) אידיופתי; ב) רעיל; ג) מדבק; ד) עם קולגנוזות; 2) היפרטרופי; 3) מגביל; 4) דיספלזיה אריתמית של החדר הימני; 5) שילוב של אחד מ-4 סוגי קרדיומיופתיה עם יתר לחץ דם עורקי. 2. קרדיומיופתיה מורחבת קרדיומיופתיה מורחבת (DCM) היא מחלה של שריר הלב המאופיינת בהתרחבות מפוזרת של כל חדרי הלב (בעיקר החדר השמאלי), שבה הפתולוגיה של תפקוד השאיבה של הלב נמצאת בחזית וכתוצאה מכך. , אי ספיקת לב כרונית (מכאן השם השני הוא גודש, כאשר הלב אינו מסוגל לשאוב דם במלואו והוא "מקופא" ברקמות ואיברי הגוף). הדופן השרירי של הלב נשאר ללא שינוי או היפרטרופיה בדרגות שונות. מחלות וגורמים שקדמו להתפתחות DCM מתוארים בטבלה שלהלן (ראה טבלה 5). לוח 5 מחלות וגורמים שקדמו להתפתחות DCMP
זוהי הצורה הנפוצה ביותר של נזק לשריר הלב. השכיחות היא 5-8 מקרים לכל 100 איש בשנה. אין היסטוריה משפחתית ברורה לחולים אלו. גברים חולים פי 000-2 יותר מנשים. פתוגנזה. כתוצאה מהתהליך הדלקתי בשריר הלב (מיוקרדיטיס), מתרחש מוות של תאים בודדים בחלקיו השונים. במקרה זה, הדלקת היא ויראלית במהותה, ותאים המושפעים מהנגיף הופכים לגורמים זרים עבור הגוף. בהתאם לכך, כאשר מופיעים אנטיגנים בגוף, מתפתח קומפלקס של תגובות תגובה חיסונית שמטרתם להשמידם. בהדרגה, תאי שריר מתים מוחלפים ברקמת חיבור, שאין לה יכולת הרחבה והתכווצות הגלומה בשריר הלב. כתוצאה מאובדן תפקודים בסיסיים של שריר הלב, הלב מאבד את יכולתו לתפקד כמשאבה. בתגובה לכך (כתגובה מפצה), חדרי הלב מתרחבים (כלומר, הם מתרחבים), ובחלק הנותר של שריר הלב מתרחשת עיבוי ודחיסה (כלומר, מתפתחת היפרטרופיה שלו). כדי להגביר את אספקת החמצן לאיברים ולרקמות הגוף, מתרחשת עלייה מתמשכת בקצב הלב (טכיקרדיה סינוס). תגובה מפצה זו רק משפרת באופן זמני את תפקוד השאיבה של הלב. עם זאת, האפשרויות של הרחבת שריר הלב והיפרטרופיה מוגבלות על ידי כמות שריר הלב הקיימא והן אינדיבידואליות לכל מקרה ספציפי של המחלה. עם המעבר של התהליך לשלב הדקומפנסציה מתפתחת אי ספיקת לב כרונית. אולם בשלב זה נכנס לתמונה מנגנון פיצוי נוסף: רקמות הגוף מגבירות את שאיבת החמצן מהדם בהשוואה לגוף בריא. אך מנגנון זה אינו מספק, שכן ירידה בתפקוד השאיבה של הלב מביאה לירידה באספקת החמצן לאיברים ולרקמות, הנחוצה לתפקודם התקין, בעוד שכמות הפחמן הדו חמצני בהם עולה. ב-2/3 מהחולים בחללי החדרים בשלבים המאוחרים של המחלה נוצרים פקקים פריאטליים (עקב ירידה בתפקוד השאיבה של הלב וכן התכווצות לא אחידה של שריר הלב בחדרי הלב ), ואחריו התפתחות של תסחיף במחזור הריאתי או המערכתי. שינויים פתוהיסטולוגיים ופתומורפולוגיים בלב. צורת הלב הופכת לכדורית, המסה שלו עולה מ-500 ל-1000 גרם, בעיקר בגלל החדר השמאלי. שריר הלב הופך לרופף, עמום, עם שכבות לבנבנות ניכרות של רקמת חיבור, ישנה חילופין אופיינית של קרדיומיוציטים היפרטרופיים ואטרופיים. מיקרוסקופית מתגלה פיברוזיס מפוזר, ניתן לשלב אותה עם ניוון והיפרטרופיה של קרדיומיוציטים, בהם יש עלייה משמעותית בנפח הגרעינים, מספר המיטוכונדריות, היפרפלזיה של מנגנון גולגי, עלייה במספר המיופיברילים. , חופשי ומזוהה עם הריבוזומים של הרשת האנדופלזמית, שפע של גרגירי גליקוגן. תמונה קלינית. אין סימנים ספציפיים למחלה. התמונה הקלינית היא פולימורפית ונקבעת על ידי: 1) תסמינים של אי ספיקת לב; 2) הפרעות קצב והולכה; 3) תסמונת תרומבואמבולית. כל התופעות הללו מתפתחות בשלב הסופני של המחלה, ולכן ההכרה ב-DCM לפני הופעת התסמינים הללו מעוררת קשיים משמעותיים. ברוב המקרים, הפרוגנוזה של המחלה נקבעת על ידי התבוסה של החדר השמאלי של הלב. לפני תחילת אי ספיקת לב, DCM הוא סמוי. התלונות השכיחות ביותר על אי ספיקת לב שכבר החלה הן תלונות על ירידה בביצועים, עייפות מוגברת, קוצר נשימה בזמן מאמץ ולאחר מכן במנוחה. בלילה יש לו שיעול יבש (שווה ערך לאסטמה לבבית), מאוחר יותר - התקפי אסטמה אופייניים. חולים מציגים כאב אנגינאלי אופייני. עם התפתחות גודש במחזור הדם, מופיעה כבדות בהיפוכונדריום הימני (עקב הרחבת הכבד), נפיחות ברגליים. אבחון. בעת אבחון המחלה, סימן חשוב הוא הגדלה משמעותית של הלב (אין סימנים למחלת לב מסתמית או יתר לחץ דם עורקי). קרדיומגליה מתבטאת בהתרחבות של הלב לשני הכיוונים, הנקבעת על ידי הקשה, כמו גם תזוזה של הדחף האפיקי שמאלה ולמטה. במקרים חמורים, נשמעים קצב דהירה, טכיקרדיה וקולות של אי ספיקה יחסית של המסתמים המיטרליים או התלת-צדדיים. ב-20% מהמקרים מתפתח פרפור פרוזדורים. לחץ הדם הוא בדרך כלל תקין או מעט מוגבר (עקב אי ספיקת לב). מחקרים ביוכימיים של דם ושתן יכולים לזהות חומרים רעילים שונים, כמו גם מחסור בוויטמינים. שיטות מחקר אינסטרומנטליות מאפשרות לזהות: 1) סימנים של קרדיומגליה; 2) שינויים באינדיקטורים להמודינמיקה מרכזית; 3) הפרעות קצב והולכה. ה-EKG אינו מראה שינויים אופייניים או שהשינויים אינם ספציפיים. מדובר בסימנים של עלייה בגודל הלב, הפרעות הולכה בצורת חסימה של הענף הקדמי של הרגל השמאלית של הצרור האטריואטריקולרי (His bundle) או חסימה מלאה של רגל שמאל (15% מהמקרים). ); כמו גם טכיקרדיה מתמשכת בסינוס (קצב הלב עולה לרוב על 100 פעימות לדקה). הפונוקרדיוגרמה מאשרת נתונים אוסקולטוריים בצורה של קצב דהירה, זיהוי תכוף למדי של אוושה סיסטולית (עקב אי ספיקה יחסית של המסתם המיטרלי או התלת-צדדי). עם גודש במחזור הדם הריאתי, מתגלה מבטא של הטון II. צילום רנטגן מגלה עלייה משמעותית בחדרים (לעתים קרובות בשילוב עם עלייה מתונה באטריום השמאלי) וסטגנציה של דם במחזור הדם הריאתי (הקטן). הפרות במחזור הדם הריאתי מתבטאות בעלייה בדפוס כלי הדם הריאתי, כמו גם הופעת טרנסודאט בחללי הצדר, הנוצר עקב לחץ מוגבר בכלי הריאות. שיטת האקו לב היא אחת השיטות העיקריות באבחון המחלה. אקו לב עוזר לזהות התרחבות של שני החדרים, היפוקינזיה של הקיר האחורי של החדר השמאלי, תנועה פרדוקסלית של המחיצה הבין חדרית במהלך הסיסטולה. בנוסף, אקו לב מאפשר לך להבהיר את העלייה במשרעת התנועה של העלונים ללא שינוי של המסתם המיטרלי. מחקרים אינסטרומנטליים נוספים אינם חובה לקביעת אבחנה, אולם תוצאותיהם מאפשרות לפרט את מידת ההפרעות ההמודינמיות ואת אופי השינויים המורפולוגיים בשריר הלב. מחקר רדיואיזוטופי של הלב (סינטיגרפיה שריר הלב) מבוצע כדי להבהיר את מצב תפקוד השאיבה של הלב, כמו גם כדי לקבוע את אזורי שריר הלב המת. מחקר האינדיקטורים של המודינמיקה המרכזית מגלה נפח דקות ושבץ נמוך (מדדי דקות ושבץ), עליה בלחץ בעורק הריאתי. מבחינה אנגיוקרדיוגרפית, מתגלים אותם שינויים כמו בבדיקת האקו לב. ביופסיה חיה של שריר הלב אינה אינפורמטיבית לקביעת האטיולוגיה של קרדיומיופתיה. במקרים מסוימים ניתן לזהות בביופסיה אנטיגן ויראלי או עלייה בתכולת LDH וכן ירידה בייצור האנרגיה על ידי המיטוכונדריה. עם זאת, ניתן להשתמש בשיטה כירורגית זו כדי להבהיר את האטיולוגיה של המחלה וטיפול נוסף. המניפולציה מתבצעת באופן הבא: תחת הרדמה מקומית, עורק ווריד גדולים מחוררים (מחוררים), ואז מעבירים מכשיר מיוחד עם מספריים קטנות בקצהם לאורך המסלול שלהם אל הלב. כאשר ביופסיה של שריר הלב משולבת עם אנגיוגרפיה כלילית (הזרקת חומר ניגוד לעורקים הכליליים המספקים את הלב), ניתן לשלול מחלת עורקים כליליים בחולה כאחת המחלות שיש להן תסמינים דומים ל-DCM. שני מחקרים אלו מבוצעים תחת בקרת טלוויזיית רנטגן. אבחון דיפרנציאלי. היא מבוצעת בעיקר עם דלקת שריר הלב והדיסטרופיה של שריר הלב, כלומר עם אותם מצבים הנקראים לעיתים באופן בלתי סביר קרדיומיופתיה משנית. ביופסיה של שריר הלב מספקת סיוע משמעותי באבחנה מבדלת של קרדיומיופתיה מורחבת ומחלות לב המתרחשות עם עליה בולטת: 1) עם דלקת שריר הלב המפוזרת חמורה, חדירה תאית של הסטרומה נמצאת בשילוב עם שינויים דיסטרופיים ונמקיים בקרדיומיוציטים; 2) עם עמילואידוזיס ראשונית המתרחשת עם נזק ללב (מה שנקרא גרסה קרדיופתית של עמילואידוזיס ראשונית), יש שקיעה משמעותית של עמילואיד ברקמת הביניים של שריר הלב, בשילוב עם ניוון של סיבי שריר; 3) עם המוכרומטוזיס (מחלה הנגרמת על ידי הפרה של חילוף החומרים של ברזל), משקעים של פיגמנט המכיל ברזל נמצאים בשריר הלב, נצפות דרגות שונות של ניוון וניוון של סיבי שריר, והתפשטות של רקמת חיבור. כגרסה של DCM, ניתן לשקול קרדיומיופתיות רעילות הנגרמות על ידי תרופות. חומרים רבים עלולים לגרום לנזק רעיל לשריר הלב: אתנול, אמטין, ליתיום, קדמיום, קובלט, ארסן, איזופרוטרנול ורעלים אחרים. שינויים היסטופתולוגיים ברקמות שריר הלב מופיעים כדיסטרופיה מוקדית. בעתיד מתרחשת התפתחות של מיקרו-אוטמים, המלווה בתגובה דלקתית היקפית. הדוגמה הבולטת ביותר לקרדיומיופתיה רעילה היא קרדיומיופתיה, המופיעה אצל אנשים שצורכים בירה מוגזמת. זה נובע מהנוכחות של קובלט בו, שמתווסף לבירה כדי לשפר את הקצף. קובלט חוסם את פעולת ויטמין B1, וגם משפיע ישירות על השינוי בתהליכים האנזימטיים של התא. בשלב החריף של מהלך הקרדיומיופתיה של קובלט, מציינים נוכחות של ניוון הידרופי ושומני, הרס של אברונים תוך-תאיים ונמק מוקדי של קרדיומיוציטים. בעתיד מתפתחת פיברוזיס אינטרסטיציאלי מפוזר או קטן מוקד, התוצאה הסופית היא היווצרות של צלקות נרחבות. קרדיומיופתיה קובלט חמורה יותר מקרדיומיופתיה אלכוהולית. אם האבחנה נעשית בזמן, נצפתה ריפוי קליני של חולים. קרדיומיופתיה אלכוהולית. לאתנול יש השפעה רעילה ישירה על קרדיומיוציטים. בנוסף, עם שיכרון אתיל כרוני, יש לעתים קרובות חוסר תזונה. הוכח כי אלכוהול מוביל להצטברות חומצות שומן בקרדיומיוציטים, שכן יש מחסור באנרגיה, הנחוצה לפעילותם. אצטלדהיד, שנוצר במהלך חילוף החומרים של אלכוהול, יכול להיות גורם להשפעות רעילות ישירות על סינתזת חלבון. אלכוהוליזם מלווה גם בהפעלה של וירוסים סמויים. מבחינה מקרוסקופית, שריר הלב רופף, דמוי חימר, לפעמים נצפות צלקות קטנות. העורקים הכליליים שלמים. בדיקה מיקרוסקופית מראה שילוב של דיסטרופיה (הידרופית ושומנית), ניוון והיפרטרופיה של קרדיומיוציטים, יתכנו מוקדים של תמוגה של קרדיומיוציטים וטרשת. האזורים הפגועים של שריר הלב מנוגדים לאלו שלא השתנו. בדיקה מיקרוסקופית אלקטרונית של דגימות ביופסיה לב מראה התרחבות ציסטית של הרשת הסרקופלזמית ומערכת ה-T של קרדיומיוציטים, האופיינית לקרדיומיופתיה אלכוהולית. סיבוכים של קרדיומיופתיה אלכוהולית - מוות פתאומי כתוצאה מפרפור חדרים או אי ספיקת לב כרונית, תסמונת תרומבואמבולית. טיפול. טיפול בקרדיומיופתיה הוא משימה קשה, שכן הגורמים הספציפיים להופעתם אינם ידועים. העקרונות הכלליים של הטיפול ב-DCM אינם שונים באופן משמעותי מהטיפול באי ספיקת לב כרונית. במקרים של DCM שניוני מטופלת בנוסף במחלה הקודמת (מחלת מסתמי לב וכו') וננקטים כל האמצעים להעלמת הגורמים ל-DCM. למעשה, אנו יכולים לדבר על טיפול בחולים עם קרדיומיופתיה רק כאשר מופיעים סימנים קליניים. באי ספיקת לב, גליקוזידים לבביים אינם יעילים. חולים מפתחים במהירות אי סבילות לתרופות (שיכרון גליקוזידים), ולכן יש צורך להשתמש בגליקוזידים המופרשים במהירות מהגוף (סטרופנטין, איזולאניד). מרחיבי כלי דם היקפיים יעילים למדי, במיוחד עם תסמונת אנגינאלית נלווית (ניטרונג, sustak, nitrosorbide). יש לרשום תרופות אלו לאי ספיקת לב חמורה, קשה לטיפול באמצעות גליקוזידים ומשתנים. עם תסמונת אנגינאלית, יש צורך להשתמש בתרופות אנטי-אנגינליות, רצוי חנקות ממושכות (sustak, nitrong, nitrosorbid). חוסמי אדרנו יעילים (הם נקבעים בהיעדר סימנים של אי ספיקת לב). מבין השיטות המודרניות לטיפול כירורגי של DCMP, היעילה ביותר היא השתלת לב (השתלה). עם זאת, האפשרויות לבצע פעולה זו מוגבלות באופן משמעותי. מסיבה זו, כחלופה להשתלת לב בטיפול המודרני, להגדלת תוחלת החיים של חולי DCMP, פותחו ומתבצעים ניתוחים משחזרים, שמטרתם להעלים אי ספיקה של מסתמי הלב המיטרלי והתלת-צדדי. חיסול אופרטיבי של אי ספיקה של שסתומים אלה מאפשר לזמן מה "להאט" את תחילת השלב הסופי של המחלה. חלופה נוספת להשתלת לב בחולים עם DCM הייתה הסרה חלקית של החדר השמאלי על מנת להקטין את גודלו (פעולת בפטיסט). לא כל כך מזמן, לטיפול בחולים עם DCMP, פותחו מודלים מיוחדים של קוצבי לב, הם מאפשרים לך להפוך את העבודה של חדרי הלב לסינכרונית. הדבר מביא לשיפור במילוי חדרי הלב בדם ולעלייה בתפקוד השאיבה של הלב. נושא נפרד צריך להיחשב DCM בילדים, שהוא 5-10 מקרים לכל 100 ילדים בשנה. ראוי לציין כי המחלה יכולה להתפתח בקבוצות גיל שונות, כולל תינוקות. הנתונים שהתקבלו במחקר על קבוצת ילדים הם כדלקמן: חולים קיבלו 000 אפשרויות טיפול (מונותרפיה עם פרדניזולון, מונותרפיה עם דיגוקסין או פרדניזולון + דיגוקסין). יעילות הטיפול הוערכה לפי הקריטריונים הבאים: קצב הלב נקבע לפני ואחרי הטיפול, קצב הנשימה, מצב שבר הפליטה וקטע ההתכווצות. ניתוח התוצאות שהתקבלו מראה כי ההשפעה הגדולה ביותר בטיפול בקרדיומיופתיה מורחבת בילדים צעירים מושגת בשילוב של קורטיקוסטרואידים וגליקוזידים (פרדניזולון ודיגוקסין). לאחר השלמת המהלך העיקרי של הטיפול (פרדניזולון במתן 3 מ"ג/ק"ג ליום במשך 2 ימים, דיגוקסין), חלה ירידה ניכרת בקצב הלב, ירידה בקוצר הנשימה. על רקע מונותרפיה עם פרדניזולון, מתרחשת ירידה בקצב הלב. מונותרפיה עם דיגוקסין מובילה לירידה בטכיקרדיה וקוצר נשימה. בהתחשב בחוסר המומלץ לרשום תרופות ציטוסטטטיות בילדים צעירים, מאחר ונצפו מספר לא מבוטל של סיבוכים בטיפול, עדיף ברפואת ילדים להשתמש בגליקוזידים לבביים ארוכי טווח בשילוב עם הורמונים קורטיקוסטרואידים לקרדיומיופתיה מורחבת. מניעה. מניעה של DCM כוללת הימנעות מאלכוהול, קוקאין ומעקב קפדני אחר פרמטרים לבביים במהלך כימותרפיה של הגידול. זה שימושי להקשיח את הגוף מגיל צעיר. הימנעות מוחלטת מאלכוהול ב-DCM אלכוהולי משפרת את התכווצות הלב ועשויה לבטל את הצורך בהשתלת לב. העובדה שברוב המקרים האבחנה מתרחשת בשלב של אי ספיקת לב יכולה להוביל גם לתוצאות שליליות בטיפול. אבחון מוקדם של קרדיומיופתיה מורחבת יכול להתבצע באמצעות אקוקרדיוגרפיה אקראית (הקרנה), המתבצעת במהלך הבדיקה הרפואית השנתית, וכן בעת בדיקת אנשים עם תורשה הסובלים ממחלה זו. במקרה זה ניתן להגביר את יעילות הטיפול התרופתי ב-DCM. הרצאה מס' 3. מחלות של מערכת הלב וכלי הדם. קרדיומיופתיה היפרטרופית קרדיומיופתיה היפרטרופית (HCM) היא מחלה לא כלילית של שריר הלב החדרי (בעיקר השמאלי), המאופיינת בהיפרטרופיה מסיבית של הקירות שלהם עם בליטה של המחיצה הבין חדרית (IVS) לתוך חלל החדר הימני, אשר יכול להיות מעובה באופן משמעותי. , ירידה בנפח הפנימי של החדרים, התכווצות תקינה או מוגברת של שריר הלב החדרים ופגיעה בהרפיה (הפרעה דיאסטולית). השכיח ביותר הוא היפרטרופיה מבודדת של המחיצה הבין-חדרית (היצרות היפרטרופית תת-אאורטית מבודדת - IHSS) או החלק האפיקלי של החדרים. מיון. סיווג HCM לפי לוקליזציה של היפרטרופיה (ED Wigle et al., 1985 עם תוספות). I. LV היפרטרופיה. 1) היפרטרופיה א-סימטרית, שבה מתרחשת היפרטרופיה של שריר הלב של דפנות בודדות או מקטעים של החדרים (כולל היפרטרופיה של IVS - 90% עם או בלי חסימת דרכי יציאה של החדר השמאלי, אמצע החדר - 1%, היפרטרופיה של החדר השמאלי העליון - 3%, היפרטרופיה של הקיר החופשי חדר שמאל וחלק אחורי של IVS - 1%). 2) היפרטרופיה סימטרית (קונצנטרית) של החדר השמאלי, כאשר היפרטרופיה של שריר הלב משתרעת על כל דפנות החדרים, מתרחשת ב-5% מהמקרים. II. היפרטרופיה של הלבלב. במקרה שבו היפרטרופיה של שריר הלב מונעת יציאה תקינה של דם מחדרי הלב, הם מדברים על צורה חסימתית של HCM. במקרים אחרים, HCM אינו חסימה. אטיולוגיה. המחלה יכולה להיות מולדת או נרכשת. HCM מולד עובר בתורשה באופן אוטוזומלי דומיננטי. בתוך אותה משפחה, ניתן לראות צורות וגרסאות שונות של HCM. לרוב, היפרטרופיה אסימטרית של המחיצה הבין חדרית עוברת בתורשה. הצורה הנרכשת של HCM מתרחשת בחולים קשישים עם היסטוריה של יתר לחץ דם עורקי. השכיחות היא 0,02-0,05%. הסיבות להתפתחות HCM נרכש אינן מובנות במלואן. על פי אחת ההשערות המוצעות, אנשים עם HCM נרכש בתקופה שלפני הלידה מפתחים פגם בקולטנים האדרנרגיים של הלב המעורבים בוויסות פעילות הלב, בפרט קצב הלב. כתוצאה מכך, הרגישות לנוראדרנלין והורמונים דומים, המגבירים את קצב הלב, עולה משמעותית, מה שמשפיע על התפתחות היפרטרופיה של שריר הלב בהם, ובסופו של דבר HCM. תמונה פתואיסטולוגית. סידור מבולבל, שגוי, כאוטי של קרדיומיוציטים ומיופיברילים בקרדיומיוציטים, פיברוזיס שריר הלב הוא הפרה של הארכיטקטוניקה של שריר הלב. פתוגנזה. הפרעות המודינמיות נוצרות עקב פגיעה בתפקוד הדיאסטולי של הלב. במהלך הדיאסטולה, לא זורם מספיק דם לחדרים (במיוחד השמאלי) עקב צפיפותם וקשיחותם, מה שמוביל לעלייה מהירה בלחץ הקצה הדיאסטולי. גם נוקשות מוגברת של שריר הלב וגם לחץ תוך-חדרי מוגבר גורמים לפליטת פחות דם מהחדר במהלך הסיסטולה. לאספקה נאותה של חמצן לאיברים ולרקמות הגוף (עם תפקוד תקין של מערכת הלב וכלי הדם), ליישום כל עומס, שחרור הדם מהלב חייב להגביר. בהתאם לכך, בתגובה לעומס, קצב הלב עולה. עם התפתחות HCM, התמלאות הלב בדם סובלת במנוחה, ועם עלייה בקצב הלב במהלך תקופת הפעילות הגופנית היא מושפעת לרעה אף יותר. כתוצאה מכך, אין עלייה נאותה בתפקוד השאיבה של הלב במהלך פעילות גופנית ב-HCM. פעילות גופנית ב-HCM משפיעה על העלייה בלחץ התוך-חדרי, מה שמוביל לעלייה בלחץ באטריום השמאלי הממוקם מעל, כמו גם בכלי הדם הקטנים (ריאתיים). בתנאים אלו מתפתחים תפקוד יתר והיפרטרופיה של הפרוזדור השמאלי, ובהמשך - יתר לחץ דם ריאתי ("פאסיבי"). כתוצאה מכך נוצר קוצר נשימה, שהוא פרופורציונלי למידת העומס. מכיוון שבמהלך פעילות גופנית פליטת הדם מהחדר השמאלי אינה תואמת את העלייה בעומס, זרימת הדם בעורקים הכליליים המזינים את שריר הלב עצמו מתחילה לסבול. ממלא תפקיד חשוב והעובדה שב-HCM יש אי התאמה בין מסה משמעותית של שריר הלב עם היפרטרופיה לבין האפשרות של אספקת דם כלילי, שנשאר זהה לזו של אנשים בריאים. הירידה בזרימת הדם דרך העורקים הכליליים מובילה להופעה של אנגינה פקטוריס באמצע ובחצי השמאלי של בית החזה, המקרינה לזרוע השמאלית, מתחת לכתף השמאלית. כמו קוצר נשימה, אנגינה פקטוריס מתעוררת על ידי מאמץ פיזי. במקרים מסוימים של HCM במהלך פעילות גופנית, גם אספקת הדם המוחי מתדרדרת, וכתוצאה מכך לסינקופה. יש לציין כי כדי להפחית את העלייה בלחץ התוך-חדרי במהלך פעילות גופנית, קיים מנגנון פיצוי, אשר פעולתו מבוססת על כך שחלל הפרוזדור השמאלי מתרחב, ועובי הדפנות שלו גדל. כתוצאה מכך, יש מילוי נוסף של החדר השמאלי בדם במהלך פעילות גופנית. עם זאת, מדובר בפיצוי זמני בלבד בשל העובדה שרזרבה של הפרוזדור השמאלי כ"משאבה" אינה משמעותית, והרחבה משמעותית של חלל הפרוזדור השמאלי מביאה להתפתחות פרפור פרוזדורים. תמונה קלינית. HCM מאופיין במגוון קיצוני של תסמינים, הגורם לאבחון שגוי. נוכחות ותזמון התלונות ב-HCM נקבעים בעיקר על ידי 2 גורמים: צורת ה-HCM ומיקום הנגע. החדר החזק ביותר של הלב הוא החדר השמאלי, ולכן, עם היפרטרופיה של דפנות שריר הלב, תלונות עשויות שלא להופיע במשך זמן רב. נזק מבודד לחדר ימין של הלב הוא נדיר ביותר. בצורה הלא חסימתית של HCM, כאשר שום דבר לא מפריע ליציאת הדם מהחדר, ייתכן שהמטופל לא יציג תלונות כלשהן. לעיתים יתכנו קוצר נשימה (עם מאמץ פיזי משמעותי), הפרעות בעבודת הלב וכן דופק לא סדיר. בצורה חסימתית של HCM, פליטת הדם מהלב במהלך פעילות גופנית מופחתת באופן משמעותי עקב הימצאות חסימה ליציאת הדם מהחדר. במקרה זה, התלונות האופייניות הן קוצר נשימה במאמץ, אנגינה פקטוריס והתעלפות. המחלה מאופיינת בהתקדמות איטית של התלונות מרגע הופעתה. בשל הדמיון בין התלונות (כאבים באזור הלב ומאחורי עצם החזה) ונתוני המחקר (אוושה סיסטולית חזקה), מחלת לב שגרונית ומחלת לב כלילית מאובחנים לרוב בטעות. התמונה הקלינית של HCM היא: 1) סימנים של היפרטרופיה של שריר הלב חדרית (בעיקר משמאל); 2) סימן לתפקוד חדרי דיאסטולי לא מספיק; 3) סימנים משתנים של חסימת דרכי יציאה של חדר שמאל. אבחון. בתהליך החיפוש האבחוני, המשמעותי ביותר הוא זיהוי של אוושה סיסטולית, שינוי בדופק ודחף אפיקלי עקירה. לתמונת ההשמעה של הלב בחולים עם HCM חסימתית יש מספר מאפיינים: הצליל המרבי של האוושה הסיסטולית (אוושה פליטה) נקבע בנקודת בוטקין ובקודקוד הלב, חומרת האוושה פרופורציונלית ל- מידת החסימה, התעצמותה מתרחשת כאשר המטופל קם בפתאומיות, כמו גם במהלך בדיקת Valsalva; הטון השני נשמר תמיד; רעש אינו מתבצע על כלי הצוואר. הדופק בדרך כלל גבוה ומהיר. זאת בשל היעדר היצרות בדרכי היציאה מהחדר השמאלי בתחילת הסיסטולה, אך לאחר מכן, עם התכווצות שרירים חזקים, מופיעה היצרות "פונקציונלית" של דרכי היציאה, וכתוצאה מכך הדופק. גל יורד בטרם עת. פעימת הקודקוד בכ-1/3 מהמקרים היא בעלת אופי "כפול": בהתחלה, במישוש, מורגשת מכה מהתכווצות הפרוזדור השמאלי, ואז מהתכווצות החדר השמאלי. לנוחות זיהוי תכונה זו של פעימת הקודקוד, המישוש נעשה בצורה הטובה ביותר כאשר המטופל שוכב על צידו השמאלי. לאבחון של HCM, נתוני אקו לב הם בעלי החשיבות הגדולה ביותר, המאפשרים להבהיר את המאפיינים האנטומיים של המחלה, את חומרת ההיפרטרופיה של שריר הלב, חסימה של דרכי היציאה של החדר השמאלי. מתגלים הסימנים הבאים: היפרטרופיה אסימטרית של IVS, בולטת יותר בשליש העליון, היפוקינזיס שלו; תנועה סיסטולית של העלון הקדמי של המסתם המיטרלי בכיוון הקדמי; מגע של העלון הקדמי של המסתם המיטרלי עם IVS בדיאסטולה. סימנים לא ספציפיים הם: היפרטרופיה של הפרוזדור השמאלי, היפרטרופיה של הקיר האחורי של החדר השמאלי, ירידה במהירות הממוצעת של הכיסוי הדיאסטולי של העלה הקדמית של המסתם המיטרלי. ב-ECG, כל שינוי ספציפי נמצא רק עם היפרטרופיה של חדר שמאל מפותח מספיק. על ידי רישום אק"ג למשך 24 שעות (ניטור הולטר), מתגלות הפרעות קיימות בקצב הלב. בדיקת א.ק.ג עם פעילות גופנית במינון באמצעות ארגומטר אופניים או הליכון מאפשרת להעריך את חומרת תסמיני המחלה, הפרוגנוזה שלה ולפתח טיפול מתאים. היפרטרופיה מבודדת של IVS גורמת לעלייה באמפליטודה של גל Q ב-Leads בחזה השמאלי (V5-6), מה שמקשה על האבחנה המבדלת עם שינויים מוקדיים עקב אוטם שריר הלב. עם זאת, רוחב קטן של גל Q מאפשר להוציא אוטם שריר הלב. בתהליך של התפתחות עומס יתר המודינמי של הפרוזדור השמאלי, האק"ג עשוי להראות סימנים של היפרטרופיה של פרוזדור שמאל: התרחבות גל P במשך יותר מ-0,10 שניות, עליה. במשרעת שלו, הופעת גל P דו-פאסי בעופרת V1 כאשר השלב השני גדל באמפליטודה ומשך הזמן. אבחון רנטגן חשוב רק בשלב המתקדם של המחלה, כאשר ניתן לקבוע עלייה בחדר השמאלי ובאטריום השמאלי, הרחבה של החלק היורד של אבי העורקים. בפונוקרדיוגרמה נשמרות המשרעות של צלילי I ו-II, המהווה סימן דיפרנציאלי של HCM מהיצרות של פתח אבי העורקים, ומתגלה גם אוושה סיסטולית בחומרה משתנה. שיטות מחקר פולשניות (חיטוט בחלקים השמאליים של הלב, אנגיוגרפיה ניגודיות) אינן חובה כיום, שכן אקו לב מספק מידע אמין למדי לצורך ביצוע אבחנה. עם זאת, לעיתים משתמשים בשיטות אלו במקרים שנויים במחלוקת על מנת להבהיר את האבחנה או בהכנת המטופלים לניתוח. בדיקה לבבית משמשת תחת בקרת טלוויזיית רנטגן. טכניקה לביצוע השיטה: על ידי ניקור עורק גדול בהרדמה מקומית עם המשך הכנסת צנתר מיוחד לחלל הלב, נמדד שיפוע הלחץ (ההבדל) בין החדר השמאלי לאבי העורקים היוצא ממנו. בדרך כלל, שיפוע זה לא צריך להיות. עם זאת, עם HCM, יש הפרש לחצים בין החדר השמאלי לאבי העורקים מ-50 ל-150 מ"מ כספית. Art., עלייה בלחץ הקצה-דיאסטולי בחלל החדר השמאלי עד 18 מ"מ כספית. אומנות. שיפוע הלחץ יורד לאחר החדרת חוסמי β. כמו כן, במהלך בדיקת הלב, מוזרק חומר ניגוד לחלל החדר (ventriculography) כדי לחקור את התכונות האנטומיות שלו. במספר חולים (ככלל, מדובר באנשים מעל גיל 40), אנגיוגרפיה של העורקים הכליליים (אנגיוגרפיה כלילית) משמשת בו-זמנית לפני ניתוח לב כדי להבהיר את האטיולוגיה של אנגינה פקטוריס ולא לכלול מחלת עורקים כליליים נלווית. טיפול. הבסיס לטיפול תרופתי ב-HCM הוא תרופות המשפרות את זרימת הדם לחדרי הלב בדיאסטולה. תרופות אלו הן קבוצה של חוסמי β (אנפרילין, אטנולול, מטופרולול ופרופרנולול, 160-320 מ"ג ליום ועוד) וקבוצה של אנטגוניסטים ליוני סידן (ורפמיל, אך בזהירות). נובוקינמיד ודיסופירמיד גם מפחיתים את קצב הלב ויש להם השפעה אנטי-ריתמית. בתחילת הטיפול משתמשים במינונים קטנים של תרופות אלה, ולאחר מכן גדל המינון בהדרגה עד למקסימום הנסבל על ידי המטופל. חוסמי β משמשים בזהירות בסוכרת, אסטמה של הסימפונות וכמה מחלות אחרות. כאשר מטפלים בתרופות אלו, יש צורך בניטור מתמיד של לחץ הדם והדופק. מסוכנת היא ירידה בלחץ מתחת ל-90/60 מ"מ כספית. אומנות. וקצב לב מתחת ל-55 לדקה. אם למטופל יש הפרעות קצב מסוכנות שלא ניתן לטפל בהן באמצעות חוסמי β או אנטגוניסטים של יוני סידן, אזי משתמשים בנוסף בתרופות אנטי-ריתמיות אחרות לטיפול בחולים כאלה. מינוי נוגדי קרישה מומלץ להפרעות קצב התקפיות ופרפור פרוזדורים, וכן בנוכחות קרישי דם בחדרי הלב (וורפרין וכו'). במהלך תקופת הטיפול בתרופות אלה, יש צורך לעקוב באופן קבוע אחר מספר אינדיקטורים של מערכת קרישת הדם. עם מנת יתר משמעותית של נוגדי קרישה יתכנו דימום חיצוני (אף, רחם וכו') ופנימי (המטומות וכו'). טיפול כירורגי מתבצע בחולים עם HCM חסימתי כאשר הטיפול הרפואי אינו יעיל או כאשר הגרדיאנט בין החדר השמאלי לאבי העורקים הוא יותר מ-30 מ"מ כספית. אומנות. (מבצעים את פעולת המיוטומיה או המיאקטומיה - כריתה או הסרה של חלק משריר הלב היפרטרופי של החדר השמאלי). מבוצעות גם החלפת מסתם מיטרלי ואבלציה לא ניתוחית IVS. מניעה. כל החולים עם HCM, במיוחד אלה עם צורה חסימתית, הם התווית נגד בספורט שיכול להגביר משמעותית את הפעילות הגופנית על פני תקופה קצרה (אתלטיקה, כדורגל, הוקי). מניעת המחלה טמונה באבחון מוקדם, המאפשר להתחיל טיפול מוקדם במחלה ולמנוע התפתחות היפרטרופיה חמורה של שריר הלב. חובה לבצע אקו לב בקרב קרובי משפחה גנטיים של המטופל. בדיקת א.ק.ג ו-EchoCG, המבוצעים במהלך בדיקה רפואית שנתית, חשובים אף הם לאבחון. בחולים עם צורה חסימתית של HCM יש צורך במניעת אנדוקרדיטיס זיהומית (טיפול אנטיביוטי וכו'), שכן נוכחות חסימה יוצרת תנאים להתפתחות מצב מסכן חיים זה. הרצאה מס' 4. מחלות מערכת הלב וכלי הדם. קרדיומיופתיה מגבילה קרדיומיופתיה מגבילה (RCMP) - (מהמילה הלטינית restrictio - "הגבלה") - קבוצת מחלות של שריר הלב והאנדוקרדיום, שבהן, כתוצאה מפיברוזיס בולט ואובדן גמישות, מסיבות שונות, קיימת הגבלה קבועה במילוי. של החדרים בדיאסטולה. מילוי החדרים מתבצע בשלב של מילוי מוקדם, ולאחריו ייצוב הלחץ התוך-חדרי. המחלה מלווה במילוי דם לא מספיק של הלב, מה שמוביל עוד יותר להתפתחות של אי ספיקת לב כרונית. קרדיומיופתיה מגבילה היא הפחות נחקרה והפחות נפוצה מבין כל הקרדיומיופתיה. RCMP כולל: Lefler's parietal fibroplastic endocarditis (נמצא במדינות עם אקלים ממוזג, המתואר על ידי W. Loffler et al., 1936) ופיברוזיס אנדומיוקרדיאלי (נמצא במדינות אפריקה הטרופית, מתואר על ידי D. Bedford et E. Konstman). בעבר, הם נחשבו כשני תהליכים פתולוגיים עצמאיים. עם זאת, התמונה הפתומורפולוגית במחלות אלו שונה מעט. גורמים ל-RCM. RCM ראשוני הוא נדיר מאוד, והגורם המוכח היחיד להופעתו הוא מה שמכונה תסמונת היפראוזינופילית (מחלת לפלר, Leffler's parietal fibroplastic endocarditis). זה מופיע בעיקר אצל גברים בגילאי 30-40 שנים. עם תסמונת היפראוזינופילית מתרחשת דלקת של האנדוקרדיום, שבמשך הזמן מגיעה לשיאה בדחיסה משמעותית של האנדוקרדיום והיצמדות גסה שלו לשריר הלב הסמוך, מה שמוביל לירידה חדה בהארכה של שריר הלב. תסמונת לפלר מאופיינת גם באאוזינופיליה מתמשכת למשך 6 חודשים או יותר (1500 אאוזינופילים לכל 1 מ"מ3), נזק לאיברים פנימיים (כבד, כליות, ריאות, מח עצם). ברוב המוחלט של המקרים, המקור של RCMP הוא משני, בשל סיבות אחרות, ביניהן הנפוצות ביותר הן: 1) עמילואידוזיס - מחלה הקשורה להפרה של חילוף החומרים של חלבון בגוף; במקביל, ברקמות של איברים שונים, נוצר חלבון לא תקין (עמילואיד) ומופקד בכמויות גדולות; כאשר הלב ניזוק, העמילואיד גורם לירידה בכיווץ והארכה שלו; 2) המוכרומטוזיס - הפרה של חילוף החומרים של ברזל בגוף, המלווה בתוכן מוגבר של ברזל בדם, עודף שלו מופקד באיברים ורקמות רבים, כולל שריר הלב, ובכך גורם לירידה בהארכה שלו; 3) סרקואידוזיס - מחלה של אטיולוגיה לא ידועה, המאופיינת ביצירת צבירי תאים (גרנולומות) באיברים וברקמות; הריאות, הכבד, בלוטות הלימפה והטחול מושפעים לרוב; והתפתחות גרנולומות בשריר הלב מביאות לירידה בהארכה שלו; 4) מחלות אנדוקרדיאליות (פיברוזיס אנדוקרדיאלי, פיברואלסטוזיס אנדוקרדיאלי וכו'), כאשר יש עיבוי ודחיסה משמעותיים של האנדוקרדיום, מה שמוביל גם להגבלה חדה של הרחבת שריר הלב. פיברואלסטוזיס של האנדוקרדיום, בפרט, יכול להתרחש רק אצל תינוקות; מחלה זו אינה תואמת את החיים עקב התפתחות מוקדמת של אי ספיקת לב חמורה. פתוגנזה. עם RCM, תאימות שריר הלב סובלת מסיבות שונות. כתוצאה מכך, מילוי החדרים בדם פוחת והלחץ התוך-חדרי עולה באופן משמעותי. עם זאת, בניגוד ל-HCM, האפשרות לפתח היפרטרופיה מפצה של שריר הלב בקרדיומיופתיה רשמית קטנה. לפיכך, לאחר זמן מה, מתרחשת סטגנציה במחזור הדם הריאתי ותפקוד השאיבה של הלב פוחת, מה שמוביל לאגירת נוזלים הדרגתית בגוף, התפתחות של נפיחות מתמשכת של הרגליים, הפטומגליה ומיימת. אם הדחיסה של האנדוקרדיום משתרעת עד השסתומים האטריואטריקולריים (מיטרלי וטריקוספיד), הדבר מחמיר על ידי התפתחות אי הספיקות שלהם, ומוביל גם לפקקת בחללי הלב בשל כושר ההתכווצות וההרחבה המופחתים שלהם. התפשטות שברי קרישי דם אלה עם זרם הדם עלולה לגרום לתרומבואמבוליזם וחסימת כלי דם גדולים, התקפי לב של איברים פנימיים. עם התפשטות התכלילים הפתולוגיים של שריר הלב לאזור מערכת ההולכה של הלב, עלולות להופיע הפרעות שונות בהולכה של הדחף הלבבי, מלווה בהתפתחות חסימות. עם RCMP, סוגים שונים של הפרעות קצב נצפים לעתים קרובות למדי. בהתבסס על האמור לעיל, אנו יכולים להסיק כי המחלה מנקודת מבט פתוגנטית מתקדמת בשלושה שלבים. שלב I - חדירת נמק - אאוזינופילית של שריר הלב ואיברים אחרים. שלב II - פקקת - היווצרות קרישי דם בחלל החדר השמאלי והימני, התפתחות של סיבוכים תרומבואמבוליים ועיבוי הדרגתי של האנדוקרדיום בעיקר באזורי הקודקוד ובסמוך לשסתומים האטrioventricular. שלב III - סיבי, מאופיין בהתעבות של האנדוקרדיום עד מספר מילימטרים, מתבטאת פיברוזיס שריר הלב - בעיקר אזורים תת-אנדוקרדיאליים. החלל נמחק חלקית עקב פקקת מאורגנת, פיברוזיס של שסתום המסתם המיטרלי, רגורגיטציה מיטראלית. הרחבת פרוזדורים בולטת. נצפתה חוסר תפקוד דיאסטולי מגביל. תמונה קלינית. ביטויי המחלה הם פולימורפיים ביותר ונקבעים על ידי תסמינים של הפרעות במחזור הדם במעגל הקטן או הגדול (בהתאם לנזק השולט בחדר הימני או השמאלי). תלונות עשויות להיעדר או להיות עקב גודש במחזור הריאתי או המערכתי. חולים מתלוננים בדרך כלל על קוצר נשימה, המופיע לראשונה במהלך פעילות גופנית, וככל שהמחלה מתקדמת נצפה קוצר נשימה במנוחה. עקב ירידה בתפקוד השאיבה של הלב, המטופל מתלונן על עייפות וסובלנות לקויה לכל עומס. עם הזמן מצטרפות נפיחות ברגליים, כבד מוגדל ונפטופים בבטן. מעת לעת מופיע דופק לא סדיר, ועם התפתחות חסימות מתמשכות עלולה להיות התעלפות. השלב הראשון של התפתחות המחלה (נמקית) מאופיין בהופעת חום, ירידה במשקל, שיעול, פריחה בעור וטכיקרדיה. אבחון. זיהוי RCM קשה ביותר. אפשר לדבר בביטחון על פתולוגיה זו רק לאחר אי הכללה של מספר מחלות דומות (כגון דלקת שריר הלב אידיופטית מסוג אברמוב-פידלר, פריקרדיטיס אקסאודטיבית, מומי לב מסתמיים). כאשר בודקים חולים עם RCMP, מתגלים תסמינים האופייניים לאי ספיקת לב (בצקת, הפטומגליה ומיימת), כמו גם פעימות בולטות של ורידי הצוואר. זה האחרון נובע מהקושי באספקת הדם ללב עקב יכולת הרחבה לקויה של שריר הלב. בזמן ההאזנה יש חשיבות רבה לזיהוי עלייה בלב, אוושה סיסטולית מאוחרת רכה וטון III מוקדם חזק (עקב מילוי מהיר של החדרים בזמן הדיאסטולה). אוושים בלב מתגלים גם בחולים עם אי ספיקת מסתם אטריו-חדרי. מחקר א.ק.ג. חושף היפרטרופיה מתונה של שריר הלב בחדרי הלב, כמו גם הפרעות קצב והולכה שונות של דחף הלב, שינויים לא ספציפיים בגל ה-T ב-EKG. אקו לב היא אחת השיטות האינפורמטיביות ביותר לאבחון המחלה, בעזרתה עיבוי האנדוקרדיום, שינוי באופי המילוי של חדרי הלב, ירידה בתפקוד השאיבה של הלב, תנועה מהירה. מתגלים של העלון הקדמי של המסתם המיטרלי במהלך הדיאסטולה ותנועה מוקדמת מהירה של הקיר האחורי של החדר השמאלי כלפי חוץ. הדמיית תהודה מגנטית מאפשרת לקבל מידע על האנטומיה של הלב, לקבוע תכלילים פתולוגיים בשריר הלב ולמדוד את עובי האנדוקרדיום. כאשר בוחנים את הפרמטרים של המודינמיקה המרכזית, נקבע לחץ מילוי מוגבר בשני החדרים, והלחץ הסופי בשמאל עולה על זה בחדר הימני. Ventriculography מגלה כיווץ מוגבר של החדר השמאלי, קווי מתאר חלקים של דפנותיו, לעיתים עם פגם מילוי בקודקוד (עדות למחיקה). במקרים מסוימים נקבעים שקעים באזור השרירים הפפילריים. ישנם סימנים לאי ספיקת מסתמים, במיוחד המסתם המיטרלי או התלת-צדדי. אבחון דיפרנציאלי. באבחון המבדל של RCM חשוב מאוד לקחת בחשבון את הדמיון של המחלה בביטויים חיצוניים עם פריקרדיטיס מכווץ, אך שיטת הטיפול במחלות אלו הפוכה בתכלית. ביופסיה תוך-וויטלית של שריר הלב והאנדוקרדיום משמשת בדרך כלל במקביל עם בדיקה לבבית, המאפשרת מידע רב יותר להבהרת אופי המחלה והמשך טיפול. במקרים נדירים ביותר, כאשר שיטות האבחון הנ"ל אינן מאפשרות להבחין בין RCM לבין פריקרדיטיס מכווצת, מתבצעת בדיקה ישירה של קרום הלב על שולחן הניתוחים. כל החולים עם RCMP זקוקים לבדיקה קלינית, ביוכימית ונוספת, כדי לקבוע גורמים שאינם לבביים למחלה. טיפול. הטיפול במחלה מעורר קשיים משמעותיים. רוב התרופות המשמשות לטיפול באי ספיקת לב עשויות שלא להביא את התוצאות הרצויות בשל העובדה שבגלל מאפייני המחלה, לא ניתן להשיג שיפור משמעותי בהיענות שריר הלב (במקרים מסוימים, נרשמים אנטגוניסטים של יוני סידן למטרות אלו). משתנים (אלדקטון) משמשים לסילוק עודפי נוזלים בגוף. כדי לחסל הפרעות הולכה מתמשכות, ייתכן שיהיה צורך להתקין (השתלה) קוצב קבוע. זה נגרם על ידי מחלות כגון סרקואידוזיס והמוכרומטוזיס, מה שמוביל להתפתחות של RCMP משני, הם כפופים לטיפול עצמי. בטיפול בסרקואידוזיס משתמשים בתרופות הורמונליות (פרדניזולון ועוד) ובמקרה של המוכרומטוזיס הקזת דם קבועה (להורדת ריכוז הברזל בגוף). הטיפול בעמילואידוזיס שריר הלב תלוי ישירות בסיבות להתרחשותו. רצוי להשתמש בתרופות נוגדות קרישה לפקקת בחדרי הלב. טיפול כירורגי נעזר במקרים של RCMP שנגרם על ידי נזק לאנדוקרדיאלי. במהלך הניתוח, במידת האפשר, נכרת החלק באנדוקרדיום שעבר שינויים. במקרים מסוימים, אם יש אי ספיקה של השסתומים האטrioventricular, התותבות שלהם מבוצעות. צורות מסוימות של נזק בשריר הלב עמילואיד מטופלות באמצעות השתלת לב. מניעת RCMP. למרבה הצער, אמצעי המניעה למחלה זו מוגבלים. בעיקר, יש צורך בזיהוי מוקדם של גורמים הניתנים למניעה של עמילואידוזיס, סרקואידוזיס, המוכרומטוזיס ועוד, להשגת מטרות אלו ישנה חשיבות רבה לבדיקה רפואית שנתית של האוכלוסייה. הרצאה מס' 5. מחלות של מערכת הלב וכלי הדם. אנדוקדיטיס זיהומית אנדוקרדיטיס זיהומית (IE) - מחלה המורכבת מנגע פוליפוזיס-כיב של מנגנון המסתמים של הלב (לעתים קרובות עם התפתחות של אי ספיקה מסתמית) או אנדוקרד פריאטלי (לעתים קרובות יותר, האנדותל של אבי העורקים או העורק הגדול הקרוב ביותר מושפע). המחלה נגרמת על ידי מיקרואורגניזמים פתוגניים שונים ומלווה בנגע מערכתי של האיברים הפנימיים (כליות, כבד, טחול) על רקע תגובתיות שונה של האורגניזם. עד כה, בפרסומים מודפסים שונים, ניתן למצוא את המונחים ששימשו בעבר "אנדוקרדיטיס חיידקית", "אנדוקרדיטיס ספטית ממושכת" המתייחסים לתהליך פתולוגי זה. עם זאת, המונח "אנדוקרדיטיס זיהומיות" הוא שהחליף אותם שמשקף טוב יותר את הגורם למחלה הנגרמת על ידי מגוון רחב של מיקרואורגניזמים - גורמים חיידקיים, ריקטסיה, וירוסים ופטריות. מספר החולים עם IE הולך וגדל ברחבי העולם. הסיבה לכך היא נוכחות של מה שנקרא קבוצות סיכון (חולים עם פגיעות טרשת עורקים, ראומטיות, טראומטיות במסתמים, מומי לב או מסתם, פגם במחיצת החדרים, קוארקטציה של אבי העורקים) כתוצאה מהעובדה שהזיהום מתרחש ביתר קלות על פתולוגית. שסתום או אנדוקרד שונה. אטיולוגיה. הגורמים הפתוגניים של המחלה הם לרוב קבוצת הקוקוס של מיקרואורגניזמים - סטרפטוקוקוס (ורידנס סטרפטוקוקוס בודד בעבר ב-90% מהמקרים), סטפילוקוקוס (זהוב, לבן), אנטרוקוקוס, פנאומוקוק. בשנים האחרונות, עקב השימוש הנרחב באנטיביוטיקה, מגוון הפתוגנים המיקרוביאליים השתנה. המחלה יכולה להיגרם על ידי פלורה גרם שלילית (Escherichia coli, Pseudomonas aeruginosa, Proteus, Klebsiella); הופיעו עדויות לתפקיד החשוב של פטריות פתוגניות, Sarcinus, Brucella ווירוסים. מחלות הנגרמות על ידי פתוגנים אלו חמורות יותר, במיוחד אנדוקרדיטיס הנגרמת על ידי זיהום פטרייתי (מתרחשת בדרך כלל עקב שימוש לא הגיוני באנטיביוטיקה). עם זאת, במספר חולים הגורם הסיבתי האמיתי של המחלה אינו מזוהה (תדירות תוצאות תרבית דם שליליות היא 20-50%). לעתים קרובות, זיהום מתרחש באתר של מסתם תותב - מה שנקרא תותב IE, המתפתח בעיקר בתוך חודשיים לאחר ניתוח החלפת מסתם לב. במקרה זה, לסוכן הסיבתי של המחלה יש לרוב אופי סטרפטוקוקלי. לפיכך, מקורות הזיהום והבקטרמיה ב-IE שונים מאוד (ניתוחים בחלל הפה, ניתוחים והליכי אבחון באזור האורגניטלי, התערבות כירורגית במערכת הלב וכלי הדם (כולל החלפת מסתם), שהייה ממושכת של הצנתר בווריד, עירוי תוך ורידי תכופים ושיטות מחקר אנדוסקופיות, המודיאליזה כרונית (shunt arteriovenous), מתן תרופות תוך ורידי). ישנם מה שנקרא IE ראשוני, שהתפתח על שסתומים שלמים, כמו גם IE על רקע שינויים מולדים ונרכשים בלב ובמנגנון המסתם שלו - אנדוקרדיטיס שניוני. שינויים אלו מאפשרים להבחין בחולים לקבוצות סיכון נפרדות: מומי לב (מולדים ונרכשים), צניחת מסתם מיטרלי, מפרצת עורקים, מפרצת לאחר אוטם, שאנטים, מצב לאחר ניתוח בלב וכלי דם גדולים. פתוגנזה. מנגנון ההתפתחות של IE מורכב ואינו נחקר מספיק, אולם ניתן לזהות את הנקודות העיקריות בהתפתחות המחלה. אם יש מוקד של זיהום בגוף בהשפעת חסינות הומורלית ומקומית (תאית) משתנה עם סטייה של תגובות אימונולוגיות, גורמים אנדוגניים ואקסוגניים שונים, מתפתחת בקטרמיה. מהדם, מיקרואורגניזמים נכנסים לשסתמי הלב, ויוצרים שם מוקד משני של זיהום. הקיבוע והרבייה של מיקרואורגניזמים על האנדוקרדיום מקלים על ידי מספר גורמים: שינוי קודם ברקמה ובשטח השסתום, נוכחות של מסות פקקת עליו, הנובעות בהשפעת ההשפעה המזיקה הישירה של זרם הדם. כאשר מחזור הדם התוך-לבי שלו משתנה במצבים של מחלת לב קיימת. במקביל, תאי דם שונים (טסיות וכו') "דביקים" לאתר הפגיעה הטראומטית, ויוצרים גידולי תאים הדומים לנטיפי קרח התלויים על השסתום. צמחים אלו הופכים זמינים לזיהום שחדר למצע כלי הדם. דפורמציה של השסתומים עקב התרחשות של שיפוע לחץ גדול, צרות החור ושינויים במהירות זרימת הדם תורמים גם הם להחדרת גורמים זיהומיים לאנדוקרדיום עם היווצרות מוקד זיהומי. כאשר שסתום שלם בעבר ניזוק, מתרחשים שינויים המשבשים את המאפיינים הנורמליים של חלקים בודדים של שסתום זה (מופיעה נפיחות), תהליכים אקסודטיביים או שגשוג ("דלקת מסתם אינטרסטיציאלית" - שלב פרה-קליני). בהתפתחות המחלה ניתן להבחין בשלב III. שלב I (רעיל זיהומיות) ממשיך בדרגות חומרה שונות של שיכרון. יש גידול של חיידקים, הרס של מסתמים, המוביל להתפתחות מחלות לב; באותו שלב, התהליך מוכלל לעתים קרובות עקב התפשטות ההמטוגנית של הזיהום - חתיכות של קודקודים או מושבות של מיקרואורגניזמים יכולים להיפרד מהשסתום, הקודקודים יכולים להיקרע. ניתוק פיסות צמחייה מיקרוביאלית של שסתומים תורם להחדרת תסחיפים נגועים לחלקים שונים של מיטת כלי הדם ומחמיר תופעות ספיגה. חלקים מהשסתום או צמחיית חיידקים מסתובבים בגוף עם זרימת דם, כאשר הם נכנסים למוח, הם גורמים לאוטם מוחיים, המלווים בשיתוק, paresis והפרעות נוירולוגיות שונות אחרות. המסתם, שעבר הרס, אינו יכול לבצע את תפקידו, ובקרוב יש אי ספיקת לב שמתפתחת במהירות הבזק. שלב II - אימונו-דלקתי, בו מיקרואורגניזמים קבועים על השסתומים גורמים לרגישות אוטומטית ממושכת ולנזק היפררגי לאיברים ולרקמות הגוף (הכללה חיסונית של התהליך). במהלך תקופה זו, מתחמי מערכת החיסון מסתובבים בדם ומתקבעים ברקמות (לב, כליות, כבד, כלי דם). הפרעות חיסוניות ואוטואימוניות גורמות להתפתחות של דלקת כלי דם ודלקת קרביים (אימונוקומפלקס נפריטיס, דלקת שריר הלב, הפטיטיס, קפילריטיס וכו'). שלב III - דיסטרופי - מתרחש עם התקדמות התהליך הפתולוגי: התפקודים של מספר איברים מופרעים, מתרחשת אי ספיקת לב וכליות, מה שמחמיר עוד יותר את מהלך המחלה. מיון. נכון לעכשיו, נעשה שימוש בסיווג ובמינוח של IE, המשקפים את הצורה הקלינית, וריאנט הקורס, מידת הפעילות, השלב הפתוגני והצורה הקלינית והמורפולוגית של המחלה (ראה טבלה 6). לוח 6 סיווג של IE
כמו כן, מבחינים בין IE פעיל ללא פעיל (מרפא). יש גם סיווג כירורגי, שבו יש: 1) הנגע מוגבל לעליוני המסתם; 2) הנגע משתרע מעבר לשסתום. IE חריף (מתקדם במהירות, מתפתח במשך 8-10 שבועות) הוא נדיר, בדרך כלל אצל אנשים שלא חלו בעבר במחלת לב, ומתבטא קלינית בתמונה של אלח דם כללי. עם שיטות טיפול מודרניות, אפשר לתרגם את זה ל-subacute. IE תת-חריף (הנפוץ ביותר) נמשך 3-4 חודשים, עם טיפול תרופתי הולם, עלולה להתרחש הפוגה. עם זאת, יתכנו הישנות של המחלה. IE ממושך נמשך חודשים רבים עם תקופות של החמרה והפוגה, הוא מאופיין בביטויים קליניים קלים, פרמטרים מעבדתיים קלים והפרעות כלליות. המחלה בדרך כלל מגיבה היטב לטיפול. עם מהלך שלילי, סיבוכים חמורים מתעוררים, והחולים מתים מאי ספיקת לב מתקדמת, הגדלת שיכרון ספיגה. תמונה קלינית. בהתאם לגורם הסיבתי של הזיהום, IE יכול להתרחש באופן פתאומי ולהתפתח במהירות (Staphylococcus aureus, enterococci) או להופיע סמוי (viridans streptococcus). ביטויים של IE מוצגים בצורה של תסמונות. 1) תסמונת של שינויים דלקתיים וספטיסמיה (חום, צמרמורות, פריחות דימומיות, שינויים בפרמטרים של שלב החריף בדם: לויקוציטוזיס עם תזוזה שמאלה, עלייה ב-ESR, הופעת חלבון C-reactive, עלייה בפיברינוגן, α2-גלובולינים. 2) תסמונת השיכרון הכללי של הגוף (חולשה, הזעה, כאבי ראש, מיאלגיה וארתרלגיה, אובדן תיאבון, חיוורון של העור עם גוון איקטרי). 3) תסמונת של פגיעה במסתמים (היווצרות מחלת לב). 4) תסמונת של הפרעות חיסוניות "מעבדתיות" (נוכחות של קומפלקסים חיסונים שמסתובבים בדם או מקובעים בכליות, שריר הלב, כלי הדם; היפרגמגלבולינמיה; הופעת גורם שגרוני; זיהוי נוגדנים נגד רקמות). 5) תסמונת של סיבוכים תרומבואמבוליים (דלקת כליות מוקדית, אוטם שריר הלב, טחול, מעיים, תרומבואמבוליזם במוח, כלי הגפיים התחתונים וכו'). 6) תסמונת של הכללה של נגעים (גלומרולונפריטיס מפוזר, דלקת שריר הלב, הפטיטיס, דלקת כלי דם וכו'). חומרת התסמונות הללו שונה. זה תלוי באופי של מהלך IE, שלב, סוג הפתוגן. לדוגמה, Staphylococcal IE מאופיין בפעילות גבוהה של התהליך, תסמינים חמורים של שיכרון כללי והתפתחות של סיבוכים מוגלתיים. אנדוקרדיטיס פטרייתי מלווה בדרך כלל בחסימה תסחפית של עורקים גדולים, במיוחד של הגפיים התחתונות. תמונה אופיינית של המחלה אופיינית ל-IE הנגרמת על ידי סטרפטוקוקוס וירידנס. התפרצות המחלה קשורה לעיתים קרובות לזיהום חריף או להחמרה של זיהום כרוני, כמו גם למספר מניפולציות רפואיות. אופייני במיוחד הוא השילוב של עלייה בטמפרטורת הגוף בדרגות שונות (מחום ממושך ועד מצב תת-חום או טמפרטורה רגילה) עם צמרמורות והזעה. המטופל מגיש תלונות בו-זמנית עקב נוכחות של תהליך זיהומי ושיכרון, כמו גם סיבוכים תרומבואמבוליים של נזק לבבי. לחולים עשויה להיות היסטוריה של אפיזודות של טיפול אנטיביוטי ארוך טווח (זה מתרחש כאשר IE חוזר בחולים שטופלו בעבר). אבחון. החשיבות הגדולה ביותר לקביעת אבחנה נכונה היא איתור הנזק למסתמי הלב על ידי שינויים בדפוס ההשמעה של מומי לב קיימים; הופעת רעש "נוסף". מתגלים נגעים אופייניים של העור והריריות: צבע עור Café au lait, שטפי דם, תסמינים חיוביים של הכט (צביטה) וקנצ'לובסקי-רומפל-לייד (חוסם עורקים), וכן צמתים של אוסלר - גושים צפופים היפראמיים כואבים על פני כף היד ו קצות האצבעות , סימן לוקין-ליבמן (כתמי לוקין) - דימום על קפל המעבר של הלחמית. לעתים קרובות נצפית טחול ב-IE. ירידה משמעותית במשקל (לפעמים 15-20 ק"ג) אופיינית מאוד. במקרים נדירים מתפתחת דלקת קרום הלב (רעש חיכוך פלאורלי חלש הנגרם על ידי משקעים פיבריניים על קרום הלב). בדיקה גופנית עשויה לגלות לחץ דם מוגבר, המעיד על התפתחות של גלומרולונפריטיס מפוזר. לפעמים נקבעים סימנים של תפקוד לקוי של מערכת העצבים המרכזית (פרזיס, היפרקינזיס, רפלקסים פתולוגיים וכו') כתוצאה מתסחיף של כלי מוח. במקרה זה, טעות האבחון הנפוצה ביותר היא הערכת תסמונת מסוימת כביטוי של מחלה עצמאית (לדוגמה, עם סימנים בולטים של נזק לכבד, דלקת כבד מאובחנת וכו '). עם זאת, האבחנה של IE מבוססת בעיקר על זיהוי מוקדם של הגורם הסיבתי של המחלה. לשם כך, נעשה שימוש במחקרים המעבדתיים והאינסטרומנטליים הבאים. 1) השגת תרבית דם חיובית היא הסימן האבחוני החשוב ביותר של IE. יש צורך גם בניתוח כדי לבחור את האנטיביוטיקה היעילה ביותר במקרה זה. לפחות 2-3 מהם נדרשים כדי לאשר את האבחנה. יש חשיבות רבה לטכניקת דגימת הדם והתרבות, זמן החיסון (רצוי בשיא החום), שימוש באמצעי מועשר. 2) ביצוע NBT (בדיקת nitrobluttetrazolium) - אבחון של זיהומים חיידקיים מערכתיים, המאפשר להבדיל בין זיהומים חיידקיים למחלות דלקתיות אחרות. השיטה מבוססת על הפחתת צבע NBT מסיס על ידי נויטרופילים למשקע פורמזן בלתי מסיס. אם מספר התאים החיוביים ל-NBT הוא יותר מ-10%, הבדיקה נחשבת חיובית. 3) בדיקת דם קלינית לאיתור אינדיקטורים לשלב חריף: עלייה ב-ESR ל-50 מ"מ/שעה או יותר, לויקוציטוזיס עם הסטה של נוסחת הלויקוציטים שמאלה או (בשלב II) ניתן לזהות לויקופניה ואנמיה היפוכרומית. ערך אבחוני מוצמד לזיהוי היסטוציטים בדם הנלקח מתנוך האוזן. התוכן שלהם של יותר מ-6 בשדה הראייה עשוי להצביע על לטובת IE. בדיקת דם ביוכימית מראה עלייה בתכולת הפיברינוגן, α2-גלובולינים ו-α-גלובולינים - עד 30-40%. 4) זיהוי שינויים אימונולוגיים: היפרגמגלבולינמיה, מתחמי חיסון במחזור, ירידה בטיטר המשלים, הופעת גורם שגרוני (אנטיגלובולין), תגובה מוגברת של טרנספורמציה אימפריאלית של לימפוציטים עם PHA (phytohemagglutinin) ואנטיגנים חיידקיים, זיהוי נוגדנים נגד רקמות. 5) בדיקת שתן מתבצעת לבירור נגעים של איברים ומערכות שונות, כאשר מתגלה גלומרולונפריטיס המתבטאת בפרוטאינוריה, צילינדריה והמטוריה. עלייה בתכולת הבילירובין, טרנסמינאזות מעידה על נזק לכבד. 6) סימן אבחוני ישיר של IE - נוכחות צמחייה על מסתמי הלב - מתגלה באמצעות אקו לב. לפיכך, מכל מגוון התסמינים, יש להבחין בין העיקריים והנוספים. הקריטריונים העיקריים לאבחון של IE: 1) חום עם טמפרטורה מעל 38 מעלות צלזיוס עם צמרמורת; 2) כתמי לוקין; 3) גושים של אוסלר; 4) אנדוקרדיטיס על מסתמים ללא שינוי (ראשוני) או על רקע מומי לב ראומטיים ומולדים. דלקת שריר הלב זיהומית; 5) תרומבואמבוליזם עורקי מרובה, קרעים של מפרצת מיקוטית עם שטפי דם; 6) טחול; 7) תרבית דם חיובית; 8) השפעה חיובית מובהקת משימוש באנטיביוטיקה. קריטריונים נוספים לאבחון של IE: 1) עלייה בטמפרטורת הגוף עד 38 מעלות צלזיוס, צינון; 2) שטפי דם על העור; 3) ירידה מהירה במשקל; 4) דלקת מפרקים אסימטרית של מפרקים קטנים של ידיים, רגליים; 5) אנמיזציה; 6) ESR מעל 40 מ"מ לשעה; 7) SRV חיובי בחדות; 8) נוכחות של גורם שגרוני; 9) α-גלובולינים מעל 25%; 10) עלייה בתכולת האימונוגלובולינים M, E ו-A. אבחון דיפרנציאלי. למרות שתרומבואמבוליזם נצפה לרוב ב-IE, אין לשלול גורמים אחרים לתסחיף בעורק של מחזור הדם המערכתי: אוטם שריר הלב טרנס-מורלי ומפרצת לב, דלקת שריר הלב אברמוב-פידלר אידיופטית ופרפור פרוזדורים ממקורות שונים, אך נצפה בעיקר בהיצרות. של פתח האטrioventricular שמאל. אנדוקרדיטיס ראומטית וזיהומית היא בעלת החשיבות הגדולה ביותר לאבחנה מבדלת (טבלה 7). לוח 7 קריטריונים לאבחון דיפרנציאלי עבור אנדוקרדיטיס ראומטית ו-IE ממושך
התסמינים האופייניים ל-IE כוללים טחול מוגדל. עם זאת, טחול גדול, מוצק, ללא כאבים נראה בעמילואידוזיס; רך, ללא כאבים מעיד על היפרפלזיה ספטית שלו. כאב הוא ציין עם אוטם של הטחול, ממוקם subcapsularly. טחולית עשויה להיות אחד הביטויים של יתר לחץ דם פורטלי באי ספיקת לב ימנית. במקרה זה, זה משולב עם מיימת והפטומגליה. עלייה בגודל הכבד עם IE ממושך נצפתה לעתים קרובות למדי. היפרפלזיה ספטית מאופיינת בהגדלה קטנה יחסית ועקביות רכה של הכבד. יש ניוון שומני ולעיתים נדירות ביותר - אוטמי כבד. לרוב, עלייה בכבד קשורה לגודש ורידי עם אי ספיקת לב ימנית. בהיעדר מיימת, הגודש מוכר בדיעבד על ידי ירידה בגודל הכבד לאחר טיפול בגליקוזידים לבביים ומשתנים. טיפול. הטיפול ב-IE צריך להיות מוקדם ואטיוטרופי ככל האפשר, תוך התחשבות בנתונים בקטריולוגיים. לפני שתרופות אנטיבקטריאליות מצאו את השימוש הנרחב שלהן בפרקטיקה הרפואית, רוב החולים עם IE מתו מזיהום ומסיבוכיו. כעת יותר מ-80% נרפאים בהצלחה. אבל עבור כמעט 20%, הטיפול התרופתי אינו יעיל, ובמהרה הם מפתחים אי ספיקת לב, שכמעט ואינה ניתנת לטיפול. בהקשר זה, רצוי שילוב של טיפול שמרני וניתוחי. לטיפול ב-IE בכל קבוצת גיל, משתמשים בעיקר באנטיביוטיקה בעלת השפעה חיידקית על מיקרואורגניזמים, רצוי במינונים אישיים בהתאם לריכוז האנטיביוטיקה בדם ולרגישות הפתוגן אליו. תרופת הבחירה הראשונה היא עדיין פניצילין. יש לו רעילות נמוכה, מה שמאפשר להשתמש בו לאורך זמן במינונים גבוהים יחסית. המינון היומי - עד 20 IU ניתנת תוך ורידי ובשריר. עם זאת, אין לשלול את העובדה כי בחולים קשישים וסניליים, כאשר מטופלים עם פניצילין ואנטיביוטיקה אחרת במינונים גבוהים, נצפית לעתים קרובות אפקט קרדיוטוקסי: הופעה או התעצמות של אי ספיקת לב, כאב בלב, טכיקרדיה. כאשר מפחיתים את המינון או מחליפים את התרופה, תופעות אלו נפסקות. עם אטיולוגיה לא ידועה, הטיפול מתחיל במינונים גבוהים של בנזילפניצילין לשריר או תוך ורידי עד 18-000 יחידות או יותר, שילוב עם סטרפטומיצין עד 000 גרם/מ' ליום או אמינוגליקוזידים (גנטמיצין, טוברמיצין בקצב של 20-000 מ"ג. / יום) משמש. ק"ג ליום). בהעדר השפעה או לאחר קביעת הפתוגן, משתמשים בפניצילינים חצי סינתטיים (אוקסצילין, מתיצילין או אמפיצילין תוך שרירי עד 000 גרם ליום). צפלוספורינים הם גם התרופות הבסיסיות המשמשות לטיפול ב-IE: הנפוצות ביותר בשימוש הן קלפורן, צפמיסין (1-4 גרם ליום, תוך שרירי ותוך ורידי), וכן זפורין (6-12 גרם ליום) וקפזול (עד 4). -10 גרם לווריד). וכו'). לפוסידין השפעה אנטי סטפילוקוקלית טובה, במקרים מסוימים הוא יעיל בעמידות של מיקרואורגניזמים לאנטיביוטיקה אחרת (10-16 גרם ליום). טיפול אנטיביוטי נקבע למשך זמן רב במהלך של 1,5-2 חודשים, עד לביטול הזיהום לחלוטין. לאחר חיסול הזיהום, מצבו הכללי של החולה משתפר, הצמחייה נעלמת על פי אקו לב ואישור מיקרוביולוגי. עם פעילות אימונולוגית מופחתת של האורגניזם, סוכנים אנטיבקטריאליים משולבים עם אימונותרפיה פסיבית (לדוגמה, עם אנדוקרדיטיס סטפילוקוקלית - עם פלזמה אנטי-סטפילוקוקלית או א-גלובולין אנטי-סטפילוקוקלי), באמצעות אימונומודולטורים (תימלין, T-אקטיבין וכו '). למניעת פקקת, למשל, עם אנדוקרדיטיס שהתפתחה על רקע אלח דם אנגיוגני, נוצרת היפוקרישה מבוקרת באמצעות הפרין (20-000 IU תוך ורידי או תת עורי). לעיכוב של אנזימים פרוטאוליטיים, נעשה שימוש בקונטריקל (עד 25-000 IU תוך ורידי). כאשר IE מסתמי תרם להיווצרות מחלת לב מסתמית או שביטויי המחלה אינם נעלמים למרות טיפול אנטיביוטי מסיבי, רצוי לבצע טיפול כירורגי. טיעון נוסף בעד התערבות כירורגית הוא תסחיף חוזר מעלוני מסתמי הלב שנהרסו בזיהום. לעיתים הזיהום חורג מגבולות טבעת המסתם תוך יצירת מורסות המהווה גם אינדיקציה לטיפול כירורגי. המטרה העיקרית של הניתוח היא לשמר את המסתם של המטופל עצמו. לפעמים הם מוגבלים להסרת צמחייה, תפירת קרעים של השסתומים וכו'. אם השסתום נהרס כמעט לחלוטין בהשפעת זיהום, הוא מוחלף במלאכותי (תותב) באמצעות תותבות מכניות וביולוגיות. מניעה. מניעת IE מורכבת מהתברואה בזמן של מוקדי זיהום כרוניים בחלל הפה, השקדים, האף, הסינוסים הפרנאסאליים, ושימוש בטיפול אנטיבקטריאלי פעיל למחלות סטרפטוקוקליות וסטפילוקוקליות חריפות (אנגינה וכו'). מומלץ להקשיח את הגוף. כל החולים במחלת לב מסתמיים, כמו גם עם תותבות מסתמים, צריכים לקחת אנטיביוטיקה באופן מניעתי יום לפני וזמן קצר לאחר כל התערבות, ולאחר מכן זיהום יכול לחדור למחזור הדם. יש צורך בהשגחה רפואית על אנשים שסבלו מדלקות חריפות בסטרפטוקוק, סטפילוקוק. הרצאה מס' 6. מחלות מערכת הנשימה. אסטמה של הסימפונות הגדרה ממצה של אסטמה לא קיימת עד היום, עם זאת, ההגדרה המלאה ביותר של מחלה זו ניתנה על ידי G. B. Fedoseev בשנת 1982. אסתמה ברונכיאלית (BA) היא מחלה עצמאית, כרונית, חוזרת עם נגע ראשוני של דרכי הנשימה. המנגנון הפתוגני העיקרי והחובה שלו הוא תגובתיות סימפונות משתנה עקב מנגנונים ספציפיים (אימונולוגיים) ו(או) לא ספציפיים, מולדים או נרכשים, והסימן הקליני העיקרי (החובה) הוא התקף אסטמה ו(או) מצב אסתמטי (מצב אסטמטי) עקב עווית של שרירים חלקים של הסימפונות, הפרשת יתר, דיסקריניה ובצקת של רירית הסימפונות. אטיולוגיה. שילוב של מספר גורמים ממלא תפקיד חשוב בהופעת אסתמה. בהקשר זה, ישנן 2 צורות של אסטמה - אטופית (מהלטינית athopia - "נטייה תורשתית") וזיהומית-אלרגית. נטייה תורשתית נובעת מהקשר של אנטיגנים היסטוריים מסוימים (HLA) עם חומרת האסטמה, ועלייה בחומרת המחלה נצפית לעתים קרובות במיוחד אצל נשאים של אנטיגנים B.35 ו ב40. גורמים פנימיים להתפתחות המחלה הם פגמים ביולוגיים במערכת החיסון, מערכת האנדוקרינית, מערכת העצבים האוטונומית, רגישות ותגובתיות הסימפונות, פינוי רירי, אנדותל כלי דם ריאתי, מערכת תגובה מהירה (תאי פיטום וכו'), חילוף חומרים של חומצה ארכידונית, וכו ' גורמים חיצוניים כוללים: 1) אלרגנים מדבקים (וירוסים, חיידקים, פטריות, שמרים וכו'); 2) אלרגנים לא מדבקים (אבקה, אבק, תעשייתי, רפואי, מזון; אלרגנים של קרציות, חרקים ובעלי חיים); 3) חומרים מגרים מכניים וכימיים (מתכת, עץ, סיליקט, אבק כותנה; אדי חומצות, אלקליות; אדים וכו'); 4) גורמים מטאורולוגיים ופיזיקו-כימיים (שינויים בטמפרטורת האוויר ובלחות, תנודות בלחץ הברומטרי, השדה המגנטי של כדור הארץ, מאמץ פיזי וכו'); 5) השפעות מלחיצות, נוירו-פסיכיות ופעילות גופנית. סוכנים זיהומיים יכולים להיות לא רק אפקט אלרגני, אלא גם להפחית את סף הרגישות של הגוף לאלרגנים לא זיהומיים (אטופיים), להגביר את החדירות של רירית הנשימה עבורם; ליצור שינוי בתגובתיות של תאי מטרה (תאי פיטום, בזופילים, מונוציטים וכו') ומערכות אפקטורים. פתוגנזה. תגובתיות משתנה של הסימפונות היא חוליה מרכזית בפתוגנזה של המחלה ויכולה להיות ראשונית או משנית. במקרה הראשון, שינויים בתגובתיות יכולים להיות מולדים או נרכשים עקב חשיפה ישירה לגורמים כימיים, מכניים, פיזיים וזיהום. שינויים משניים בתגובתיות הסימפונות הם ביטוי לשינויים בתגובתיות של מערכת החיסון, האנדוקרינית והעצבים של הגוף. לפיכך, אם מדברים על הפתוגנזה של AD, אנו יכולים להבחין ב-2 קבוצות של מנגנונים: אימונולוגי ולא אימונולוגי. מנגנונים אימונולוגיים ברוב המוחלט של המקרים דומיננטיים במהלך המחלה. הפרות של המערכת החיסונית בקרום הרירי של דרכי הנשימה, המתרחשות על פי סוגים I, III ו-IV של תגובות רגישות יתר, כלומר עם שינוי בחסינות הומורלית ותאית, מובילות לשינוי בתגובתיות הסימפונות. במקביל, חלה ירידה ב-IgA המופרש, מערכת הפגוציטוזיס מופרעת, תפקוד מדכא ה-T של לימפוציטים יורד, ייצור האינטרפרון יורד, מה שמוביל בסופו של דבר לירידה בהגנה האנטי-ויראלית של הגוף. סוג I (אטופי, ריאגיני או אנפילקטי). בתגובה לבליעה של אנטיגנים אקסואלרגניים (אבקה, חלבונים מן החי והצומח, חיידקים ותרופות), מתרחש ייצור מוגבר של IgE (reagins), המתקבעים ומצטברים על תאי פיטום (תאי אפקטור ראשוניים). זהו השלב האימונולוגי של AD. בעקבות כך מתפתח השלב הפתוכימי של התהליך - דה-גרנולציה של תאי פיטום עם שחרור חומרים וסואאקטיבים, ברונכוספסטיים וכימוקטיים (היסטמין, סרוטונין, גורמים כימוקטיים שונים ועוד). אלו מתווכים ראשוניים הפועלים על כלי דם ותאי מטרה (תאי אפקטור משניים) – אאוזינופילים, נויטרופילים, טסיות דם, מונוציטים מקרופאגים. האחרונים, כאשר הם נחשפים למתווכים ראשוניים, מפרישים מתווכים משניים (לויקוטריאנים, פרוסטגלנדינים, טרומבוקסנים, גורם מפעיל טסיות וחומרים נוספים השייכים לקבוצת האייקוסנואידים). בהשפעת חומרים פעילים ביולוגית, השלב הפתופיזיולוגי של הפתוגנזה מתחיל: החדירות של המיטה המיקרו-מחזורית עולה, מה שמוביל להתפתחות בצקת, דלקת כבדה וסמפונות. מבחינה קלינית, זה מתבטא בהפרה חריפה של סבלנות הסימפונות והתפתחות של התקף אסטמה. תגובה מסוג III (סוג אימונוקומפלקס, או תופעת ארתוס) מתפתחת בהשפעת אקסואלרגנים ואנדואלרגנים (אוטואלרגנים, הנוצרים על ידי דנטורציה של חלבונים של ברונכיולים ומכשכים כתוצאה מדלקת זיהומית או אלרגית ומפעולת חומרים מגרים שונים). התגובה מתרחשת באזור של עודף אנטיגן בהשתתפות נוגדנים מזרזים השייכים לאימונוגלובולינים של מחלקות O ו-M. ההשפעה המזיקה של קומפלקס האנטיגן-נוגדנים שנוצר מתממשת באמצעות הפעלת משלים, שחרור אנזימים ליזוזומליים. יש פגיעה בממברנות הבסיסיות, עווית של שרירים חלקים של הסימפונות, הרחבת כלי הדם והחדירות של המיקרו-וסקולטורה עולה. סוג IV (רגישות יתר תאית, מושהית) מאופיין בעובדה שללימפוציטים רגישים יש השפעה מזיקה. במקרה זה, המתווכים של התגובה האלרגית הם לימפוקינים (פועלים על מקרופאגים, תאי אפיתל), אנזימים ליזוזומליים ומערכת קינין מופעלת. בהשפעת חומרים אלה מתפתחת בצקת, נפיחות של הקרום הרירי, עווית הסימפונות, ייצור יתר של הפרשות סימפונות צמיגות. התוצאה היא הפרה חריפה של הפטנציה של הסמפונות, המתבטאת בהתקף של חנק. מנגנונים לא אימונולוגיים הם השינוי העיקרי בתגובתיות הסימפונות כתוצאה מפגמים ביולוגיים מולדים ונרכשים. מנגנונים לא אימונולוגיים פועלים על תאי אפקטור ראשוניים או משניים או על הקולטנים של השרירים החלקים של הסמפונות, כלי דם, תאי בלוטות הסימפונות. זה משנה את התגובתיות של תאי המטרה ובעיקר תאי הפיטום, המלווה בייצור יתר של חומרים פעילים ביולוגית (היסטמין, לויקוטריאנים וכו'). בתגובה לשחרורם, מתפתחים ברונכוספזם, נפיחות של הקרום הרירי, היפר ודיסקריניה של בלוטות הסימפונות. כל זה משנה באופן דרמטי את סבלנות הסמפונות וגורם להתקף אסטמה. התנגדות הסימפונות יכולה להשתנות באופן מותנה וללא תנאי כרפלקס. לדוגמה, חסימה הנובעת מחשיפה לאוויר קר, שאיפת גזים ואבק מגרים ופעילות גופנית נגרמת על ידי עווית הסימפונות דרך רפלקס הנרתיק. הסיבות לעווית הסימפונות יכולות להיות גם נזק לאזורי המשפיעים של רפלקס הברונכוכיווץ הנרתיק או חסימה של קולטני β-אדרנרגיים. לאחרונה, הם מדברים על תפקיד מיוחד בפתוגנזה של הפרות של פטנטיות הסימפונות של אי ספיקת גלוקוקורטיקואידים והפרעות דיסאובריות. אי ספיקה של גלוקוקורטיקוסטרואידים מובילה להתפתחות תגובתיות יתר של תאי פיטום, ירידה בסינתזה של קטכולאמינים והפעלה של פרוסטגלנדינים F2a, כמו גם הפרה של המערכת החיסונית (כאן אנחנו מדברים על ההשתתפות המורכבת בפתוגנזה של AD ומנגנונים אימונולוגיים ולא אימונולוגיים). היפר-אסטרוגנמיה והיפופרוגסטרונמיה פועלות על קולטנים α-ו-β-אדרנרגיים, מגבירים את הפעילות של הראשונים ומפחיתים את הפעילות של האחרונים. מיון. הדומיננטיות של מנגנון כזה או אחר בפתוגנזה של אסתמה מאפשרת לנו לזהות את המאפיינים הפתוגנטיים השונים שלה. נכון לעכשיו, נעשה שימוש בסיווג המוצע על ידי G. B. Fedoseev (1982). שלבי התפתחות AD. I - טרום-אסתמה (מצבים המאיימים על התפתחות: ברונכיטיס חריפה וכרונית, דלקת ריאות חריפה וכרונית עם אלמנטים של ברונכוספזם בשילוב עם נזלת vasomotor, אורטיקריה). II - BA שנוצר באופן קליני (נחשב ככזה לאחר ההתקף הראשון או הופעה מידית של סטטוס אסטמטיס). טפסי BA: 1) אימונולוגי; 2) לא אימונולוגי. מנגנונים פתוגנטיים (וריאנטים קליניים ופתוגנטיים) של AD: 1) אטופית; 2) תלויי זיהום; 3) אוטואימונית; 4) דיס-הורמונלי; 5) חוסר איזון נוירופסיכי; 6) חוסר איזון אדרנרגי; 7) חוסר איזון כולינרגי; 8) שינוי ראשוני בתגובתיות הסימפונות. בחולה אחד, שילוב של מספר וריאנטים קליניים ופתוגנטיים אפשרי. במצב כזה, יש צורך בזמן הבדיקה להדגיש את הגרסה העיקרית עבור מטופל זה, החשובה לטיפול הולם. במהלך מסלול ארוך של BA, יתכן שינוי במנגנון הפתוגני. חומרת הקורס לתואר ראשון: 1) מהלך קל (החמרות נדירות, 2-3 פעמים בשנה, התקפי אסתמה קצרי טווח נעצרים על ידי נטילת תרופות שונות להרחבת סימפונות בפנים); 2) חומרה בינונית (החמרות תכופות יותר 3-4 פעמים בשנה, התקפי אסתמה קשים יותר ונעצרים על ידי זריקות תרופות); 3) מהלך חמור (המתאפיין בהחמרות תכופות וממושכות, התקפים קשים, לעיתים קרובות הופכים למצב אסתמטי). חלוקת BA לפי חומרת הקורס מותנית. לכן, עם מהלך קל של BA, החולה עלול למות ממצב אסטמטי שפותח פתאום. שלבי הקורס לתואר ראשון: 1) החמרה (נוכחות של התקפים חוזרים של אסטמה או מצב אסטמטי); 2) ירידה בהחמרה (התקפים הופכים לנדירים יותר ומתונים, סימנים פיזיים ותפקודיים של המחלה פחות בולטים מאשר בשלב ההחמרה); 3) הפוגה (ביטויים אופייניים של BA נעלמים: התקפי אסטמה אינם מתרחשים; ספיפות הסימפונות משוחזרת באופן מלא או חלקי). סיבוכים: 1) ריאתי: אמפיזמה, אי ספיקה ריאתית, אטלקטזיס, pneumothorax, status asthmaticus וכו'; 2) חוץ ריאתי: cor pulmonale (פוצה ופיטר עם התפתחות אי ספיקת לב ימנית), ניוון שריר הלב וכו'. תמונה קלינית. הסימן האופייני ביותר לאסטמה הוא תלונות על התקפי חנק (קשיי נשימה בעיקר בנשיפה), קוצר נשימה ושיעול מסוגים שונים (מיובש, התקפי או עם שחרור כיח צמיג). התפתחות זיהום ברונכופולמונרי גורמת לעלייה בטמפרטורת הגוף. הקושי הנובע בנשימה באף הוא ביטוי של rhinosinusopathy אלרגי (נזלת vasomotor, polyposis), המתרחשת בדרך כלל בשלב הטרום-אסתמה. נתוני ההיסטוריה עוזרים לבסס קשר בין התפתחות התקפים וחשיפה לאלרגנים מסוימים וגורמים אחרים. לרוב מדובר בזיהום של דרכי הנשימה, במיוחד בהחמרה של המחלה. מהאנמנזה לומדים על השפעת המאמץ הגופני (כגון הליכה מהירה, צחוק ועוד), שינויים בגורמים מטאורולוגיים (כגון קור, לחות גבוהה ועוד), הפרעות דיסאובריאליות, גורמים מקצועיים על הופעת אסתמה. התקפות. חקר ההיסטוריה האלרגית תורם לאבחון של וריאנט אטופי של BA. במקרים כאלה, החמרות המחלה הן עונתיות (לעתים קרובות יותר באביב ובקיץ), מלווה בנזלת, דלקת הלחמית. לחולים כאלה יש אורטיקריה, בצקת קווינקה; אי סבילות למזון, מתגלים מספר חומרים רפואיים; יש נטייה תורשתית למחלות אלרגיות. נתונים מהאנמנזה מאפשרים לעתים קרובות לבסס את נוכחותה של מה שנקרא אסתמה אספירין. במקרה זה, אין צורה תורשתית של מחלות אלרגיות. חולים כאלה מודאגים מפגיעה בנשימה באף (גידולים פוליפים), והתסמין האופייני ביותר הוא אי סבילות לתרופות נוגדות דלקת לא סטרואידיות (חומצה אצטילסליצילית, אינדומתצין וכו'), הגורמות להתקפי אסתמה. במקרה זה, כבר ניתן להניח מנגנון פרוסטגלנדין של AD. נתונים על התפתחות מצב אסתמטי בעבר מצביעים על חומרת מהלך המחלה ומצביעים על צורך בטיפול בקורטיקוסטרואידים. אבחון. חשיבות רבה היא זיהוי ביטויים חוץ-ריאה של אלרגיות, סימנים של חסימת סימפונות, סיבוכים של אסטמה ומחלות אחרות המלוות בהתקפי ברונכוספזם. כאשר בודקים את העור, ניתן לזהות ביטויים אלרגיים: אורטיקריה, פריחות אדמומיות פפולריות, המעידות על וריאנט אימונולוגי של BA. השילוב של אסטמה עם אקזמה, נוירודרמטיטיס, פסוריאזיס נוטה לאסטמה קשה. לעתים קרובות ניתן לזהות הפרה של נשימה באף. נזלת ופוליפים נחשבים טרום אסתמה. סינוסיטיס וסינוסיטיס אחרים עלולים לגרום לחנק. בדיקה גופנית של הריאות, לעתים קרובות עקב ברונכיטיס כרונית בסיסית, עשויה לגלות סימנים של אמפיזמה המובילה להתפתחות של אי ספיקת נשימה כרונית ו-cor pulmonale. מתגלים סימנים אוסקולטיים של חסימת סימפונות: שינוי בנשימה (נשימה ממושכת, יבש, בעיקר צפצופים, צפצופים), נשיפה כפויה, החושפת עווית סימפונות סמויה (הופעה או עלייה של צפצופים יבשים). אוסקולציה של הריאות חייבת להתבצע בתנוחת המטופל בשכיבה: מספר החריצים היבשים עולה עם המנגנון ה"ווגאלי" שלהם. בהקשבה מתמדת באזור מסוים, רעלים מבעבעים עדינים בקול לח ("מתפצפצים") עשויים להעיד על מחלת ריאות מפותחת. בדיקה אובייקטיבית של החולה מעלה תסמינים של מחלות נוספות ("פרפר" על עור הפנים, לימפדנופתיה בשילוב עם עלייה בכבד ובטחול, עלייה מתמשכת בלחץ הדם, חום מתמשך ועוד), בהן. מתרחשים התקפות של עווית הסימפונות, המתבטאת בחנק (זאבת אריתמטית מערכתית, דלקת קרום העורקים הנודולרית). אז האבחנה לכאורה של AD הופכת לבלתי סבירה. ספירוגרפיה חושפת את הסימנים האופייניים לחסימת סימפונות חסימתית: ירידה בנפח הנשיפה המאולצת בשנייה הראשונה (FEV1), ירידה במקדם ה-Tiffno (FEV).1 ל-VC כאחוז) ואחוז FEV1 ל-FZhEL. במהלך החמרה של BA, נפח הריאות השיורי (RLV) ויכולת השיורית התפקודית (FOC) עולים על הרמה ההתחלתית ב-100% או יותר. כאשר מנתחים את הספירוגרמה, מתגלים סימנים של דיסקינזיה tracheobronchial, התורמים להפרה של הפטנציה הסימפונות, על ידי נוכחות של חריץ בחלק העליון של הצבע היורד של הספירוגרמה (תסמין Kolbet-Wyss). Pneumotachometry מראה את הדומיננטיות של כוח ההשראה על פני כוח הנשיפה, האופיינית לחסימת הסימפונות. על פי פנאומוטכוגרפיה עם בניית עקומת נפח הזרימה, הפרה של הפטנציה הסימפונות מאובחנת בנפרד ברמה של סימפונות גדולים, בינוניים וקטנים. הופעת עמידות מוגברת של הסימפונות, הנרשמת באמצעות ספירוגרפיה, פנאומוטקומטריה ופנאומוטכוגרפיה, בתגובה לפעילות גופנית, שאיפת אוויר קר, גזים מגרים ואצטילכולין מעידה על שינוי בתגובתיות הסימפונות. בדיקה אלרגולוגית מתבצעת באמצעות סט של אלרגנים שונים שאינם זיהומיים וזיהומיים, היא מתבצעת רק מחוץ להחמרת המחלה. כדי להעריך את ההשפעה הפרובוקטיבית של האלרגן, מבוצעות בדיקות אלרגיות בעור (יישום, צלקת ושיטות תוך-עוריות של מריחת האלרגן), ניתן למרוח את האלרגן על הלחמית של העין, רירית האף. המהימן ביותר הוא האבחנה הספציפית של אסתמה – זיהוי של תגובת יתר סימפונות ספציפית בעזרת בדיקות פרובוקטיביות באינהלציה. עם זאת, אין לאבד את העובדה שדרך ניהול זו יכולה לעורר התקף חמור של אסטמה או התפתחות של סטטוס אסטמטי. לצורך האבחנה הספציפית של AD, למשל, כאשר לא ניתן לבצע בדיקות אלרגיות, נעשה שימוש גם בבדיקת רדיואימונוסורבנט, המאפשרת הערכה כמותית של נוגדני IgE. מחקרי מעבדה עוזרים לאשר את האבחנה המוצעת, להעריך את התפתחות המחלה ואת יעילות הטיפול. קריטריון האבחון העיקרי של AD הוא הופעת אאוזינופילים בליחה, אך זהו סימן לא ספציפי, זה יכול לשמש ביטוי לתגובה אלרגית כללית של הגוף. חשיבות אבחנתית היא גם זיהוי של ספירלות קורשמן וגבישי Charcot-Leiden בליחה. מחקרי מעבדה מוכיחים נוכחות של תהליך דלקתי פעיל ואת מידת חומרתו במונחים של עלייה באינדיקטורים לשלב אקוטי. עם עלייה באי ספיקת נשימה במקרה של החמרה של אסטמה ומצב אסטמטי, חשוב ללמוד את מצב חומצה-בסיס והרכב גזי הדם. בדיקת רנטגן מאבחנת מוקדי זיהום (בסינוסים הפרה-אנזאליים, בשיניים, בכיס המרה) ונוכחות חריפה (דלקת ריאות) או החמרה של תהליך דלקתי כרוני בריאות, אמפיזמה ו-pneumosclerosis. נתוני א.ק.ג מוכיחים סימנים להתפתחות של cor pulmonale פיצוי - היפרטרופיה של הלב הימני. אבחון דיפרנציאלי. BA מובחן מאסתמה לבבית (ראה טבלה 8). לוח 8 אבחנה מבדלת של AD
כמו כן, יש צורך להבדיל בין אסתמה זיהומית-אלרגית ואטופית (ראה טבלה 9). לוח 9 אסטמה זיהומית-אלרגית ואטופית
טיפול. בטיפול באסטמה מומלצת גישה שלבית, המוסברת בחומרה המשתנה של מהלך זה אצל אנשים שונים ואצל אותו חולה. שלב 1 הוא האסטמה הכי פחות חמורה, שלב 4 הוא הגדול ביותר. שלב 1: מהלך קל לסירוגין בו מופיעים תסמיני אסתמה בחשיפה לטריגר (למשל אבקה או שיער של בעלי חיים) או עקב פעילות גופנית. שימוש ארוך טווח בתרופות אנטי דלקתיות בטיפול בחולים כאלה אינו הצביע. הטיפול מורכב מטיפול תרופתי מניעתי במידת הצורך (בשאיפה בשאיפה2אגוניסטים, קרומוגליקאט, נדוקרומיל או תרופות אנטיכולינרגיות). לעיתים, החמרות חמורות וממושכות יותר מצריכות קורס קצר של קורטיקוסטרואידים דרך הפה. אם אסתמה מתבטאת בתסמינים תכופים יותר, עלייה בצורך במרחיבי סימפונות, אזי יש צורך לעבור לשלב הבא. שלב 2. מהלך מתמשך קל. הטיפול הראשוני כולל תרופות אנטי דלקתיות, קורטיקוסטרואידים בשאיפה, נתרן קרומוגלקט או נתרן נדוקרומיל. המינון של קורטיקוסטרואידים הוא 200-500 מק"ג של beclomethasone dipropionate או budesonide ליום. לטיפול סימפטומטי, β בשאיפה2-אגוניסטים, אך לא יותר מ-3-4 פעמים ביום. עבור החמרות חמורות וממושכות יותר, ניתן קורס קצר של קורטיקוסטרואידים דרך הפה. אם התסמינים נמשכים למרות מינון ראשוני של קורטיקוסטרואידים בשאיפה, יש להעלות את המינון של beclomethasone dipropionate ל-750-800 מיקרוגרם ליום. עם זאת, חלופה להעלאת מינון ההורמונים בשאיפה, במיוחד לשליטה בהתקפי אסתמה ליליים, היא תוספת של מרחיבי סימפונות ארוכי טווח הנלקחים בלילה (במינון של קורטיקוסטרואידים בשאיפה של לפחות 500 מק"ג). שלב 3 מאופיין בחומרה בינונית של BA. חולים כאלה דורשים צריכה יומית של תרופות אנטי דלקתיות מניעתיות. המינון של קורטיקוסטרואידים בשאיפה הוא 800-2000 מק"ג בשילוב עם מרחיבי סימפונות ארוכי טווח. אתה יכול להשתמש בתיאופילינים ארוכי טווח (עם ניטור מתמיד של ריכוזם לא יותר מ 5-15 מיקרוגרם / מ"ל), β דרך הפה ובשאיפה2אגוניסטים ארוכי טווח. באופן סימפטומטי למנות β2-אגוניסטים קצרי טווח או תרופות חלופיות (שלב 2). שלב 4. אסטמה קשה, כאשר היא אינה נשלטת לחלוטין. במקרה זה, מטרת הטיפול היא להגיע לתוצאות הטובות ביותר. הטיפול הראשוני כולל קורטיקוסטרואידים בשאיפה במינון גבוה (בין 800 ל-2000 מיקרוגרם ליום של beclomethasone dipropionate) בשילוב עם מרחיבי סימפונות ארוכי טווח. במידת הצורך, יש לציין β בשאיפה כדי להקל על התסמינים.2-אגוניסטים קצרי טווח (לא יותר מ-3-4 פעמים ביום). החמרה חמורה יותר עשויה לדרוש קורס של טיפול בקורטיקוסטרואידים דרך הפה, אשר נקבעים במינונים מינימליים או כל יומיים. כדי למנוע התפתחות של תופעות לוואי, מינונים גבוהים של קורטיקוסטרואידים בשאיפה ניתנים דרך מרווח. שלב 5 כולל הפחתת תרופות תומכות. הדבר אפשרי אם אסתמה נשארת בשליטה למשך 3 חודשים לפחות, מה שעוזר להפחית את הסיכון לתופעות לוואי ומגביר את הרגישות של המטופל לטיפול המתוכנן. "הפחתת" הטיפול מתבצעת תחת שליטה מתמדת של סימפטומים, ביטויים קליניים ואינדיקטורים של תפקודי נשימה על ידי הפחתה הדרגתית (ביטול) של המנה האחרונה או תרופות נוספות. עצירת התקפות. התקף קל יכול להיות מטופל בבית עם מרחיבי סימפונות קצרי טווח. הטיפול מתבצע עד להיעלמות מוחלטת של התסמינים. התקפים מתונים וקשים דורשים לא רק מינונים נאותים של מרחיבי סימפונות קצרי טווח (בשאיפה בשאיפה2-אגוניסטים קצרי טווח), אלא גם מינוי של קורטיקוסטרואידים מערכתיים. אם למטופל יש היפוקסמיה, יש לתת חמצן. לטיפול בהתקפי אסטמה במרכז רפואי או בבית חולים, מינונים גבוהים של β בשאיפה2אגוניסטים דרך נבולייזר. השימוש במשאף אירוסול במינון מדדי דרך מרווח יעיל מאוד. עדיף, קורטיקוסטרואידים ניתנים דרך הפה, לא תוך ורידי. כאשר משתמשים בתיאופילין או אמינופילין בשילוב עם מינונים גבוהים של β2-אגוניסטים השפעה נוספת על הרחבת הסימפונות אינה מסופקת, אך הסיכון לתופעות לוואי עולה. ניתן להשתמש בתיאופילינים רק בהיעדר β2לעומת זאת, ניתן לתת אותם לווריד בשיעור של 6 מ"ג/ק"ג אמינופילין (או 5 מ"ג/ק"ג תיאופילין) עם מינון קבוע של 0,5-1,0 מ"ג/ק"ג לשעה למשך 24 שעות. לחילופין, β2אגוניסטים קצרי טווח יכולים להשתמש גם באפינפרין, אך ייתכנו תופעות לוואי משמעותיות בשימוש בו. תרופות מוקוליטיות בשאיפה, תרופות הרגעה ואנטי-היסטמינים, מגנזיום סולפט, פיזיותרפיה בחזה, הידרציה עם כמויות גדולות של נוזלים למבוגרים וילדים גדולים אינם מומלצים לטיפול בהתקפי אסטמה כדי למנוע שיעול מוגבר. מניעה. מניעה ראשונית של אסתמה כוללת טיפול בחולים במצב של טרום אסטמה, זיהוי פגמים ביולוגיים באנשים בריאים למעשה עם היסטוריה משפחתית המהווים איום להופעת אסטמה, סילוק אלרגנים שעלולים להיות מסוכנים, חומרים מגרים וגורמים אחרים מהגוף. סביבת חולים שיכולה להוביל להתפתחות המחלה. בטיפול בחולים במצב של פרה-אסתמה יש צורך בחיטוי מוקדי הזיהום, טיפול ברינוסינוזופתיה אלרגית, יישום שיטות שונות של טיפול לא תרופתי, לרבות דיקור ופסיכותרפיה, טיפול בפעילות גופנית, בארותרפיה וטיפול בספא. מוצג ביצוע hyposensitization ספציפי ולא ספציפי. הרצאה מס' 7. מחלות מערכת הנשימה. ברונכיטיס כרונית ברונכיטיס חסימתית כרונית היא נגע דלקתי מפוזר לא אלרגי של עץ הסימפונות, הנגרם על ידי השפעות ממושכות של גירוי על הסמפונות של גורמים שונים, בעל מהלך מתקדם ומאופיין באוורור ריאתי חסימתי, היווצרות ריר ותפקוד הניקוז של הסימפונות. עץ, המתבטא בשיעול, ליחה וקוצר נשימה. על פי הגדרת WHO, אם חולה משתעל כיח ברוב הימים במשך 3 חודשים רצופים לפחות במשך יותר משנתיים רצופות, המחלה נחשבת ברונכיטיס כרונית (CB). ברונכיטיס כרונית מחולקת לראשונית ומשנית. ברונכיטיס כרונית ראשונית היא מחלה עצמאית שאינה קשורה לתהליכים אחרים של הסימפונות או לפגיעה באיברים ומערכות אחרות, שבהן קיים נגע מפוזר של עץ הסימפונות. CB משני מתפתח על רקע מחלות אחרות - הן ריאתית (שחפת, ברונכיאקטזיס וכו') והן מחוץ לריאה (אורמיה, אי ספיקת לב וכו'). לרוב זה מקומי באופיו (סגמנטלי). שקול HB ראשוני. אטיולוגיה. הן גורמים אקסוגניים (עשן טבק, זיהום אוויר, תנאים מקצועיים שליליים, גורמים אקלימיים וזיהומיים) והן גורמים אנדוגניים (פתולוגיה של הלוע האף, פגיעה בנשימה דרך האף, מחלות נשימה חריפות חוזרות ונשנות, ברונכיטיס חריפה וזיהום מוקדי של דרכי הנשימה העליונות) לשחק תפקיד בפיתוח מסלולי CB, נטייה תורשתית, הפרעות מטבוליות (השמנה)). פתוגנזה. בהשפעת אקסוגניים ובהשתתפות גורמים אנדוגניים בעץ הטראכאוברונכיאלי, המאפיינים המבניים והתפקודיים של הקרום הרירי והשכבה התת-רירית משתנים, מתפתחת דלקת של הקרום הרירי ותפקוד הפטנטי והניקוז של הסמפונות מופרעים. שינויים מבניים ותפקודיים בקרום הרירי ובשכבת התת-רירית מתבטאים בהיפרפלזיה ותפקוד יתר של תאי גביע, בלוטות הסימפונות, הפרשת יתר של ריר עבה וצמיג, מה שמוביל להפרעה במערכת ההובלה הרירית. כמות הפרישים של IgA-lysozyme ולקטופרין מופחתת. בצקת של הקרום הרירי מתפתחת, ולאחר מכן - ניוון ומטאפלזיה של האפיתל. דלקת של הקרום הרירי נגרמת על ידי חומרים מגרים שונים בשילוב עם זיהום (ויראלי וחיידקי). לחומרים כימיים (מזהמים) הכלולים באוויר יש השפעה מזיקה על דרכי הנשימה, נוצרת נפיחות של הקרום הרירי ומתרחשת עיכוב פעילות האפיתל הריסי. זה מוביל להפרה של הפינוי וירידה בתפקוד המחסום של רירית הסימפונות. תוכן קטרל מוחלף בקטרל-מוגלתי, ולאחר מכן מוגלתי. התפשטות התהליך הדלקתי למקטעים המרוחקים של עץ הסימפונות משבשת את ייצור החומר הפעילי השטחי ומפחיתה את פעילותם של מקרופאגים מכתשי הפגוציטים חלקיקים זרים. אם הברונכוספזם המתרחש במקרה של דלקת בולט, אז מתפתח מרכיב ברונכוספסטי (לא אלרגי). הזיהום הנלווה במהלך החמרה של הדלקת תורם להתפתחות מרכיב אסתמטי (אלרגי), המאפשר לייחס CB כזה לטרום אסטמה. תסמונת חסימתית מתפתחת עקב שילוב של מספר גורמים: 1) עווית של שרירים חלקים של הסימפונות כתוצאה מהשפעות מגרים של גורמים אקסוגניים ושינויים דלקתיים בקרום הרירי; 2) הפרשת יתר של ריר, שינויים בתכונותיו הריאולוגיות, המובילות להפרעה בהובלה רירית וחסימה של הסמפונות עם סוד צמיג; 3) מטפלזיה של אפיתל מקשקשיות גליליות לשכבות והיפרפלזיה שלה; 4) הפרות של ייצור חומרי שטח; 5) בצקת דלקתית וחדירת רירית; 6) קריסה של סימפונות קטנים ומחיקת ברונכיולים; 7) שינויים אלרגיים בקרום הרירי. אם מעורבים בתהליך הסימפונות בקליבר גדול (ברונכיטיס פרוקסימלי), חסימת הסימפונות אינה מתבטאת. אבל במקרה של נזק לסמפונות קטנים ובינוניים, מתרחשת הפרה בולטת של הפטנציה הסימפונות. עם זאת, עם נגע מבודד של סימפונות קטנים (ברונכיטיס דיסטלי), נטול קולטני שיעול, קוצר נשימה עשוי להיות העדות היחידה לברונכיטיס מפותחת, ושיעול מופיע כאשר סימפונות גדולים יותר מעורבים בתהליך. יחסים שונים של שינויים בקרום הרירי גורמים להיווצרות צורה קלינית מסוימת: 1) עם ברונכיטיס לא חסימתית קטארלית, שוררים שינויים שטחיים בתכונות המבניות והתפקודיות של הקרום הרירי; 2) עם ברונכיטיס מוקופורולנטי (מוגלתי), התהליכים של דלקת זיהומית שולטים. עם זאת, מצב אפשרי גם כאשר ברונכיטיס catarrhal לטווח ארוך עקב תוספת של זיהום יכול להיות mucopurulent, וכו 'בגרסה הלא חסימתית של כל הצורות הקליניות של ברונכיטיס כרונית, הפרעות אוורור בולטות מעט; 3) הפרעות חסימתיות מופיעות בתחילה רק על רקע החמרה של המחלה ונגרמות משינויים דלקתיים בסימפונות, היפר ודיסקריניה, ברונכוספזם (מרכיבים הפיכים של חסימה), אך לאחר מכן הן נמשכות ללא הרף, בעוד התסמונת החסימתית גדלה. לאט. בברונכיטיס כרונית חסימתית, עיבוי הקרום הרירי והשכבה התת-רירית שולטים בצקת והפרשת יתר, וגם הפרעות אוורור מתמשכות אופייניות. חסימה מפותחת של הסימפונות הקטנים מובילה לאמפיזמה. במהלכה, HB עוברת אבולוציה מסוימת. כתוצאה מהתפתחות של אמפיזמה ו-pneumosclerosis, אוורור לא אחיד של הריאות הוא ציין, אזורים hyper-ו hypoventilated נוצרים. בשילוב עם שינויים דלקתיים מקומיים, הדבר מוביל לפגיעה בחילופי גזים, אי ספיקת נשימה, היפוקסמיה עורקית ויתר לחץ דם ריאתי, ולאחר מכן התפתחות המצב העיקרי מסכן החיים - אי ספיקת חדר ימין. מיון. אין כיום סיווג מקובל של CB. חשוב לחלק את ה-CB לווריאציות חסימתיות ולא חסימות, כאשר כל אחת מהן יכולה להתפתח תהליך דלקתי קטראלי (רירי), קטרל-מוגלתי או מוגלתי. הסיווג כולל גם צורות נדירות - CB דימומי ופיבריני. לפי רמת הנזק הסימפונות, הם מבחינים: עם נגע דומיננטי, ברונכי גדולה (ברונכיטיס פרוקסימלי) ועם נגע דומיננטי של סימפונות קטנים (ברונכיטיס דיסטלי) (N. R. Paleev, 1985). תמונה קלינית. התסמינים העיקריים של CB הם שיעול, ייצור כיח וקוצר נשימה. במהלך החמרה של המחלה או עקב היפוקסיה עם התפתחות אי ספיקת ריאות וסיבוכים אחרים, מזוהים תסמינים כלליים (הזעה, חולשה, עלייה בטמפרטורת הגוף, עייפות וכו'). שיעול הוא הביטוי האופייני ביותר למחלה. בהתבסס על האופי והעקביות של הליחה, אפשר להניח וריאנט של מהלך המחלה. בגרסה הלא חסימתית של ברונכיטיס קטארלית, השיעול מלווה בשחרור של כמות קטנה של כיח רירי ומימי (בדרך כלל בבוקר, לאחר פעילות גופנית או עקב נשימה מוגברת). בתחילת המחלה, השיעול אינו מטריד את החולה; המראה של שיעול התקפי מעיד על התפתחות של חסימה הסימפונות. השיעול מקבל גוון נובח והוא התקפי באופיו עם קריסה נשימתית בולטת של קנה הנשימה וסמפונות גדולים. עם ברונכיטיס מוגלתי ומוקופורולנטי, החולים מודאגים יותר משיעול כיח. במקרה של החמרה במחלה, הליחה מקבלת אופי מוגלתי, כמותה עולה, לעיתים ליחה מופרשת בקושי (עקב חסימת הסימפונות בזמן החמרה). בגרסה החסימתית של ברונכיטיס, השיעול אינו פרודוקטיבי ופורץ, מלווה בקוצר נשימה, עם כמות קטנה של כיח. קוצר נשימה מופיע בכל החולים עם ברונכיטיס כרונית בזמנים שונים. הופעת קוצר נשימה בחולי "שיעול ממושך" בתחילה עם מאמץ פיזי משמעותי מעידה על תוספת של חסימת הסימפונות. ככל שהמחלה מתקדמת, קוצר הנשימה הופך בולט יותר וקבוע יותר, כלומר, מתפתחת אי ספיקה נשימתית (ריאתית). בגרסה הלא חסימתית, CB מתקדם באיטיות, קוצר נשימה מופיע בדרך כלל 20-30 שנה לאחר הופעת המחלה. חולים כאלה כמעט אף פעם לא מתקנים את הופעת המחלה, אלא רק מצביעים על הופעת סיבוכים או החמרות תכופות. האנמנזה מגלה רגישות יתר לקירור, ורוב החולים מדווחים על עישון ממושך. במספר חולים המחלה קשורה לסכנות תעסוקתיות בעבודה. בעת ניתוח היסטוריה של שיעול, יש צורך לוודא כי למטופל אין פתולוגיה אחרת של מנגנון הסימפונות הריאה (שחפת, גידולים, ברונכיאקטזיס, פנאומוקונוזיס, מחלות מערכתיות של רקמת החיבור וכו'), המלווה באותם תסמינים. לפעמים היסטוריה מצביעה על hemoptysis עקב פגיעות קלה של רירית הסימפונות. hemoptysis חוזר מצביע על צורה דימומית של ברונכיטיס. בנוסף, המופטיזיס בברונכיטיס כרונית ארוכת טווח עשויה להיות התסמין הראשון של סרטן ריאות או ברונכיאקטזיס. אבחון. אוסקולט חושף נשימה קשה (עם התפתחות אמפיזמה היא עלולה להיחלש) וצפצופים יבשים בעלי אופי מפוזר, שגווניו תלוי בקליבר של הסמפונות הפגועים (צפצופים, הנשמעים בבירור בנשיפה, אופייניים לנזק לסימפונות קטנים ). השינויים בנתוני ההאזנה יהיו מינימליים בברונכיטיס כרונית לא חסימתית בהפוגה והבולטים ביותר במהלך החמרה של התהליך (פרקים רטובים בקליברים שונים שעלולים להיעלם לאחר שיעול טוב וייצור כיח). עם החמרה של ברונכיטיס חסימתית, קוצר הנשימה עולה, התופעות של אי ספיקת נשימה מתגברות. סוד צמיג מוגלתי מסבך עוד יותר את סבלנות הסמפונות. המרכיב החסימתי שהצטרף הן לצורות הקטררליות והן לצורות המוקופורולנטיות של ברונכיטיס, ובמהלך תקופת ההחמרה או במהלך האבולוציה שלהן, מחמיר משמעותית את מהלך הברונכיטיס. סימנים לחסימת סימפונות: הארכת שלב הנשיפה עם נשימה רגועה ומאולצת במיוחד; צפצופים בפקיעה (מושמע טוב יותר בנשימה מאולצת ובתנוחת שכיבה); תסמינים של אמפיזמה ריאתית חסימתית. במקרים מתקדמים של ברונכיטיס כרונית ובתוספת סיבוכים, סימני אמפיזמה של הריאות, אי ספיקה נשימתית ולב (חדר ימין) - מופיעים לב ריאתי משוחרר: אקרוציאנוזיס, פספוס או נפיחות ברגליים וברגליים, שינויים בציפורניים ב צורת משקפי השעון, והפלנגות הסופיות של הידיים והרגליים - בצורת מקלות תיפוף, נפיחות של ורידי צוואר הרחם, פעימה באזור האפיגסטרי עקב החדר הימני, מבטא של הטון II בחלל הבין-צלעי II משמאל לעצם החזה, הגדלת כבד. משפיע על תמונת המחלה ותוספת של מרכיב אסתמטי (אלרגי), כאשר יש דמיון לאסתמה הסימפונות. לאינדיקטורים מעבדתיים ואינסטרומנטליים יש מידה שונה של משמעות בהתאם לשלב התהליך. בתקופה הראשונית של המחלה או בשלב ההפוגה, ייתכן שלא יהיו שינויים. עם זאת, לאינדיקטורים אלו חשיבות רבה לזיהוי פעילות התהליך הדלקתי; בירור הצורה הקלינית של המחלה; זיהוי סיבוכים; אבחנה מבדלת עם מחלות שיש להן תסמינים קליניים דומים. בדיקת רנטגן של איברי החזה מתבצעת בכל החולים עם ברונכיטיס כרונית, אולם ככלל, אין שינויים בריאות בצילומי רנטגן רגילים. ייתכן שיש עיוות רשת של דפוס הריאה, עקב התפתחות של דלקת ריאות. עם מהלך ארוך של התהליך, מתגלים סימנים של אמפיזמה. עם התפתחות הלב הריאתי, מופיעה בליטה של תא המטען של העורק הריאתי בקו המתאר השמאלי של צל הלב, התרחבות העורקים הבסיסיים, ואחריה היצרות בצורת חרוט שלהם וירידה בקוטר של הפריפריה. ענפים. לבדיקת רנטגן תפקיד חשוב באבחון של סיבוכים (דלקת ריאות חריפה, ברונכיאקטזיס) ובאבחנה מבדלת עם מחלות עם תסמינים דומים. ברונכוגרפיה משמשת רק לאבחון ברונכיאקטזיס. לברונכוסקופיה חשיבות רבה באבחון של ברונכיטיס כרונית ובידול שלה ממחלות המבטאות תמונה קלינית דומה. זה מאשר נוכחות של תהליך דלקתי; מבהיר את אופי הדלקת (האבחנה של ברונכיטיס דימומית או פיברינית נעשית רק לאחר מחקר זה); מגלה הפרעות תפקודיות של העץ הטראכאוברוכיאלי (חשוב במיוחד לזהות קריסת נשיפה - דיסקינזיה של קנה הנשימה וסמפונות גדולים); עוזר בזיהוי נגעים אורגניים של עץ הסימפונות. בנוסף, ברונכוסקופיה מאפשרת לקבל את תכולת הסמפונות או שטיפות למחקרים מיקרוביולוגיים, טפילולוגיים וציטולוגיים. המחקר של תפקוד הנשימה החיצונית מתבצע כדי לזהות הפרעות מגבילות וחוסמות של אוורור ריאתי. לפי הספירוגרמה, מדד ה-Tiffno מחושב (היחס בין נפח הנשיפה המאולץ ב-1 s - FEV1 ליכולת החיונית של הריאות - VC באחוזים) ואינדיקטור למהירות האוויר - PSV (יחס האוורור המקסימלי של הריאות - MVL ל-VC). עם התפתחות של תסמונת חסימתית, יש ירידה במדד המהירות המוחלט של נשימה חיצונית (MVL ו-FEV1), מעבר למידת ההפחתה של VC; מדד ה-Tiffno יורד וההתנגדות הסימפונות בפקיעה עולה. לפי pneumotachometry, הדומיננטיות של כוח ההשראה על פני כוח הנשיפה מתגלה כסימן מוקדם לחסימת הסימפונות. זיהוי הפרות של פטנטיות הסימפונות ברמות שונות של עץ הסימפונות אפשרי בעזרת פנאומוטכוגרפים מיוחדים, המאפשרים לקבל עקומת "זרימה - נפח". חסימה היקפית מאופיינת בירידה משמעותית בעקומת הזרימה-נפח באזור הנפח הנמוך. ההערכה המשותפת של תנגודת הסימפונות ונפחי הריאות עוזרת גם היא לקבוע את רמת החסימה. במקרה של חסימה בגובה הסמפונות הגדולים, חלה עלייה בנפח השיורי של הריאות (RLV), ויכולת הריאה הכוללת (TLC) אינה עולה. עם חסימה היקפית, נצפית עלייה משמעותית יותר ב-TRL ועלייה ב-TRL. כדי לזהות את חלקו של עווית הסימפונות בשיעור הכולל של חסימת הסימפונות, אוורור ומכניקת הנשימה נלמדות לאחר סדרה של בדיקות תרופתיות. לאחר שאיפת תרסיסים מרחיבי סימפונות, ביצועי האוורור משתפרים בנוכחות מרכיב ספסטי של חסימת דרכי הנשימה. רדיופולמונוגרפיה באמצעות האיזוטופ הרדיואקטיבי 133Xe מתבצעת כדי לזהות אוורור לא אחיד הקשור לחסימת הסמפונות הקטנים. זהו הסימן האבחוני המוקדם ביותר לסוג זה של חסימת הסימפונות. אלקטרוקרדיוגרפיה נחוצה כדי לזהות היפרטרופיה של החדר הימני והאטריום הימני המתפתחת עם יתר לחץ דם ריאתי. סטייה בולטת של ציר QRS ימינה, תזוזה של אזור המעבר שמאלה (R / S < 1 ב-V4-V6), ECG מסוג S מזוהים; גל P חד גבוה במובילים VF, III, II. בדיקת דם קלינית מגלה אריתרוציטוזיס משנית הנובעת מהיפוקסיה כרונית עם התפתחות של אי ספיקה ריאתית חמורה. אינדיקטורים של "שלב חריף" מתבטאים בצורה מתונה: ESR תקין או מוגבר באופן מתון, לויקוציטוזיס קטן, כמו גם הסטת נוסחת הלויקוציטים שמאלה. כעדות לביטויים אלרגיים, אאוזינופיליה אפשרית. מחקר של כיח ותכולת הסימפונות עוזר לקבוע את חומרת הדלקת. עם דלקת חמורה, התוכן מוגלתי או מוגלתי-רירי, מכיל נויטרופילים רבים ומקרופאגים בודדים, תאים שהשתנו דיסטרופית של אפיתל הריצות והקשקשיים מיוצגים בצורה גרועה. עבור דלקת מתונה, התוכן קרוב יותר למוקופורולנטי; מספר הנויטרופילים מצטמצם, מספר המקרופאגים, הריר ותאי האפיתל הסימפונות עולה. עם דלקת קלה, תוכן הסימפונות הוא רירי, תאים מפורקים של האפיתל והסמפונות שולטים; מקרופאגים ונויטרופילים מעטים. בדיקה מיקרוביולוגית של כיח ותכולת הסימפונות חשובה כדי לזהות את האטיולוגיה של החמרות של ברונכיטיס כרונית והבחירה בטיפול אנטי-מיקרוביאלי. אבחון דיפרנציאלי. לוח 10 קריטריונים לאבחון דיפרנציאלי עבור CB
טיפול. כולל סט של מדדים שונים במהלך תקופת ההחמרה וההפוגה של המחלה. במהלך תקופת החמרה של מחלה כרונית, שני כיווני טיפול נבדלים: אטיוטרופי ופתוגני. טיפול אטיוטרופי מכוון להעלמת התהליך הדלקתי בסימפונות: יש לציין טיפול באנטיביוטיקה, תרופות סולפה, חומרי חיטוי, פיטונסידים וכו'. הטיפול מתחיל באנטיביוטיקה מסדרת הפניצילין (פניצילין, אמפיצילין) או קבוצה של צפלוספורינים (צפמסין). , tseporin), ובהיעדר השפעה, אנטיביוטיקה של הקבוצה משמשת רזרבה (gentamicin, וכו '). דרך המתן המועדפת ביותר היא תוך קנה הנשימה (תרסיס או מילוי במזרק גרון דרך ברונכוסקופ). טיפול פתוגנטי מכוון לשיפור אוורור ריאתי; שחזור של סבלנות הסימפונות; שליטה על יתר לחץ דם ריאתי ואי ספיקת חדר ימין. שיקום האוורור הריאתי, בנוסף לחיסול התהליך הדלקתי בסימפונות, מקל על ידי טיפול בחמצן וטיפול בפעילות גופנית. הדבר העיקרי בטיפול בברונכיטיס כרונית - שחזור של ספיפות הסימפונות - מושג על ידי שיפור הניקוז שלהם וביטול ברונכוספזם. כדי לשפר את ניקוז הסימפונות, מכיחים נקבעים (משקה אלקליין חם, מרתח עשבי תיבול, מוקלטין וכו'), תרופות מוקוליטיות (אצטילציסטאין, ברומהקסין; עם הפרשה צמיגה מוגלתית - אירוסולים של אנזימים פרוטאוליטיים - כימופסין, טריפסין); נעשה שימוש ברונכוסקופיה טיפולית. כדי לחסל ברונכוספזם, eufillin משמש (תוך ורידי, בנרות, טבליות), אפדרין, אטרופין; פגישות בודדות בתרסיס של תרופות סימפטומימטיות אפשריות: fenoterol, orciprenaline sulfate (asthmopenta) ותרופה מקומית חדשה "Soventol", תרופות אנטיכולינרגיות: atrovent, troventol. הכנות יעילות של אמינופילין ממושך (teopec, teodur, theobelong וכו') - 2 פעמים ביום. בהיעדר השפעה של טיפול כזה, מנות קטנות של קורטיקוסטרואידים ניתנות דרך הפה (10-15 מ"ג פרדניזולון ליום) או תוך קנה הנשימה (השעיה הידרוקורטיזון - 50 מ"ג). כטיפול נוסף, מנה: 1) תרופות נגד שיעול: עם שיעול לא פרודוקטיבי - libexin, tusuprex, bromhexine, עם שיעול פריצה - קודאין, דיונין, stoptussin; 2) תרופות המגבירות את עמידות הגוף: ויטמינים A, C, קבוצה B, ממריצים ביוגנים. כיום, בטיפול בברונכיטיס כרונית, נעשה שימוש יותר ויותר בתרופות מתקנות אימונו: T-activin או thymalin (100 מ"ג תת עורית למשך 3 ימים); בפנים - קטרג'ן, נתרן נוקלינאט או פנטוקסיל (תוך שבועיים), לבמיסול (דקריס). טיפול פיזיותרפיה: מרשם דיאטרמיה, אלקטרופורזה של סידן כלוריד, קוורץ באזור החזה, עיסוי חזה ותרגילי נשימה. עם ברונכיטיס בינוני עד חמור, יחד עם טיפול נגד הישנות וטיפול בבריאות, חולים רבים נאלצים לקבל כל הזמן תרופות תומכות. טיפול תחזוקה נועד לשפר את סבלנות הסימפונות, הפחתת יתר לחץ דם ריאתי ומלחמה באי ספיקת חדר ימין. אותן תרופות נקבעות כמו בתקופת ההחמרה, רק במינונים קטנים יותר, בקורסים. תחזית. הפרוגנוזה להחלמה מלאה היא לא חיובית. הפרוגנוזה הפחות טובה היא ל-CB חסימתיים ול-CB עם נזק דומיננטי לסימפונות הדיסטליים, מה שמוביל במהירות להתפתחות של אי ספיקת ריאות ולהיווצרות cor pulmonale. הפרוגנוזה הטובה ביותר היא ל-CB שטחי (קטארלי) ללא חסימה. הרצאה מס' 8. מחלות מערכת הנשימה. דלקת ריאות דלקת ריאות היא מחלה זיהומית ודלקתית חריפה בעלת אופי מוקדי, שבה חלקי הנשימה ורקמת החיבור הבין-סטיציאלית של הריאות מעורבים בתהליך הפתולוגי. סיווג מאת E.V. Gembitsky (1983). לפי אטיולוגיה: 1) חיידקי (המציין את הפתוגן); 2) ויראלי (המציין את הפתוגן); 3) קורניטי; 4) ריקטסיאל; 5) מיקופלזמה; 6) פטרייתי; 7) מעורב; 8) זיהומיות-אלרגיות; 9) אטיולוגיה לא ידועה. לפי פתוגנזה: 1) ראשוני (תהליך דלקתי חריף עצמאי); 2) משני (סיבוך של מחלות של מערכת הלב וכלי הדם עם הפרעות במחזור הדם במחזור הדם הריאתי, מחלות כרוניות של הכליות, מערכות הדם, חילוף חומרים, מחלות זיהומיות או להתפתח על רקע מחלות נשימה כרוניות). מאפיינים קליניים ומורפולוגיים: 1) parenchymal (עבור דלקת ריאות פנאומוקוקלית): croupous; מוֹקְדִי; 2) מודעת ביניים. לפי לוקליזציה והיקף: חד צדדי; דוּ צְדָדִי. לפי חומרה: חמור ביותר; כָּבֵד; לְמַתֵן; קלה ומוצלחת. במורד הזרם: חד; ממושך (רזולוציה רדיולוגית וקלינית של דלקת ריאות). אטיולוגיה. רוב דלקות הריאות הן ממקור זיהומיות. דלקת ריאות אלרגית וכאלה הנגרמות על ידי גורמים פיזיקליים או כימיים הם נדירים. דלקת ריאות חיידקית מאובחנת לעתים קרובות יותר בקרב אנשים בגיל העמידה וקשישים; דלקת ריאות ויראלית - בצעירים. באטיולוגיה של דלקת ריאות חיידקית ראשונית, התפקיד המוביל שייך ל-pneumococci. במהלך מגיפת שפעת, התפקיד של אסוציאציות ויראליות-חיידקיות (בדרך כלל סטפילוקוקוס), כמו גם מיקרואורגניזמים אופורטוניסטיים, גובר. בדלקת ריאות משנית, את התפקיד האטיולוגי המוביל ממלאים חיידקים גרם שליליים (דלקת ריאות קלבסיאלה ובצילוס שפעת); בהתרחשות של דלקת ריאות שאיפה, החשיבות של זיהום אנאירובי היא רבה. פתוגנזה. הפתוגן הזיהומי נכנס מבחוץ למקטעי הנשימה של הריאות דרך הסמפונות: שאיפה ושאיפה (מהלוע האף או מהלוע האף). בדרך המטוגני, הפתוגן חודר לריאות בעיקר במהלך דלקת ריאות משנית או במהלך התהוות הטרומבוטית של דלקת ריאות. התפשטות לימפוגנית של זיהום עם התרחשות של דלקת ריאות נצפית רק עם פצעים בחזה. קיים גם מנגנון אנדוגני להתפתחות דלקת ברקמת הריאה, עקב הפעלת המיקרופלורה בריאות. תפקידו גדול בדלקת ריאות משנית. התפתחות דלקת ריאות מתאפשרת על ידי גורמים שליליים של הסביבה החיצונית והפנימית, שבהשפעתם יש ירידה בהתנגדות הבלתי ספציפית הכללית של הגוף (דיכוי פגוציטוזיס, ייצור בקטריוליזינים וכו') ודיכוי של מקומיים מנגנוני הגנה (ליקוי בפינוי רירי, ירידה בפעילות הפגוציטית של מקרופאגים מכתשי ונויטרופילים וכו'). חשיבות משמעותית בפתוגנזה של דלקת ריאות מיוחסת גם לתגובות אלרגיות ואוטואלרגיות. ספרופיטים ומיקרואורגניזמים פתוגניים, ההופכים לאנטיגנים, תורמים לייצור נוגדנים המקובעים על תאי הקרום הרירי של דרכי הנשימה, שם מתרחשת תגובת האנטיגן-נוגדן, מה שמוביל לנזק לרקמות ולהתפתחות התהליך הדלקתי. בנוכחות של דטרמיננטים אנטיגנים נפוצים של מיקרואורגניזמים ורקמת ריאה, או כאשר רקמת הריאה ניזוקה על ידי וירוסים, מיקרואורגניזמים, רעלים וחומרים רעילים, מה שמוביל לביטוי התכונות האנטיגניות שלה, מתפתחים תהליכים אוטואלרגיים. תהליכים אלו תורמים לקיום ארוך יותר של שינויים פתולוגיים ולמהלך ממושך של המחלה. תמונה קלינית. תסמונות עיקריות: 1) שיכרון (חולשה כללית, עייפות, כאבי ראש וכאבי שרירים, קוצר נשימה, דפיקות לב, חיוורון, אובדן תיאבון); 2) תסמונת של שינויים דלקתיים כלליים (תחושת חום, צמרמורות, חום, שינויים בפרמטרים של שלב החריף בדם: לויקוציטוזיס עם הסטה של נוסחת הלויקוציטים שמאלה, עלייה ב-ESR, רמת פיברינוגן, α2-גלובולינים, הופעת חלבון C-reactive); 3) תסמונת של שינויים דלקתיים ברקמת הריאה (הופעה של שיעול וליחה, קיצור צליל הקשה), רעד קול מוגבר וברונכופוניה, שינויים בתדירות ובאופי הנשימה, הופעת גלים לחים, שינויים רדיולוגיים; 4) תסמונת מעורבות של איברים ומערכות אחרים. חומרת הביטויים הללו מאפיינת את חומרת מהלך דלקת הריאות (ראה טבלה 11). לוח 11 תסמינים ומהלך של דלקת ריאות
בשלבים שונים של מהלך דלקת הריאות, התמונה הקלינית עשויה להשתנות מתוספת של סיבוכים מסוימים: ריאתי וחוץ ריאתי. ריאתי: היווצרות אבצס; פלאוריטיס (פארא ומטפנאומוני), לעתים רחוקות יותר - אמפיאמה פלאורלית; הצטרפות של מרכיב אסתמטי, היווצרות בצקת ריאות והתפתחות של כשל נשימתי חריף אפשרי. סיבוכים חוץ ריאתיים: הלם זיהומי-רעיל (עם תסמינים של אי ספיקת כלי דם חריפה, אי ספיקת כליות וחדר שמאל חריף, כיב של הקרום הרירי של מערכת העיכול ודימום, התפתחות של קרישה תוך-וסקולרית מפושטת; דלקת שריר הלב זיהומית-אלרגית; דלקת קרום הלב זיהומית; דלקת קרום המוח או דלקת קרום המוח; דלקת כליה; הפטיטיס בדלקת ריאות croupous חמורה, התפתחות פסיכוזות שיכרון אפשרי, ובדלקת ריאות כוללת קונפלוונטית - לב ריאתי חריף. התלונות העיקריות של חולה עם דלקת ריאות: שיעול, ייצור כיח, כאבים בחזה, מחמירים בנשימה ושיעול, קוצר נשימה, פגיעה ברווחה הכללית, חום. שיעול עשוי להיות יבש או עם ליחה (רירית, רירית, מוגלתית-רירית, דמית). כיח "חלוד" אופייני לדלקת ריאות לובארית, דמית - לדלקת ריאות הנגרמת על ידי Klebsiella (בצילוס פרידלנדר) ודלקת ריאות ויראלית; כיח דם מוגלתי מעיד על דלקת ריאות ממקור סטרפטוקוקלי. שיעול מתמשך עם כמות קטנה של כיח רירי נצפה עם דלקת ריאות מיקופלזמלית, המאופיינת גם בתחושת כאב בגרון. כאבים בצד, המחמירים בנשימה עמוקה ושיעול, אופייני לדלקת ריאות פנאומוקוקלית הלוברית, וכן מעורבות הצדר בתהליך הפתולוגי. עם לוקליזציה של דלקת ריאות בחלקים התחתונים של הריאות ומעורבות הצדר הסרעפתי בתהליך, הכאב יכול להקרין אל חלל הבטן, המדמה תמונה של בטן חריפה. אם חלק הקנים העליון או התחתון של הריאה השמאלית מעורב בתהליך, הכאבים ממוקמים באזור הלב. ב-25% מהחולים, התלונה על קוצר נשימה היא אחת המרכזיות, בעיקר עם דלקת ריאות שהתפתחה על רקע מחלות נשימה כרוניות ואי ספיקת לב. חומרת קוצר הנשימה עולה במקביל להפרה של הרווחה הכללית. תסמינים של שיכרון חמור הם האופייניים ביותר לדלקת ריאות קורניטית ומיקופלזמלית, והם נצפים גם בדלקת ריאות סטפילוקוקלית, שפעת ופנאומוקוקלית (קרופוזית). החולה עלול להיות מוטרד מצמרמורות ועלייה בטמפרטורת הגוף עד חום. על רקע כללי של שיכרון וטמפרטורת חום, מופיעים תסמינים מקומיים. אבחון. כדי לבצע אבחנה אטיולוגית חשובה הערכה נכונה של תסמיני המחלה בתחילתה. צרידות או חוסר יכולת לדבר אופייניים לדלקת ריאות הנגרמת על ידי נגיף הפאראאינפלואנזה. לכרית, כאב בעיניים, כאב גרון בעת בליעה, הפרשות רבות מהאף מבלי לשנות חלקים אחרים של דרכי הנשימה מתרחשים עם דלקת ריאות הנגרמת על ידי אדנוווירוס. המשמעותי ביותר לאבחנה היא נוכחות של תסמונת של שינויים דלקתיים ברקמת הריאה. תסמונת זו מורכבת מהתסמינים הבאים: 1) פיגור בנשימה של הצד הפגוע של החזה; 2) קיצור צליל הקשה באזור הקרנת הנגע במידה רבה או פחותה; 3) רעד קול מוגבר וברונכופוניה באותו אזור; 4) שינוי באופי הנשימה (קשה, ברונכיאלי, מוחלש וכו'); 5) הופעת רעשים נשימתיים פתולוגיים (קולות רטובים מבעבעים עדינים וקרפיטוס). אופי הנשימה יכול להשתנות בדרכים שונות. בשלב הראשוני של דלקת ריאות croupous, הנשימה יכולה להיות מוחלשת, עם נשיפה ממושכת; בשלב ההפטיזציה, יחד עם עלייה בקהות צליל ההקשה, נשמעת נשימה הסימפונות; עם הרזולוציה של המוקד הריאות עם ירידה בקהות הקשה, הנשימה הופכת קשה. עם דלקת ריאות מוקדית, הסימפטומים הקבועים ביותר הם נשימה קשה ולח, צלצול רעלים מבעבעים עדינים. עם זאת, עם דלקת ריאות הילרית מרכזית, הנתונים הפיזיים מוצגים בצורה גרועה מאוד, וזיהוי דלקת ריאות אפשרי רק לאחר בדיקת רנטגן. דלקות ריאות של Mycoplasma נבדלות על ידי מחסור בנתונים פיזיים. שיכרון חמור, בשילוב עם מספר קטן מאוד של צפצופים, נצפית בדלקת ריאות הנגרמת על ידי דלקת ריאות Klebsiella. במקרים מסוימים, במהלך ההאזנה, עלולים לבוא לידי ביטוי מספר רב של רעלים יבשים של בס וטרבל, שאינם אופייניים לתסמונת ההסתננות הדלקתית. זה קורה עם דלקת ריאות שהתפתחה על רקע ברונכיטיס כרונית; דלקת ריאות הנגרמת על ידי המקל של פייפר; במקרה של הצטרפות לדלקת ריאות של מרכיב אלרגי. תסמינים עוזרים לבצע אבחנה אטיולוגית: 1) זיהוי של כתמים קטנים, כמו עם אדמת, פריחה בשילוב עם לימפדנופתיה אופיינית לזיהום בנגיף אדנו; 2) הגדלה מקומית של בלוטות הלימפה מצביעה על דלקת ריאות פריפוקלית; 3) דלקת ריאות פטרייתית בשילוב עם נגעים של הריריות, העור והציפורניים; 4) תסמונת hepatolienal וצהבת קלה נמצאים בדלקות ריאות קורניטיות ו-Curickettsial; 5) עבור דלקת ריאות croupous טיפוסית, המראה של המטופל הוא אופייני: פנים חיוורות עם סומק קדחתני בצד הנגע, התפרצויות הרפטיות, נפיחות של כנפי האף בעת נשימה. השיטה החשובה ביותר לבירור נוכחות דלקת ריאות ומידת המעורבות של רקמת הריאה בתהליך היא פלואורוגרפיה גדולה ובדיקת רנטגן של איברי החזה. דלקות ריאות סטפילוקוקליות נבדלות על ידי פילוח ברור של נגעי ריאות עם מעורבות של מספר מקטעים בתהליך. הסימן הרדיולוגי האופייני להם הוא היווצרות של חללים מרובים בריאות מסוג pneumocele ביום 5-7 מתחילת המחלה, ומאוחר יותר - חללים נמקיים עם נוכחות של נוזל. בניגוד למורסות אמיתיות, התצורה ומספר החללים משתנים במהירות. נגע לובר הוא ביטוי של דלקת ריאות croupous או דלקת ריאות הנגרמת על ידי Klebsiella. האונה העליונה, בעיקר הריאה הימנית, מושפעת לרוב. בדיקת רנטגן מגלה תפליט בחלל הצדר. לעתים קרובות מתרחשת תפליט כזה עם דלקת ריאות סטרפטוקוקלית, עם דלקת ריאות הנגרמת על ידי מקל פייפר, אשר ממוקם באונה התחתונה ואצל 2/3 מהחולים לוכד יותר מאונה אחת של הריאה. נתוני בדיקת רנטגן חשובים במיוחד באיתור דלקת ריאות עם שינויים קלים (דלקת ריאות אינטרסטיציאלית והילרית). במקרים מסוימים, להבהרת האבחנה, מצוינות טומוגרפיה וברונכוגרפיה, המסייעות להבהרת האבחנה במקרים של נסיגה מאוחרת של שינויים מסתננים, עם מהלך מסובך (מורסה, תפליט בחלל הצדר). הם משמשים כדי לא לכלול תהליכים פתולוגיים אחרים עם מצגות קליניות ורדיולוגיות דומות. ברונכוגרפיה חושפת חללי ריקבון ברקמת הריאה, כמו גם נוכחות של ברונכיאקטזיס, שסביבם, במהלך החמרה, יתכנו שינויים חודרניים (דלקת ריאות פריפוקל). באבחון של דלקת ריאות אוטם, מחקר רדיונוקלידים של זרימת הדם הריאתית ממלא תפקיד מסוים, חושף את הפרותיו. בדיקה בקטריולוגית של כיח (או שטיפות סימפונות) לפני רישום אנטיביוטיקה עוזרת לזהות את הפתוגן ולקבוע את רגישותו לאנטיביוטיקה. מיקרואורגניזם לא תמיד מזוהה הוא הגורם הגורם לדלקת ריאות. אבחנה אטיולוגית מדויקת יותר יכולה להתבצע באמצעות מחקרים אימונולוגיים: תגובת קיבוע משלים (RCC) ותגובת עיכוב hemagglutination (HITA) עם אנטיגנים נגיפיים וחיידקיים. באבחון של דלקת ריאות ויראלית ו-ויראלית-חיידקית יש חשיבות למחקרים וירולוגיים וסרולוגיים (תוצאות של מחקר תרבית של ליחה, כולל בדיקה ביולוגית בעכברים, שיטת טיפוח וירוסים בעובר עוף מתפתח, שיטת אימונופלואורסצנטי, א. שיטה סרולוגית באמצעות סרה מזווגת נגד וירוסים, מייחסת חשיבות לעלייה של פי 4 בלבד בטיטר הנוגדנים). בדיקת כיח עוזרת להבהיר את אופי דלקת הריאות. מספר רב של אאוזינופילים מצביע על תהליכים אלרגיים, נוכחות של תאים לא טיפוסיים מעידה על דלקת ריאות ממקור סרטני; Mycobacterium tuberculosis נמצא בשחפת; סיבים אלסטיים - עדות לקריסת רקמת הריאה. עם דלקת ריאות מיקוסיס, יחד עם זיהוי פטריות, יש חוסר בפלורה פיוגנית עקב ההשפעה המעכבת של תוצרי הפסולת של פטריות. על פי מיקרוסקופיה של מריחות כיח מוכתמות בגראם, ניתן לדבר על מיקרואורגניזמים גרם שליליים או גרם חיוביים שחיים בסימפונות כבר ביום הראשון לשהות המטופל בבית החולים. חומרת התהליך הדלקתי נשפטת על פי חומרת פרמטרי הדם בשלב החריף והדינמיקה שלהם (לויקוציטוזיס עם שינוי בנוסחת הלויקוציטים, עלייה ב-ESR, תוכן מוגבר של α2-גלובולינים, פיברינוגן, הופעת SRV, עליה ברמת החומצות הסיאליות). עם מהלך ממושך של דלקת ריאות ופיתוח סיבוכים, נלמדת התגובתיות האימונולוגית של הגוף. ירידה בחסינות ההומורלית (IgM) והתאית (הגירה מאוחרת של לויקוציטים, שינויים בבדיקות המאפיינות את מערכת הלימפוציטים מסוג T) מחייבת טיפול אימונומודולטורי. טיפול. מיד לאחר האבחון, יש צורך להתחיל טיפול אטיוטרופי בדלקת ריאות. רעיונות אמפיריים לגבי פתוגן אפשרי הם בעלי חשיבות רבה, שכן בדיקה בקטריולוגית של ליחה מתבצעת במשך זמן רב למדי וברוב החולים, גם עם גישה מודרנית למחקר זה, נותנת תוצאות לא ודאות ולעיתים שגויות. כרגע, הפניצילינים איבדו את חשיבותם כתרופה המועדפת בטיפול בדלקת ריאות. זאת בשל העובדה שמשמעותיים אטיולוגית להתפתחות דלקת ריאות, בנוסף לפנאומוקוק והמופילוס שפעת, הם מיקרואורגניזמים תוך תאיים מחייבים - Mycoplasma pneumoniae ו- Chlamydia pneumoniae, אשר עמידים להשפעות חיידקיות של אנטיביוטיקה מקבוצת β-lactam. אי אפשר להתעלם מהעובדה שרגישות יתר לתרופות אלו מתפתחת במהירות בחולים. בהקשר לאמור לעיל, בטיפול בדלקת ריאות מוקדשת תשומת לב רבה למקרולידים, אשר הוכחו כיעילים לא רק נגד פנאומוקוק, אלא גם נגד Mycoplasma pneumoniae, Chlarnydia pneumoniae. עם זאת, חשוב לא לאבד מעיני את העובדה שאריתרומיצין, שהוא הסטנדרט של קבוצת תרופות זו, בשל יציבותו הנמוכה בסביבה חומצית (ומכאן זמינות ביולוגית נמוכה), וכן השכיחות הנרחבת של זני פנאומוקוק עמידים. לאריתרומיצין, מאבד מערכו הקליני.משמעות. כתרופות בחירה, הוא הוחלף בתרופות אחרות מקבוצת המקרולידים - אזיתרומיצין, רוקסיתרומיצין, רובמיצין וכו'. מספר מקרולידים משמשים גם לשימוש פומי ופארנטרלי (לדוגמה, רובמיצין). כתוצאה מכך, השימוש בהם מוצדק במהלך החמור של התהליך הדלקתי בריאות (לדוגמה, בתחילה רובמיצין ניתן לווריד במשך 2-3 ימים, ולאחר מכן, עם הדינמיקה החיובית של התהליך הפתולוגי, המטופל עובר ל- נטילת תרופה זו דרך הפה). היתרון של רובמיצין אינו מוטל בספק, שכן הוא אינו יוצר אינטראקציה עם תיאופילינים, תוך מניעת אפשרות של מנת יתר של תרופות אלו, שכן תיאופילינים ורובמיצין משמשים יחד בטיפול בחולים עם מחלות ריאות חסימתיות כרוניות. ידוע גם שתת-קבוצה זו של מקרולידים (מקרולידים 16 איברים) הן תרופות עם רמה מינימלית של תופעות לוואי. בחולים מעל גיל 65, בשל ההטרוגניות של הספקטרום האטיולוגי של דלקת ריאות ועם מחלות ריאות חסימתיות כרוניות, ניתן להשתמש בפניצילינים חצי סינתטיים לטיפול אנטיביוטי ראשוני, ובהיעדר השפעה חיובית לאחר טיפול זה עבור 3-4 ימים, השימוש בצפלוספורינים מוצדק. חשוב לזכור שספקטרום הפעולה של צפלוספורינים מדור I וחלק מהדור השני הוא מיקרואורגניזמים גרם חיוביים וגרם שליליים, וצפלוספורינים מהדור השלישי פועלים בעיקר על פתוגנים גרם שליליים. צפלוספורינים מהדור הראשון מיוצגים ע"י צפלותין (קפלין), צפזולין (קפזול), וכו'. תרופות מהדור השני כוללות צפורוקסימה (קטוצף), צפלוסטין (בונצפין) ואחרות. צפלוספורינים מהדור השלישי: צפלוטקסיים (קלפורן), צפופרזון (ספוביד), צפטריאקסון ( longacef). דלקות ריאות בשאיפה קשורות למיקרופלורה אנאירובית או גראם-שלילית, הקובעת את השימוש באמינוגליקוזידים או צפלוספורינים מהדור השלישי בשילוב עם מטרונידזול-סמיסוקינאט (500 מ"ג לווריד 2-3 פעמים ביום). מצבי כשל חיסוני משפיעים גם על אופי התרופות שנבחרו, אשר במקרה זה תלוי באופי הפתוגן. במקרים כאלה, התוכנית המיושמת מורכבת מאמינוגליקוזידים וצפלוספורינים מודרניים. משך הטיפול האנטיביוטי היעיל לחולה עם דלקת ריאות הוא 7-10 ימים. כאשר רושמים טיפול, יש לקחת בחשבון שב-7-15% מהמקרים ייתכן שלא תהיה השפעה מטיפול זה. זה מצביע על הצורך להחליף אנטיביוטיקה, על סמך תוצאות מחקר מיקרוביולוגי. אפשרות נוספת היא שימוש בתרופות אלטרנטיביות, מה שנקרא אנטיביוטיקה מהבחירה השנייה: צפלוספורינים מודרניים, אימיפנם, מונובקטמים, פלורוקינולונים. פלואורוקווינולונים (ofloxacin, pefloxacin, ciprofloxacin) יעילים נגד פתוגנים גרם שליליים, כולל Pseudomonas aeruginosa, וכמה קוקי גראם חיוביים (Staphylococcus aureus), אך אינם פעילים כאשר הם נחשפים לאנאירובים. ניתן לשקול בצדק את פלואורוקינולונים כחלופה למקרולידים בזיהומי כלמידיה, לגיונלה ומיקופלזמה. אנטיביוטיקה של מונובקטם בצורתם המודרנית מיוצגת על ידי aztreonam (azactam), הפעיל בעיקר נגד אירובי גרם שלילי (סלמונלה, שיגלה, פרוטאוס, Escherichia coli, Klebsiella וכו'); והוא גם יציב תחת פעולת β-lactamases. Imipenem - תרופה אנטיבקטריאלית מקבוצת ה-carbapenem, נקבעת רק בשילוב עם cilastatin, המעכב את חילוף החומרים של אימיפנם. התרופה יעילה מאוד נגד אנאירובים רבים, קוקוסים גרם חיוביים ומוטות גרם שליליים. מינון של אנטיביוטיקה המשמשת לטיפול בדלקת ריאות. 1) פניצילינים: בנזילפניצילין (500-000 IU לווריד כל 1-000 שעות או 000-6 IU כל 8 שעות תוך שרירית), אמפיצילין (500-000-1 גרם תוך ורידי כל 000 גרם תוך ורידי כל 000. אמוקסיצילין (4-0,5 גרם כל 1,0 שעות דרך הפה או 2,0-6 גרם כל 8-0,5 שעות תוך שרירית, תוך ורידי), אוקסצילין (6 גרם כל 0,5-1,0 שעות דרך הפה, תוך שרירית, תוך ורידי). 2) צפלוספורינים: דור I - צפלותין (קפלין) (0,5-2,0 גרם כל 4-6 שעות תוך שרירית, תוך ורידי), צפזולין (קפזול) (0,5-2,0 גרם, כל 8 שעות תוך שרירית, תוך ורידי), דור שני - צפורוקסימה (זינזף) , ketocef) (0,75-1,5 גרם כל 6-8 שעות תוך שרירית, תוך ורידי), דור שלישי - cefotaxime (claforan) (1,0-2,0 גרם, מקסימום עד 12 גרם ליום כל 12 שעות תוך שרירית, תוך ורידי), ceftriaxone (longacef, rocefin) (1,0-2,0-4,0 גרם כל 24 שעות תוך שרירית, תוך ורידי). 3) אמינוגליקוזידים: גנטמיצין (80 מ"ג כל 12 שעות תוך שרירית, תוך ורידי), אמיקסין (10-15 מ"ג/ק"ג כל 12 שעות תוך שרירית, תוך ורידי), טוברמיצין (ברולמיצין) (3-5 מ"ג/ק"ג כל 8 שעות תוך שרירית, תוך ורידי) . 4) מקרולידים: אריתרומיצין (0,5 גרם כל 6-8 שעות דרך הפה או 0,5-1,0 גרם כל 6-8 שעות תוך ורידי), רובמיצין (3,0 מיליון IU כל 8-12 שעות דרך הפה או 1,5. 3,0-8 מיליון IU כל 12-XNUMX שעות תוך ורידי). 5) פלואורוקווינולונים: פפלוקסצין (לפלצין) (400 מ"ג כל 12 שעות דרך הפה, IV), ציפרופלוקסצין (סיפרוביי) (500 מ"ג כל 12 שעות דרך הפה או 200-400 מ"ג כל 12 שעות תוך ורידי), אופלוקסצין (זנוצין, טריוויד) (200 מ"ג) כל 12 שעות בעל פה). 6) טטרציקלינים: דוקסיציקלין (ויברמיצין) (200 מ"ג ביום 1, בימים שלאחר מכן - 100 מ"ג כל 24 שעות דרך הפה), מינוציקלין (מינוצין) (200 מ"ג ביום 1, בימים שלאחר מכן - 100 מ"ג כל 12 שעות דרך הפה), aztreonam (azactam) (1,0-2,0 גרם כל 8-12 שעות), imipenem/cilstatin (thienam) (500 מ"ג כל 6-8 שעות תוך שרירי). כמו כן, חשוב כי, ככלל, מהלך ממושך או מתקדם של המחלה נובע מטיפול אנטיביוטי ראשוני לא מספק. עם זאת, בנוסף לכך, ישנן מספר גורמים מקומיים וסיסטמיים המובילים למהלך ארוך ומתמשך של דלקת בריאות: מדובר בחסימת דרכי אוויר מקומית (סרטן, אדנומה, חסימת ריריות ועוד); ברונכיאקטזיס (מולדת, נרכשת); סיסטיק פיברוזיס; פגמים במערכת החיסון (נרכשת); שאיפה חוזרת (כלזיה, סרטן הוושט וכו'); הפעלה של זיהום שחפת סמוי; התפתחות אבצס בריאות; טיפול אנטיביוטי לא מספק. הרצאה מס' 9. מחלות במערכת העיכול. מחלות של הוושט. דלקת בוושט וכיב פפטי של הוושט 1. דלקת בוושט חריפה דלקת בוושט חריפה היא נגע דלקתי של הקרום הרירי של הוושט הנמשך בין מספר ימים ל-2-3 חודשים. אטיולוגיה ופתוגנזה. גורמים אטיולוגיים: מחלות זיהומיות, פציעות, כוויות, הרעלה, תגובות אלרגיות, טעויות תזונתיות. מבין הגורמים הזיהומיים, המאפיינים ביותר של דלקת הוושט החריפה הם דיפטריה, קדחת ארגמן, טיפוס וטיפוס, שפעת, פאראאינפלואנזה, זיהום אדנוווירוס, חזרת. גורמים מזיקים פיזיים וכימיים מיוצגים על ידי קרינה מייננת, כוויות כימיות, מזון חם וקר מאוד ותבלינים. מיון. אין סיווג אחד. אפשר להשתמש בסיווג עבודה של דלקת בוושט חריפה. מבחינה מורפולוגית, נבדלים בין הסוגים המפורטים של דלקת הוושט החריפה: קטרל, בצקתי, שחיקתי, פסאודוממברני, דימומי, פילינג, נמק, פלגמוני. לפי אטיולוגיה: זיהומיות, כימיות, פיזיות, מזון. בשלבים אנדוסקופיים: 1 - בצקת והיפרמיה של הרירית, 2 - הופעת שחיקות בודדות בחלק העליון של קפלי הרירית הבצקתיים, 3 - בצקת משמעותית והיפרמיה של הרירית עם מוקדים של ריריות נשחקות ומדממות, 4 - " בכי "- קרום רירי נשחק בצורה דיפוזית, מדמם במגע הקל ביותר של האנדוסקופ. תמונה קלינית. Catarrhal esophagitis היא הצורה הנפוצה ביותר של esophagitis חריפה. זה מתרחש על רקע טעויות בתזונה: בעת אכילת מזון חריף, קר וחם, עם פציעות קלות, כוויות אלכוהול. זה מתבטא קלינית בצריבה וכאב מאחורי עצם החזה, מה שמאלץ את המטופלים לסרב לאוכל במשך מספר ימים. אנדוסקופית ציין ושט דלקת תואר I-II, רנטגן - היפרקינזיה של הוושט. דלקת וושט שחיקתית מתרחשת עם מחלות זיהומיות (סנפיר, טיפוס, אלח דם, תהליכים פטרייתיים) ואלרגיות. זה מופיע גם עם כוויות כימיות ופציעות של הוושט. למעשה, צורה זו של דלקת הוושט היא שלב באבולוציה של דלקת הוושט הקטרלית. התמונה הקלינית העיקרית מורכבת מהתסמינים של המחלה הבסיסית. התסמינים הקליניים דומים לאלו של דלקת הוושט הקטרלית: כאב משמעותי בחזה במהלך מעבר המזון; צרבת, גיהוקים, ריר יתר, ריח רקוב מהפה (קקוסמיה). בדוק אנדוסקופית סימנים של ושט II-III דרגה. בדיקה היסטולוגית מגלה היפרמיה, בצקת ברירית, שטפי דם, שחיקה. בדיקת רנטגן מראה שפע של ריר בוושט, מבנה מחדש של ההקלה עם היווצרות מאגרי בריום שטוחים בצורת אורך עד 1 ס"מ, והיפרקינזיה של דפנות הוושט. דלקת בוושט דימומית היא צורה קלינית נדירה של דלקת ושט שחיקתית. האטיולוגיה זהה לזו של דלקת בוושט שחיקתית. תסמונת כאב עז והמטמזיס אופייניות מבחינה קלינית. אנדוסקופיה מגלה דלקת דרגה III-IV עם דומיננטיות של המרכיב הדימומי. יש ניתוק של הקרום הרירי המדמם בצורה של רצועות דקות צרות. דלקת ושט פיברינית (פסאודוממברנית). גורמים אטיולוגיים בו הם קדחת ארגמן, דיפטריה, מחלות דם, מחלות פטרייתיות, השפעות של טיפול בקרינה. המרפאה נשלטת על ידי דיספאגיה וכאבים עזים, המחמירים לאחר אכילה, בחילות, הקאות. עם הקאות, סרטי פיברין משתחררים, ייתכן שיש hemoptysis. מבחינה אנדוסקופית, על האזורים הפגועים של הרירית, נמצאים רובדים פיבריניים אפורים וצהובים-אפורים, הנוצרים על ידי שכבות של פיברין ודטריטוס המכסות את פני הרירית. עם דחייה של פסאודוממברנות, נוצרות שחיקות שטוחות מתרפאות לאט, לפעמים כיבים מדממים. לאחר תהליך זיהומי חמור נותרות היצרות קרומיות בוושט, הנעלמות לאחר בוגינאז' חוזר. דלקת ושט קרומית (פילינג) לפי האטיולוגיה היא כימית (כוויות של הוושט), זיהומיות (הגורמים הם אלח דם, שלבקת חוגרת, אבעבועות שחורות, זיהום הרפס כללי). מרפאת המחלה משתנה - מצורות קלות, המאובחנות אנדוסקופיות, ועד קשות. במרפאה של דלקת ושט קרומית חמורה שוררים שיכרון, דיספאגיה ותסמונת כאב. דימום אפשרי, ניקוב של הוושט, mediastinitis, אשר, ככלל, מסתיים במוות. בבדיקה אנדוסקופית נצפה נזק לכל שכבות הוושט, שהאפיתל שלו נדחה בשכבות. כאשר המחלה הבסיסית שוככת, לעיתים נותרות בוושט היצרות קרומיות סימטריות וא-סימטריות או גסות. דלקת ושט נמק היא צורה נדירה של דלקת חריפה של הוושט. התפתחותו מוקלת על ידי חסינות מופחתת במחלות קשות כגון אלח דם, קדחת טיפוס, קנדידה, אי ספיקת כליות סופנית. המרפאה מאופיינת בדיספאגיה כואבת, הקאות, חולשה כללית, דימומים, התפתחות תכופה של מדיאסטיניטיס, דלקת ריאות, דלקת ריאות. לאחר הטיפול במחלה הבסיסית נותרות היצרות בוושט, המאובחנות כשינויים טרום סרטניים פקולטטיביים. דלקת ושט ספטית היא דלקת מקומית או מפוזרת נדירה של דפנות הוושט של אטיולוגיה סטרפטוקוקלית או שמתרחשת כאשר הרירית ניזוקה מגוף זר, עם כוויות, כיבים ויכולה לעבור מאיברים שכנים. לפעמים דלקת ושט פלגמונית חריפה מתרחשת כסיבוך של כל צורה של דלקת ושט חריפה, המובילה לאיחוי מוגלתי של דפנות הוושט. קריסת הדפנות מלווה בפריצת דרך של מוגלה לתוך רקמת המדיאסטינום, התפתחות של mediastinitis, דלקת פלאוריטיס, ברונכיטיס מוגלתי, דלקת ריאות, ספונדיליטיס, קרע באבי העורקים או כלי דם גדולים אחרים. הצטרפות של זיהום אנאירובי עלולה להוביל לאמפיזמה מדיסטינית או פנאומוטורקס ספונטני. התמונה הקלינית מאופיינת בשיכרון חושים, חום גבוה, כאבים מאחורי עצם החזה ובצוואר, הקאות. בבדיקה יש נפיחות בצוואר, ניידות בחלק זה של עמוד השדרה מוגבלת. המיקום של הראש מאולץ, עם נטייה לצד אחד. המחלה הופכת לעתים קרובות ל-mediastinitis מוגלתי. בבדיקות דם - היפרלוקוציטוזיס, ESR מואץ. בדיקה אינסטרומנטלית (רנטגן, אנדוסקופית) בשלב האקוטי אינה מסומנת. בתקופת ההצטלקות, חובה לבצע בדיקת רנטגן בשל הסיכון לפתח עיוותים גסים והיצרות ציטרית של הוושט. טיפול. עקרונות הטיפול בוושט חריף: אטיוטרופי, פתוגנטי וסימפטומטי. טיפול אטיוטרופי - טיפול במחלה הבסיסית. במחלות זיהומיות מסובכות על ידי דלקת בוושט חריפה, משתמשים באנטיביוטיקה (פרנטרלית). עם שינויים נמקיים ודימומים בולטים בוושט, מומלץ להימנע מאכילה במשך 2-3 שבועות. במהלך תקופה זו, יש לציין תזונה פרנטרלית, מתן תוך ורידי של הידרוליזטים של חלבונים, תערובות של חומצות אמינו, תוך-ליפידים, ויטמינים וטיפול בניקוי רעלים. לאחר הפחתת הדלקת, נקבעים מזונות חסכוניים מבחינה תרמית וכימית: חלב חם, שמנת, מרקי ירקות, דגנים נוזליים. כדי להפחית תסמינים מקומיים של דלקת - בתוך תמיסות של טאנין 1%, קולרגול - 2%, נובוקאין - 1-2% לפני הארוחות. העפיצות נלקחות במצב אופקי כשראש המיטה מונמך נמוך. בהיעדר ההשפעה של ניהול מקומי של תכשירים עפיצים, משככי כאבים לא נרקוטיים נקבעים באופן פרנטרלי. כדי להפחית את ההשפעות של דיסקינזיה של הוושט, תרופות פרוקינטיות (cerucal, raglan, cisapride) משמשות דרך הפה לפני הארוחות. עם שחיקות מרובות, הכנות ביסמוט (דנול, vikair), זריקות של solcoseryl מסומנים. עם דלקת ושט דימומית, מסובכת על ידי דימום, משתמשים בתכשירים של חומצה aminocaproic, vikasol, dicynone. עם דימום מסיבי, עירוי דם או פלזמה נקבע. עם דלקת ושט מוגלתית, נמקית, החולה צריך להיות בתזונה פרנטרלית במשך זמן רב, נעשה שימוש בטיפול מסיבי עם מספר אנטיביוטיקה, והמורסה מתנקזת. היצרות בוושט מתוקנות על ידי בוגינאז'. במקרים נדירים מבוצעת גסטרוסטומיה. תחזית. הפרוגנוזה לקטרראל ודלקת בוושט שחיקתית חיובית. היעלמות ספונטנית של הסימפטומים של דלקת הוושט אפשרית בתנאי שהמחלה הבסיסית מתוקנת כראוי. הפרוגנוזה של דלקת ושט פסאודוממברנית, אקפוליאטיבית ופלגמונית היא חמורה. בכל המקרים, בכפוף להחלמה מהמחלה הבסיסית, דלקת הוושט מסתיימת בהיווצרות היצרות צלקת, אשר לאחר מכן דורשות תיקון. חולים עם צורות חמורות של דלקת הוושט המסובכת על ידי היצרות הוושט אינם מסוגלים לעבוד. מניעה של דלקת בוושט חריפה מורכבת מאבחון וטיפול נאותים ובזמן של המחלה הבסיסית. 2. דלקת ושט כרונית דלקת ושט כרונית היא דלקת כרונית של הקרום הרירי של הוושט הנמשכת עד 6 חודשים. הגרסה השכיחה ביותר היא דלקת בוושט פפטית (רפלוקס ושט), שעלולה להסתבך על ידי כיב פפטי של הוושט. אטיולוגיה ופתוגנזה. הגורם העיקרי למחלה הוא ריפלוקס מתמיד של תוכן קיבה לוושט, לעיתים תכולת מרה ומעי, כלומר דלקת בוושט פפטית היא כוויה אספטית של הוושט על ידי חומצת קיבה. בפתוגנזה של דלקת הוושט של ריפלוקס, חשובות רגורגיטציה של תוכן חומצי והפרה של טיהור וריקון הוושט ממנו. קצב הפינוי של הוושט מגירוי כימי נקרא פינוי הוושט. עם פינוי תקין, ריפלוקס בודד של הפרשות אגרסיביות אינו גורם לרפלוקס ושט. מזון חם, אלכוהול, עישון וגורמים אקסוגניים אחרים מפחיתים את פינוי הוושט. גורמים אלו כוללים מזון מהיר, בו נבלעת כמות משמעותית של אוויר יחד עם האוכל. גם איכות המזון חשובה: בשר שומני, שומן חזיר, פסטה, תבלינים מתובלים עוזרים לעכב את פינוי המזון מהקיבה, ולאחר מכן ריפלוקס של התוכן לוושט. תרופות מפחיתות משמעותית את הטונוס של הסוגר התחתון של הוושט ומעודדות ריפלוקס: אנטגוניסטים של סידן, חנקות, משככי כאבים נרקוטיים, תרופות אנטיכולינרגיות, תיאופילין והאנלוגים שלו, תרופות מקבוצת הפרוסטגלנדינים. ישנם חמישה קריטריונים לפתוגניות של ריפלוקס ביצירת הוושט הפפטי: תדירות, נפח, רגורגיטציה, הרכב כימי, מצב רירית הוושט ורגישות לגורם כימי (דלקת הדפנות מפחיתה רגישות), קצב התרוקנות (פינוי) , אשר תלוי בעיקר בפריסטלטיקה פעילה, רוק פעולת alkalizing וליחה. התרחשות של ריפלוקס ושט מקודמת על ידי בקע של פתח הוושט של הסרעפת, כיב תריסריון, הפרעות לאחר כריתת קיבה ואלרגיות. גם נטייה לאלרגיה חשובה. בדיקה מורפולוגית של חולים עם דלקת ושט פפטית מגלה בצקת, היפרמיה של הרירית, חדירת התת-רירית של המקטע הסופרדיאפרגמטי של הוושט. קיימות שתי אפשרויות להתפשטות של דלקת כרונית - דלקת ושט רפלוקס מלאה ומקומית. עם מעורבות בתהליך של יותר מ 2/3 של רירית הוושט, התפתחות של reflux tracheitis, reflux bronchitis אפשרי. בחלק העליון של קפלי הוושט מתרחשות שחיקות, כיבים קטנים (במקומות של השקיה מרבית עם תוכן קיבה). דלקת כרונית של הוושט מובילה להתכווצות ספסטית ולקיצור של האיבר. תמונה קלינית. סימנים אופייניים של ריפלוקס ושט כוללים תחושת צריבה מאחורי עצם החזה, צרבת, רגורגיטציה, אשר מחמירה בשכיבה, דיספגיה והשפעה חיובית של נטילת סותרי חומצה. כאבים בחזה עלולים להופיע לאחר אכילה, המזכירים אנגינה פקטוריס. התרחשות כאב ברפלוקס ושט קשורה לגירוי פפטי של דופן הוושט ולעוויתות שלו במהלך רגורגיטציה של תוכן קיבה חומצי, כמו גם עם הפרה של הרירית הצניחת. מאפיינים בולטים של כאב זה: אופיו הארוך והצורב, לוקליזציה בתהליך ה-xiphoid, הקרנה לאורך הוושט, לעתים רחוקות יותר לחצי השמאלי של בית החזה, אין השפעה ניכרת מנטילת נוגדי חומצה, נוגדי עוויתות, עלייה במצב אופקי, במיוחד לאחר אֲכִילָה. יש לתת תשומת לב מיוחדת באבחון קליני לתסמינים קלים של דיספאגיה, כגון תחושת גוש מאחורי עצם החזה, תחושת מזון חם העובר בוושט. סימן לדלקת הוושט מתחילה בהדרגה עשוי להיות ריור והרגל של שתיית מים עם האוכל. בדיקה גופנית של חולים עם רפלוקס ושט אינה מספקת מידע משמעותי מבחינה אבחנתית. סיבוכים של ריפלוקס ושט כוללים דימום, כיב, היצרות, קיצור של הוושט וממאירות. דלקת ושט ריפלוקס כרונית יכולה להוביל להתפתחות של בקע היאטלי צירי. אבחון ואבחון מבדל. שיטת המחקר היקרה ביותר לפתולוגיה זו היא אנדוסקופיה, שבמהלכה מציינים היפרמיה, בצקת ועיבוי קפלי הקרום הרירי. ציפוי לבנבן המכסה את הקרום הרירי הוא אמין, אשר בשלבים הראשונים של המחלה יכול להיות דק, בקושי מורגש, אבל עם תהליך ארוך - לבן מסיבי או אפור מלוכלך. באזורים מסוימים, על רקע של רובד לבן, נראה לעתים קרובות הקרום הרירי האדום הבוהק של הוושט. במקרים מסוימים מתגלים פגמים שחוקים וכיבים בצורת פסים. שינויים בקרום הרירי יכולים להתאים לכל אחד מארבעת השלבים של דלקת הוושט: מהיפרמיה ועד לקרום רירי "בוכה". עם דלקת בוושט חמורה, הרבה רוק וליחה מצטברים בלומן. pH-metry, בניגוד לאנדוסקופיה, מאפשרת להעריך בצורה אובייקטיבית יותר את פינוי הוושט. צילומי רנטגן חושפים ריפלוקס קיבה-וופגיאלי. יש צורך להבחין ברפלוקס ושט עם כיב פפטי של הקיבה והתריסריון, מחלת לב כלילית, דלקת כיס המרה כרונית ודלקת לבלב. התסמין המוביל באבחנה המבדלת הוא כאב. הבחנה עם כיב פפטי מסייעת בהיעדר כאבים מאוחרים ו"רעבים" בדלקת הוושט, כמו גם נתונים המתקבלים מאנדוסקופיה של הוושט והקיבה. כאבים כליליים, בניגוד לדלקת הוושט, מתאפיינים בקשר עם מתח פיזי ורגשי, השפעת חנקות, סימני איסכמיה על ה-ECG, כולל כאלו לפי ארגומטריית אופניים. נתוני אולטרסאונד של איברי הבטן עוזרים לשלול את הפתולוגיה של כיס המרה והלבלב כגורם לתסמונת הכאב. טיפול. טיפול ברפלוקס ושט כולל טיפול במחלות שגרמו לה ורישום טיפול אנטי ריפלוקס. למטופלים מומלץ להימנע מהרמת משקולות, להתכופף. יש צורך לנקוט בעמדה הנכונה במהלך מנוחה ושינה (ראש המיטה מורם ב-15-20 ס"מ, בזווית של 30-50 מעלות). מומלץ לנרמל את משקל הגוף, לאכול באופן חלקי (הארוחה האחרונה - 3 שעות לפני השינה). אלכוהול ומזונות חריפים אינם נכללים בתזונה. הקצה סופחים ותרופות בסיסיות שיש להם השפעה מגנה על הקרום הרירי. חומרים אלה כוללים את Venter, הניתן דרך הפה במינון של 1 גרם (רצוי בצורת תרחיף) 30-40 דקות לפני הארוחות 3 פעמים ביום ובפעם הרביעית על בטן ריקה לפני השינה. מהלך הטיפול הוא 4-8 שבועות. Almagel, phosphalugel, maalox, gastal יש השפעה דומה. תרופות אלו משמשות בתקופת מערכת העיכול (10/1-2 שעות לאחר הארוחות ובלילה) עד להפוגה מוחלטת. Phosphalugel ו-Maalox נקבעים 2-1 מנות 2-2 פעמים ביום, גסטאל - 3-2 טבליות ביום. סודה תה, תערובת של Bourget, חימר לבן עקב יעילות לא מספקת לא מומלץ להשתמש. עוטף ופעולה עפיצה יש ביסמוט חנקתי 3 גרם 1-3 פעמים ביום. נצפתה פעילות אנטי-ריפלוקס גבוהה של נוגד חומצה חדש, טופלקן. למים מינרליים - "בורג'ומי", "אסנטוקי מס' 4", "ג'רמוק", "סמירנובסקאיה" יש אפקט בסיסי. כדי להפחית הפרשת קיבה חומצית, חוסמי H נקבעים.2קולטני היסטמין (סימטידין, רניטידין, פמוטידין), מעכבי Ka-K-ATPase (אומפרזול), חוסם סלקטיבי של קולטנים M-כולינרגיים של תאים פריאטליים, בוסקופן האנלוגי שלו. Cimetidine רשום 400 מ"ג 2 פעמים ביום, ranitidine - 300 מ"ג ופמוטידין - 40 מ"ג פעם אחת בערב לאחר ארוחת הערב. אומפרזול מומלץ לצורות עמידות של ריפלוקס ושט שחיקתי וכיבית. זה נקבע במינון של 30-40 מ"ג ליום למשך 3-4 שבועות. כדי לנרמל הפרעות פינוי מוטורי במחלת ריפלוקס, נקבעים metoclopramide (cerucal, raglan, perinorm, biomral), prepulsid (sizepride, motilium, domperidone, coordinax). Metoclopramide והאנלוגים מהדור השני שלו מגבירים את הטון של סוגר הוושט התחתון, מפחיתים את הלחץ תוך קיבה ומאיצים את הפינוי מהקיבה. הקצה metoclopramide 2 טבליה 1-3 פעמים ביום לפני הארוחות או 4 מ"ל לשריר 2 פעמים ביום. התרופה בדרך כלל נסבלת היטב. בעת השימוש בו, יובש בפה, נמנום, טינטון אפשרי, אשר פוחתים לאחר אכילה. Sizepride הוא סוכן פרוקינטי חדשני במערכת העיכול. זה מגביר את הטונוס של סוגר הוושט התחתון, משפר את פינוי הוושט, משפר את תפקוד הפינוי המוטורי של מערכת העיכול, ומדכא ריפלוקס פתולוגי (גסטרו-ושט ותריסריון). התרופה, בניגוד למטוקלופרמיד, אינה חוסמת את קולטני הדונמין, אינה מעוררת ישירה של קולטנים אנטיכולינרגיים, ונטולת תופעות לוואי הגלומות ב-cerucal ובאנלוגים שלה. זה נקבע דרך הפה ב-5 או 10 מ"ג 2-3 פעמים ביום. מהלך הטיפול נמשך בין 2-3 שבועות ל-2-3 חודשים. Cesapride עם reflux esophagitis יכול לשמש כמונותרפיה. תחזית ומניעה. התחזית לחיים ולעבודה חיובית. במקרים מסובכים, הפרוגנוזה נקבעת על פי הזמנים ואיכות הטיפול הרפואי. לחולים במחלה קשה מוקצית קבוצת מוגבלות. חולים עם רפלוקס ושט כרוני צריכים להיות תחת פיקוח של גסטרואנטרולוג. מחקרים אנדוסקופיים ומורפולוגיים מצוינים לפחות 2 פעמים בשנה עקב אפשרות של ממאירות. 3. כיב פפטי של הוושט כיב פפטי של הוושט הוא מחלה חריפה או כרונית המאופיינת בכיב של הרירית של הוושט המרוחק בהשפעת מיץ קיבה פעיל. אטיולוגיה ופתוגנזה. כיבים פפטיים כרוניים של הוושט הם סיבוכים של ריפלוקס ושט ובקע היאטלי. התרחשותם מתאפשרת על ידי ושט פנימי קצר, מטפלזיה מוקדית של הרירית, הטרוטופיה של רירית הקיבה לוושט, מחלת ריפלוקס עם אי ספיקת לב, מחלות המלוות בהקאות תכופות (תסמונת פוסט וגוטומיה, תסמונת לולאה כרונית). כיבים חריפים של הוושט אפשריים עם יובש פתולוגי של רירית הוושט (קסרוזיס), אלרגיות לתרופות, שימוש ב-NSAIDs, זיהומים פטרייתיים, זיהומים ויראליים, כוויות בעור ומחלות של מערכת העצבים המרכזית. כיבים אלו נחשבים לתסמינים. תמונה קלינית. לחלק מהחולים יש נגע כיבי משולב של הקרום הרירי של הוושט ואזור הקיבה התריסריון. תסמינים של כיב פפטי בוושט דומים לתמונה הקלינית של דלקת בוושט פפטית: צרבת מתמשכת, החמרה לאחר אכילה, בעת כיפוף הגוף, בשכיבה, מתרחשים רגורגיטציה, כאבים בבליעה ופגיעה במעבר של מזון מוצק. סיבוכים אופייניים לכיבים בוושט: ניקוב, דימום, חדירה, היצרות. הדימום מתבטא בהמטמזיס, מלנה, אנמיה היפוכרומית וירידה בפעילות הלב. ניקוב של הוושט מאובחן לעיתים רחוקות ביותר. לא ניתן להבחין בין התסמינים הקליניים של ניקוב מהסימפטומים של פגיעה מכנית חדה חדירת ולא חודרת על ידי גופים זרים. כ-14% מהכיבים בוושט חודרים לתוך הרקמות שמסביב. אבחון ואבחון מבדל. קשה מאוד לחשוד בכיב פפטי על סמך תסמינים קליניים. האבחנה מאומתת במהלך מחקרים מכשירים ומעבדתיים. האינפורמטיבי ביותר הוא בדיקת רנטגן ובדיקה אנדוסקופית. מבחינה רדיולוגית, הכיב מופיע כגומחה בוושט העל-לב עם בצקת פריפוקלית קלה של הקרום הרירי. הוושט באזור הכיב מכווץ באופן ספסטי ומעליו מתגלה התרחבות סופרסטנוטית קלה. הכיב מלווה בסימנים של היפרקינזיה ורפלוקס ושט, ותסמינים של בקע היאטלי שכיחים מאוד. לפעמים הכיב דומה לדיברטיקולום אפיפרני קטן, אך לאחרון אין מהלך קליני אופייני ואינו משולב עם אי ספיקה לבבית, בקע או דלקת בוושט. קשה יותר להבחין בין כיב פפטי של הוושט לבין סרטן אנדופיטי כיבי, המלווה בנוקשות של הדפנות והקלה של הקרום הרירי, ופיר א-סימטרי, בסימנים רדיולוגיים. המידע המהימן ביותר באימות כיב פפטי של הוושט מסופק על ידי אנדוסקופיה וביופסיה מרובה מקצוות הכיב. בעת התקדמות האנדוסקופ לכיב הפפטי, מתגלים סימנים של דלקת בוושט בשלב I-IV, חוסר תפקוד מוטורי של הוושט, בצקת פריפוקלית והיפרמיה של הקרום הרירי. כיב חריף הוא בדרך כלל עגול או סגלגל, עם קצוות תלולים, מכוסה בציפוי לבנבן או ירוק. לכיב כרוני יש תחתית שטוחה עם דפנות צפופות ולא אחידות, קצוות עדינים, משקעים מוגלתיים-סיביים, מוקדי גרגירים ושכבות ציכיות. כדי להוציא ממאירות, נלקחות 4-6 ביופסיות מקצוות הכיב. בדיקה אנדוסקופית מגלה פגמים פפטי בודדים, מוארכים לאורך ציר הוושט. אורכם משתנה בין 1-10 ס"מ, אך לעתים קרובות יותר אינו עולה על 1 ס"מ. הכיב הוא לעתים קרובות רדוד, החלק התחתון שלו מכוסה בציפוי לבנבן. היפרמיה, בצקת ברירית ושחיקות בודדות משקפות לרוב תגובה דלקתית פריפוקלית מתונה. לאחר ריפוי של כיב פפטי, נותרות בוושט צלקת ליניארית או כוכבית גסה או עיוות דמוי דיברטיקולום מחוספס של הקיר והיצרות של לומן. יש צורך להבדיל כיבים פפטי של הוושט עם כיבים בעלי אופי ספציפי (עם שחפת, עגבת). במצבים אלו, בדיקות סרולוגיות ספציפיות, תוצאות מחקרים היסטולוגיים ובקטריולוגיים עוזרות משמעותית. השילוב של הפתולוגיה של הוושט עם נזק לריאות ולאיברים אחרים מחייב בדיקה מכוונת של המטופל ביחס לתהליך ספציפי. טיפול. הטיפול כולל דיאטה: מומלץ מזון עדין מבחינה מכנית וכימית, הנלקח במנות קטנות 5-6 פעמים ביום. כדי למנוע ריפלוקס של תוכן מהקיבה אל הוושט, מיקום המטופל במיטה צריך להיות עם ראש המיטה מוגבה. תרופות נלקחות בשכיבה. מונותרפיה נקבעת עם תרופה מאחת מהקבוצות הפרמקולוגיות הבאות: נוגדות הפרשה, כולל נוגדי חומצה וסופחים, ממריצים של פונקציית הפינוי המוטורי של הקיבה (פרוקינטיקה), תרופות - סימולטורים של ריר. הטיפול מתבצע במשך זמן רב - 1,5-3 חודשים. אינדיקציות לטיפול כירורגי - חוסר ריפוי תוך 6-9 חודשים, מהלך מסובך (ניקוב, חדירה, היצרות, דימום). תחזית ומניעה. מהלך המחלה הוא הישנות. התחזית לחיים ולעבודה חיובית. מומלצת בדיקה תקופתית (1-2 פעמים בשנה) על בסיס חוץ על ידי גסטרואנטרולוג באמצעות אנדוסקופיה וביופסיה. מתבצעת מניעה עונתית (אביב - סתיו) של ריפלוקס ושט. הרצאה מס' 10. מחלות במערכת העיכול. מחלות של הקיבה. דלקת קיבה כרונית דלקת קיבה כרונית היא מחלה המתאפיינת קלינית בדיספפסיה בקיבה, ומבחינה מורפולוגית - בשינויים דלקתיים וניונים ברירית הקיבה, פגיעה בתהליכי חידוש התאים, ועלייה במספר תאי הפלזמה והלימפוציטים בקרום הרירי עצמו. אטיולוגיה ופתוגנזה. בשלב הנוכחי של התפתחות הגסטרואנטרולוגיה, הוכח כי הופעת דלקת קיבה כרונית מקלה על ידי התרחבות מיקרוביאלית של הליקובקטר פילורי (HP), הגורמת לדלקת קיבה אנטראלית ב-95% מהמקרים ולדלקת פנגאסטריטיס ב-56% מהמקרים. בתורו, הגורמים האטיולוגיים כביכול להתרחשות של דלקת קיבה כרונית ניתן לייחס במידה רבה של ודאות לגורמי סיכון (תזונה לא סדירה, עישון, צריכת אלכוהול, הפרשת יתר של חומצה הידרוכלורית ופפסין). התפקיד המוביל בהתפתחות המחלה שייך גם למנגנונים אוטואימוניים, המלווים בהצטברות נוגדנים לתאי הקודקוד של רירית הקיבה, תורשה מחמירה וכן שימוש בתרופות בעלות השפעה מזיקה על רירית הקיבה. מיון. בשנת 1990, בקונגרס הבינלאומי התשיעי של גסטרואנטרולוגים באוסטרליה, אומצה שיטתיות חדשה של דלקת קיבה כרונית, המכונה מערכת סידני. בסיסים היסטולוגיים של סיווג. 1) אטיולוגיה: דלקת קיבה כרונית הקשורה ל-HP, דלקת קיבה אוטואימונית, אידיופטית, חריפה הנגרמת על ידי תרופות. 2) טופוגרפיה: אנטראל, פונדיק, פנגסטריטיס. 3) מורפולוגיה: צורות חריפות, כרוניות, מיוחדות. בסיס אנדוסקופי לסיווג: 1) גסטריטיס של האנטרום של הקיבה; 2) גסטריטיס של גוף הקיבה; 3) פנגסטריטיס; 4) שינויים ברירית הקיבה: בצקת, אריתמה, פגיעות רירית, אקסודאט, שחיקות שטוחות, שחיקות מוגברות, היפרפלזיה של קפלים, ניוון קפלים, נראות של תבנית כלי הדם, שטפי דם על-רירית. תמונה קלינית. דלקת קיבה כרונית היא אחת המחלות השכיחות במרפאה הפנימית. שכיחותה בקרב תושבי העולם נעה בין 28 ל-75%. דלקת קיבה כרונית מתבטאת לעתים קרובות יותר בתסמינים של דיספפסיה בקיבה וכאבים באזור האפיגסטרי. לעתים רחוקות, זה אסימפטומטי. הכאב הוא בדרך כלל מקומי באזור האפיגסטרי. קיים קשר ברור בין התרחשותו עם צריכת מזון לבין לוקליזציה של התהליך הדלקתי בקיבה. בחולים עם דלקת קיבה של החלק התת-קרדיאלי והלבבי של הקיבה, כאב באזור האפיגסטרי מתרחש 10-15 דקות לאחר הארוחה, עם פתולוגיה של גוף הקיבה - 40-50 דקות לאחר הארוחה. "מאוחר", "רעב", כאבים אופייניים לדלקת קיבה של קטע הפלט של הקיבה, או תריסריון. כאב "שני גלים" - לאחר אכילה ועל בטן ריקה - נצפה עם דלקת קיבה של תת הלב והאנטרום. בתהליך מפוזר, הכאב ממוקם באזור האפיגסטרי, מתרחש לאחר אכילה והוא בעל אופי לוחץ. הם אומרים על המהלך האסימפטומטי של דלקת הקיבה כאשר לא ניתן לקבוע את הקשר בין כאב באזור האפיגסטרי לבין הנגע, המתרחש כאשר הוא אנדוגני במקורו (דלקת הקיבה הופכת משנית לפתולוגיה של איברים ומערכות אחרות). מקום חשוב לא פחות בתמונה הקלינית של דלקת קיבה כרונית הוא תסמונת דיספפטית: בחילות, גיהוקים (חמוצים, מרירים, רקובים), צרבת, עצירות או שלשולים, צואה לא יציבה. עם דלקת קיבה אנטרלית מבודדת, תלונות על צרבת ועצירות, הנובעות מהפרשת יתר של חומצה הידרוכלורית ופפסין, הופכות לחשיבות עליונה. עם pangastritis עם סימנים של ניוון חמור, בחילה, גיהוקים "רקובים", צואה לא יציבה או שלשול שולטים, אשר אופייני להפרשת תת-הפרשה של חומצה הידרוכלורית ופפסין. בחילה מתמשכת אופיינית לדלקת קיבה משנית בדלקת לבלב כרונית, דלקת כיס המרה כרונית, המתרחשת עם דיסקינזיה היפו-מוטורית של כיס המרה. אבחון. דלקת קיבה כרונית נמשכת זמן רב, עם עלייה בתסמינים לאורך זמן. החמרות מעוררות על ידי הפרעות תזונתיות. התמונה הפיזית של דלקת קיבה כרונית היא גרועה למדי. ב-80-90% מהחולים במהלך החמרה של המחלה, מחקר אובייקטיבי קובע רק כאב מקומי באזור האפיגסטרי. כאשר דלקת קיבה כרונית משולבת עם תריסריון, דלקת כיס המרה או דלקת הלבלב, ניתן לקבוע לוקליזציה של כאב שאינו אופייני לגסטריטיס, אך אופייני לפתולוגיה של איבר אחר. בדיקות דם ושתן כלליות, פרמטרים ביוכימיים של דם בחולים עם גסטריטיס כרונית אינם שונים מהפרמטרים המקבילים אצל אנשים בריאים. במחקר קופרולוגי, אין שינויים בניתוחים או שיכולים להיות סימנים להפרעת עיכול. כאשר בוחנים את תכולת הפרשת החומצה בקיבה על ידי pH-metry, מציינים גם סימנים של הפרשת יתר של חומצה וגם ירידה בייצור חומצה. אינדיקטורים להיווצרות פפסין בדלקת קיבה כרונית מתמשכים יותר ויורדים על רקע חומציות מתמשכת בנזק לאיברים מפושט. בדיקת רנטגן נוטה יותר לשלול מחלות אחרות של הקיבה (אולקוס, סרטן), לעזור באבחון של מחלת Menetrier מאשר לאשר את האבחנה של דלקת קיבה כרונית. בשל מיעוט הביטויים הקליניים של המחלה, כמו גם חוסר הספציפיות של בדיקות מעבדה, האבחנה של דלקת קיבה כרונית מבוססת על תוצאות מחקרים אנדוסקופיים ומורפולוגיים. אנדוסקופיה מגלה שינויים בחומרת רירית הקיבה בחומרה משתנה: בצקת, אריתמה, פגיעות של הקרום הרירי, אקסודאט, שחיקות שטוחות, שחיקות מורמות, היפרפלזיה או ניוון של הקפלים, נראות של תבנית כלי הדם, שטפי דם תת-ריריים. הם מדברים על דלקת קיבה כרונית עם עלייה במספר תאי הפלזמה והלימפוציטים בקרום עצמו של הקרום הרירי (בניגוד לדלקת קיבה חריפה, כאשר מופיעים לויקוציטים פולימורפונוקלאריים). בהקשר לאמור לעיל, ייתכן שהזיהוי המורפולוגי של דלקת בגסטריטיס לא יעלה בקנה אחד עם פרשנות הנתונים של הרופא. פעילות השינויים הדלקתיים ברירית הקיבה מוערכת מורפולוגית ומורפומטרית לפי מידת חדירת הלויקוציטים של lamina propria או אפיתל. אסור לנו לאבד את העובדה שדלקת קיבה אוטואימונית אינה פעילה. שינויים מורפולוגיים (חלשים, בינוניים וחמורים) - דלקת, פעילות, ניוון, מטפלזיה - ומידת הזיהום של HP נכמתים. ביטויים קליניים האופייניים לגסטריטיס נצפים גם במחלות אחרות של מערכת העיכול, ולכן, בתהליך האבחון, יש צורך באולטרסאונד של חלל הבטן, בדיקה אנדוסקופית ומורפולוגית יסודית של איברי העיכול. אבחון דיפרנציאלי. הקשה ביותר היא האבחנה המבדלת של דלקת קיבה עם מחלות תפקודיות של הקיבה, כיב פפטי של הקיבה והתריסריון, דלקת כיס המרה כרונית ודלקת הלבלב וסרטן הקיבה. מחלות פונקציונליות של הקיבה, בדומה לדלקת קיבה כרונית, יכולות להתרחש באופן סמוי או להיות מלוות בכאב ובתסמינים דיספפטיים. הם מאופיינים על ידי משך זמן קצר, נוכחות של תסמינים נוירוטיים כלליים השוררים בתמונה הקלינית של המחלה (כגון חולשה, עייפות, עצבנות, כאבי ראש, מצב רוח לא יציב, הזעה). עם הפרעות בתפקוד הקיבה, הכאב אינו תלוי באיכות המזון, או שהוא מתרחש לאחר שימוש במוצר מוגדר בהחלט. לעתים קרובות יש תסמונת של חומציות (צרבת, התפרצות חמוצה, טעם חמוץ בפה), שבניגוד לדלקת קיבה עם תפקוד הפרשה מוגבר, לא עולה לאחר אכילה, אלא בהתרגשות, הפסקות ארוכות באכילה. הקאות בפתולוגיות תפקודיות של הקיבה מתפתחות על פי מנגנון של רפלקס מותנה, מביאות להקלה על המטופל ואינן מביאות להידרדרות משמעותית במצב הכללי. בדלקת קיבה כרונית, היא מתרחשת בדרך כלל במהלך החמרה ואינה מביאה להקלה למטופל. סימפטום תכוף של תפקוד לקוי של הקיבה הוא התפרצות רועשת של אוויר. בדלקת קיבה כרונית, היא קשורה לפגיעה בעיכול המזון או בתנועתיות הקיבה ועלולה להיות חומצית אם ההפרשה נשמרת, או עם ריח של ביצים רקובות אם היא מופחתת. במחקר של הפרשת קיבה בגסטריטיס, ערכים תקינים של הפרשה מתגלים בתחילת המחלה ובעתיד נטייה לירידה בהפרשת מיץ קיבה. עם מחלות פונקציונליות של הקיבה, heterochilia הוא ציין לעתים קרובות. בדיקת רנטגן של הקיבה מאפשרת לאשר צורות כאלה של דלקת קיבה כמו נוקשה, אנגראלית, היפרפלסטית ענקית, פוליפוזיס, ובמקרה של הפרות של פונקציית הפינוי המוטורי של הקיבה (גסטרופטוזיס, תת לחץ דם) מעידה על האופי התפקודי של הקיבה. המחלה. שיטת המחקר היקרה ביותר לאבחנה מבדלת של דלקת קיבה כרונית ומחלות תפקודיות של הקיבה היא גסטרוסקופיה, המאפשרת, במקרים שנויים במחלוקת, לברר שינויים ברירית הקיבה האופיינית לדלקת קיבה או מחלות תפקודיות של הקיבה. האבחנה המבדלת של דלקת קיבה כרונית עם כיב פפטי מתוארת בהרצאה הבאה. לסרטן הקיבה יש תמונה דומה מאוד עם גסטריטיס עם תפקוד הפרשה מופחת. אבחון מוקדם של סרטן הקיבה על בסיס סימנים קליניים קשה, במיוחד בחולים הסובלים מדלקת קיבה לאורך זמן. חשיבות רבה לאבחון הסרטן הם הופעת כאב מתמשך, תלוי מעט בצריכת מזון, חולשה כללית ועייפות חסרת מוטיבציה, סטייה בתיאבון וכן ירידה מתקדמת במשקל הגוף של החולה. איתור גידול במישוש מתייחס לשלבים המאוחרים של תהליך הסרטן. תסמינים כמו שינוי במצבו של החולה, ירידה מהירה בחומציות מיץ הקיבה, "מחסור" בחומצה הידרוכלורית, הופעת תאים לא טיפוסיים במיץ הקיבה, תגובה חיובית לדם סמוי בצואה צריכים לגרום לרופא לחשוד בסרטן קיבה. חשיבות מכרעת באבחנה המבדלת הם מחקרים רנטגן וגסטרוסקופיים עם ביופסיה ממוקדת של רירית הקיבה. בחולים עם דלקת קיבה כרונית עם תפקוד הפרשה מופחת, בדיקת רנטגן מגלה ניוון של הממברנה הרירית שלו, אשר מאושרת גם על ידי גסטרוסקופיה. עם ביופסיה ממוקדת במקרים כאלה, מתגלים שינויים מבניים וניוון של הקרום הרירי. עבור סרטן קיבה, בדיקת רנטגן מאופיינת בנוכחות פגם מילוי, היעדר קפלי רירית או שינוי באופי שלהם והיעדר פריסטלטיקה באזורים מסוימים. אנדוסקופיה של הקיבה מאפשרת לזהות גידול בשלב המוקדם ביותר של התפתחותו, כאשר הגידול נמצא עדיין בתוך רירית הקיבה, וטיפול כירורגי מוביל להחלמה ביותר מ-90% מהמקרים. דלקת כיס כיס כרונית. בדלקת כיס מרה כרונית, הכאב ממוקם בהיפוכונדריום הימני והוא עמום באופיו. עם cholecystitis calculous, הכאב הוא חריף, colicky, מקרין לאזור subscapular הימני. הופעת הכאב קשורה לאכילת מזון שומני או נהיגה מטלטלת. בדלקת קיבה כרונית, הכאב באפיגסטריום מפוזר, עמום, אין הקרנה, הוא מתרחש מיד לאחר אכילת מזון יבש או תוך הפרה של הדיאטה. עם גסטריטיס ודלקת כיס המרה, הכאב מלווה בתסמינים דיספפטיים, אך תחושת כבדות באפיגסטריום, מלאות, גיהוק מזון או אוויר, טעם מתכתי בפה אופייניים יותר לדלקת הקיבה. הקאות בדלקת קיבה כרונית הן נדירות. באופן אובייקטיבי, בדלקת כיס המרה הכרונית, במיוחד חושנית, הם מזהים מתח בדופן הבטן הקדמית, היפראסתזיה של העור בהיפוכונדריום הימני, שאינה אופיינית לדלקת קיבה כרונית. במישוש של הבטן במקרה של cholecystitis כרונית, כאב הוא ציין לוקליזציה של כיס המרה. דלקת קיבה כרונית מאופיינת בכאב מפוזר. בחולים עם דלקת כיס מרה כרונית, בדיקת מרה מגלה עלייה בכמות הריר והלוקוציטים. דלקת קיבה כרונית מאופיינת בתמונה תקינה של מרה על רקע שינויים בהפרשה ובחומציות של מיץ הקיבה, כמו גם פונקציות אחרות של הקיבה (ספיגה, מוטורי). בדיקת רנטגן של כיס המרה בחולים עם דלקת כיס מרה כרונית מגלה שינוי בתפקוד הפינוי שלו, כמו גם אבנים. דלקת לבלב כרונית. בדלקת לבלב כרונית, הכאב ממוקם בחצי השמאלי של הבטן, מקרין לאזור התת-סקפולארי השמאלי, לגב התחתון ולאזור שמסביב. התרחשות של כאב קשורה לצריכה של מזון בשפע, לעתים קרובות שומני, ואלכוהול. אם דלקת קיבה כרונית מתאפיינת במהלך ארוך ומונוטוני של המחלה, אז בדלקת לבלב כרונית היא מתרחשת בהדרגה. בדיקה אובייקטיבית במקרה של דלקת לבלב כרונית מגלה יתר אסתזיה של העור בהיפוכונדריום השמאלי, כאב מתאים טופוגרפית למיקום הלבלב. במחקר מעבדתי של מיץ הלבלב בדלקת לבלב כרונית, נמצא שינוי מתמשך בבסיסיות ובאנזימים: רמת הדיאסטז בדם ובשתן עלולה להשתנות, מה שלא קורה בדלקת קיבה כרונית. מבחינה רדיולוגית, דלקת לבלב כרונית מאופיינת בהיפוך מוגבר של טבעת התריסריון, עלייה חדה בפפילה הראשית שלה (תסמין של פרוסטברג), ולעיתים בנוכחות אזורי הסתיידות של הלבלב. יש לבצע גם אבחון תוך-נוזולוגי של צורות שונות של דלקת קיבה כרונית. לפיכך, המחלה הקשורה ל-HP ממשיכה מבחינה קלינית עם תסמינים של כיבים בתריסריון, ובמקרים מסוימים היא יכולה להתקדם באופן סמוי. בדיקה אנדוסקופית ומורפולוגית מגלה אנטרופילורודואודיטיס. שחיקות בגסטריטיס הליקובקטר פילורי ממוקמות בדרך כלל באזור של דלקת חמורה (אזור אנתרופילורי של הקיבה). דלקת קיבה כרונית אוטואימונית מאופיינת קלינית בתחושת כבדות באזור האפיגסטרי, טעם לוואי לא נעים בפה, גיהוקים רקובים ובחילות. בשל ייצור לא מספיק של חומצה הידרוכלורית, מופיע שלשול. ב-10% מהמקרים, על רקע דלקת קיבה אוטואימונית, מתגלים תסמינים B12- אנמיה מחסור: חולשה, חיוורון של העור והריריות, ציפורניים שבירות, בבדיקות דם - אנמיה מגלובלסטית היפרכרומית. צורות מיוחדות של המחלה כוללות גרנולומטיות, אאוזינופיליות, היפרטרופיות (מחלת Menetrier), דלקת קיבה לימפוציטית. דלקת קיבה גרנולומטית פועלת כצורה עצמאית של המחלה או לעתים קרובות יותר - אחד המרכיבים של פתולוגיה חמורה יותר (מחלת קרוהן, שחפת, סרקואידוזיס). האבחנה מאושרת תמיד על ידי תוצאות בדיקה היסטולוגית של דגימות ביופסיה של רירית הקיבה. דלקת קיבה אאוזינופילית היא נדירה ביותר ונגרמת על ידי דלקת כלי דם מערכתית. היסטוריה של תגובות אלרגיות היא חובה. בדיקה היסטולוגית מגלה חדירת אאוזינופילית של רירית הקיבה. גסטריטיס היפרטרופית (מחלת Menetrier) מתבטאת קלינית בכאב באזור האפיגסטרי ובחילות. חלק מהחולים עלולים לחוות ירידה במשקל עקב שלשול. במחקרים אנדוסקופיים, רדיולוגיים ומורפולוגיים, נמצאים קפלי רירית היפרטרופיים ענקיים, הדומים לפיתולי המוח. דלקת קיבה לימפוציטית היא אסימפטומטית קלינית; מבחינה מורפולוגית, צורה זו מאופיינת בחדירה בולטת של רירית הקיבה על ידי לימפוציטים. טיפול. חולים עם דלקת קיבה זקוקים לאמצעים רפואיים כלליים: תזונה מאוזנת קבועה, נורמליזציה של לוחות הזמנים של עבודה ומנוחה, יישור מצבי לחץ בחיי היומיום ובעבודה. טיפול תרופתי מצוין רק בנוכחות ביטויים קליניים של דלקת קיבה כרונית. חולים עם דלקת קיבה הקשורה ל-HP מטופלים בתוכנית כיב פפטי (ראה הרצאה הבאה). אנשים עם דלקת קיבה אוטואימונית זקוקים לתוספת ויטמין B12 (500 מק"ג פעם ביום תת עורית למשך 1 יום, ולאחר מכן חזרה על קורסי טיפול), חומצה פולית (30 מ"ג ליום), חומצה אסקורבית (עד 5 גרם ליום). במידת הצורך, מתבצע טיפול חלופי בתכשירי אנזימים (מזים-פורטה, פסטאל, אנזיסטל, קריאון, pancitrate, acidin-pepsin). תסמונת הכאב נעצרת בדרך כלל על ידי מינוי נוגדי חומצה (maalox, almagel, gastal) או חוסמי קולטן H-Histamine (ranitidine, famotidine) במינונים טיפוליים בינוניים. עם צורות מיוחדות של גסטריטיס, יש צורך בטיפול במחלה הבסיסית. תחזית ומניעה. התחזית לחיים ולעבודה חיובית. חולים עם דלקת קיבה כרונית צריכים להירשם אצל גסטרואנטרולוג. הם נבדקים קלינית ואנדוסקופית עם ביופסיה לפחות פעם בשנה כדי לא לכלול שינוי גידול. המסוכנים ביותר במונחים של ניוון סרטני הם היפרטרופיים, גסטריטיס אטרופית מפוזרת עם דיספלזיה אפיתל. בצורות שחיקות של המחלה המסובכות על ידי דימום, כמו גם בצורה המנותקת של מחלת Menetrier, הפרוגנוזה נקבעת על פי הזמן וההתאמת הטיפול הניתוחי. מניעת דלקת קיבה מצטמצמת לתזונה רציונלית, עמידה במשטר העבודה והמנוחה, הגבלת צריכת NSAIDs. הרצאה מס' 11. מחלות במערכת העיכול. מחלות של הקיבה. כיב פפטי כיב פפטי (כיב פפטי) הוא מחלה כרונית חוזרת, המתבטאת קלינית בפתולוגיה תפקודית של אזור הקיבה התריסריון, ומבחינה מורפולוגית - על ידי הפרה של שלמות השכבות הריריות והתת-ריריות שלו, ולכן הכיב מרפא תמיד עם היווצרות של צלקת. אטיולוגיה. הגורם האטיולוגי העיקרי של מחלת כיב פפטי הוא ההתרחבות המיקרוביאלית של HP על פני אפיתל הקיבה. המשמעות של תוקפנות חיידקים באטיולוגיה של המחלה נחקרה מאז 1983, כאשר ג'יי וורן וב' מרשל דיווחו על גילוי של מספר רב של חיידקי S-spiral על פני האפיתל של האנטרום של הקיבה. הליקובקטריות מסוגלות להתקיים בסביבה חומצית עקב ייצור האנזים urease, אשר הופך אוריאה (מזרם הדם) לאמוניה ופחמן דו חמצני. תוצרי ההידרוליזה האנזימטית מנטרלים חומצה הידרוכלורית ויוצרים תנאים לשינוי ה-pH של הסביבה סביב כל תא חיידק, ובכך מספקים תנאים נוחים לפעילות חיונית של מיקרואורגניזמים. קולוניזציה מלאה של HP מתרחשת על פני תאי אפיתל קיבה, המלווה בנזק לאפיתל תחת פעולת פוספוליפאז. אלה האחרונים מספקים היווצרות לציטינים רעילים ופרוטאינזים ממרה, וגורמים להרס של קומפלקסים חלבונים וריר מגנים. על רקע "אלקליניזציה" של ממברנות תאי אפיתל עם אמוניה, פוטנציאל הממברנה של התאים משתנה, הדיפוזיה ההפוכה של יוני מימן מתגברת, מוות והשחתת האפיתל של רירית הקיבה. כל השינויים הללו מובילים לחדירה של HP לעומק רירית הקיבה. לא פחות חשוב בהתפתחות כיבים פפטי הם השפעות נוירו-פסיכיות, נטייה תורשתית, גורמים זיהומיים, טעויות מזון ונטילת תרופות מסוימות והרגלים רעים. לראשונה, התפיסה הנוירוגני של הופעת המחלה גובשה על ידי ברגמן, שטען כי הפרעות תורשתיות-חוקתיות של מערכת העצבים האוטונומית מובילות לעווית של השרירים וכלי הדם בדופן הקיבה, לאיסכמיה ולירידה. בהתנגדות הקרום הרירי להשפעות האגרסיביות של מיץ קיבה. תיאוריה זו פותחה עוד יותר על ידי K.N. Bykov ו-I.T. Kurtsin (1952). הם ביססו את התיאוריה הקורטיקו-ויסצרלית של אולצרוגנזה, המבוססת על נתונים על שינויים בפעילות עצבית גבוהה יותר כתוצאה מטראומה נוירו-פסיכית כרונית. בתוספת ומפורטת הדוקטרינה של הקשרים הביוכימיים וההורמונליים בוויסות הפרשת הקיבה, התנועתיות והטרופיזם, תיאוריית כיב זו שוב זכתה לתומכים רבים בשנים האחרונות. גורמים תורשתיים פופולריים בקרב חוקרים: האינרציה של התהליכים העצבים העיקריים, תכונות ספציפיות לקבוצה של דם, תכונות אימונולוגיות וביוכימיות, תסמונת נטל תורשתית. בהתרחשות של כיב פפטי, הפרעות תזונתיות היו בעלות חשיבות רבה. עם זאת, מחקרים קליניים וניסויים שנערכו בשני העשורים האחרונים ברוב המקרים לא חשפו את ההשפעה המזיקה של מוצרי מזון על רירית הקיבה התריסריון. השכיחות של מחלת כיב פפטי בקרב קבוצות משמעותיות של אנשים עם הרגלי תזונה שונים מעידה גם על החשיבות המובילה של גורמים תזונתיים. הפרעות בקצב ובסדירות התזונה, הפסקות ארוכות בין הארוחות, אכילה לא בזמן חיוניים להופעת כיבים פפטי. חוקרים הביעו דעות סותרות יחסית לגבי תפקידו של אלכוהול בכיב. ידוע שאלכוהול גורם לשינויים אטרופיים ברירית הקיבה. תצפיות אלו עומדות בסתירה לתפיסה הכללית של כיב. עם זאת, השימוש התכוף באלכוהול מלווה בהפרות של הדיאטה, שינויים איכותיים בהרכב המזון, אשר בסופו של דבר עלולים לגרום לכיב פפטי של הקיבה והתריסריון. תפקידן של ההשפעות הרפואיות באולצרוגנזה נחקר באופן פעיל. תוצאות מחקרים שפורסמו בספרות והנתונים שלנו מצביעים על כך שלתרופות נוגדות דלקת לא סטרואידיות ולהורמונים גלוקוקורטיקואידים יש את התכונות הכיביות הבולטות ביותר. פתוגנזה. הפתוגנזה של מחלת כיב פפטי עדיין לא מובנת במלואה. כאשר בוחנים את התהליכים של כיב, יש צורך להדגיש מספר הנחות: 1) מאופיין בעונתיות של החמרות של כיב פפטי; 2) יש לוקליזציה דומיננטית של כיבים פפטי באזור האנטרופילורודואודנל; 3) צוינה נוכחות של חומצה הידרוכלורית ופפסין במיץ קיבה; 4) בולטת תדירות גבוהה (עד 70%) של ריפוי ספונטני של כיבי קיבה ותריסריון; 5) קיימת דלקת קיבה אנטראלית כרונית הקשורה ל-HP; 6) החלק האנתרופילורי של הקיבה והחלק הראשוני של התריסריון הם ה"היפותלמוס" של מערכת העיכול; 7) קיימת נטייה תורשתית להתרחשות של כיבים פפטי; 8) התרחשות של כיב, הישנותו והפוגה אפשריים בנוכחות כל הגורמים לעיל. לפיכך, הרעיון המאוחד של כיב הוא כדלקמן. בחולה עם נטייה תורשתית לכיב פפטי בנוכחות דלקת קיבה חיידקית כרונית בתקופת סתיו או אביב, מציינים רק היפרפלזיה ותפקוד יתר של תאים אנדוקריניים המפרישים גסטרין, היסטמין, מלטונין וסרוטונין. ההורמונים העיקריים והאמינים הביוגנים המיוצרים על ידי אזור האנתרופילורו-דואודנל מעורבים הן בגירוי הפרשת הקיבה והן בשינוי הטרופיזם ותפוצת התאים, בעיקר באזור זה. על רקע דלקת קיבה חיידקית ותריסריון פעילה, נוצרים תנאים נוחים להיווצרות כיב. עם היווצרות של פגם פפטי, הפעילות התפקודית של תאים אנדוקריניים פוחתת. זה מוביל לירידה בתוקפנות חומצה-פפטית, שיפור בטרופיזם של רקמות באזור האנתרופילורו-דואודנל, ויצירת תנאים לריפוי כיבי קיבה ותריסריון, גם על רקע ההתרחבות המיקרוביאלית המתמשכת של HP. בתקופה החריפה של כיב פפטי, מציינת היפרפלזיה של תאים המייצרים α-אנדורפין, שהם מגיני ציטו-פרוטקטורים אוניברסליים. הם פועלים כמנגנוני ההגנה העיקריים בכיב פפטי ומספקים את תהליך ההגבלה העצמית של הכיב וריפויו, הן ישירות והן על ידי גירוי מערכת החיסון. במקביל, נוגדנים נגד HP, המסונתזים בתת-רירית הקיבה והתריסריון, נקשרים ביעילות לתאי חיידקים ומנטרלים רעלנים של HP ותורמים למותם. כל האמור לעיל תורם ליצירת איזון בין מה שנקרא גורמי תוקפנות וגורמי הגנה לבין ריפוי של פגם פפטי באזור הקיבה התריסריון. מיון. סיווג (Panfilov Yu. A., Osadchuk M. A., 1991) לוקליזציה של הפגם הפפטי: 1) כיב קיבה (חתכים תת-לביים ולבביים, חלק פילורי ותעלה פילורית, עקמומיות קטנה יותר ויותר); 2) כיב בתריסריון (חלק נורה ופוסטבולברי); 3) כיבים בקיבה ובתריסריון. מהלך של כיב פפטי. 1. קל. החמרה של הכיב היא לא יותר מפעם אחת ב-1-1 שנים, הריפוי של הפגם הפפטי מסתיים בשבוע ה-3-5 מתחילת הטיפול, חומרת הכאב והתסמונות הדיספפטיות היא בינונית. 2. מתון. הישנות לפחות 2 פעמים בשנה, אפיתל כיב - תוך 7-12 שבועות, חומרת הכאב ותסמונות דיספפטיות. 3. כבד. תקופות ההפוגה אינן עולות על 3-4 חודשים. בנוסף לכאבים עזים, ישנם סיבוכים. שלבי המחלה: 1) החמרה של הישנות כיב או הפרעות תפקודיות של מערכת הקיבה התריסריון; 2) הפוגה מלאה (בהיבטים קליניים, רדיולוגיים, אנדוסקופיים ותפקודיים); 3) לא שלם (עם שימור של הפרעות תפקודיות או מבניות באזור הקיבה התריסריון). מצב הקרום הרירי של הקיבה והתריסריון: 1) דלקת קיבה כרונית; 2) תריסריון כרוני. מצב תפקודי של מערכת הקיבה התריסריון הפרשה: תקינה, מוגברת, מופחתת. תנועתיות: רגילה, מואצת, איטית; פינוי: תקין, מואץ, מושהה, תריסריון. סיבוכים: דימום, ניקוב, חדירה, פריגסטריטיס, periduodenitis, עיוות ציטרי של הקיבה והתריסריון. תמונה קלינית. התמונה הקלינית של כיב פפטי היא פולימורפית. התסמינים תלויים במינו ובגילו של המטופל, בזמן השנה, במיקום ובגודל הכיב, במאפיינים האישיים והחברתיים של המטופל ובאיכויותיו המקצועיות. המרפאה נקבעת על ידי שילוב של תסמינים: המהלך הכרוני של המחלה מרגע הופעתה, נוכחות סימני החמרה והפוגה של המחלה, ריפוי הפגם ברירית הקיבה והתריסריון עם היווצרות של צַלֶקֶת. כיב פפטי מיוצג על ידי שני וריאנטים קליניים ומורפולוגיים: כיב קיבה וכיב תריסריון. באופן מסורתי, כאב ותסמונות דיספפטיות נבדלות. הסימן הקליני המוביל הוא כאבים בבטן העליונה. מטבעה של תסמונת הכאב, כמעט בלתי אפשרי להבחין בין דלקת קיבה חיידקית כרונית לבין כיב פפטי. כאבים באזור האפיגסטרי, על קיבה ריקה, בעיקר באביב ובסתיו, שכיחים באותה מידה גם בכיב פפטי וגם בדלקת קיבה חיידקית כרונית. הקלה בתסמונת הכאב עם מזון וסותרי חומצה תרופתיים מושגת הן בדלקת קיבה חיידקית כרונית והן בכיב פפטי. ייחודי לכיב התריסריון הוא רק נוכחות של כאב באזור האפיגסטרי בלילה. הקאות עם כיב פפטי הן נדירות. בחילות נפוצות הרבה יותר עם כיבי קיבה וכיבים בתריסריון. עצירות מלווה כיב כרוני בתריסריון. תסמינים של מחלת כיב פפטי נקבעים על פי מספר הפגמים הכיביים והלוקליזציה שלהם. כיבי קיבה מרובים שכיחים פי 3 בגברים. התמונה הקלינית במקרה זה תלויה בלוקליזציה של פגמים פפטי. עם כיבים בגוף הקיבה, כאב עמום באפיגסטריום ללא הקרנה, המתרחש 20-30 דקות לאחר האכילה, ובחילות. עם כיבים של האזור התת-קרדיאלי, כאבים עמומים תחת תהליך ה-xiphoid, המקרינים לחצי השמאלי של החזה, אופייניים. כיבי קיבה וכיבי תריסריון משולבים הם שילוב של כיב קיבה פעיל וכיב תריסריון נרפא. הם מאופיינים בשימור ארוך טווח של תסמונת הכאב, מהלך מתמשך של המחלה, הישנות תכופות של המחלה, הצטלקות איטית של הכיב וסיבוכים תכופים. כיבים חוץ-בולביים כוללים כיבים הממוקמים באזור הסוגר הבולבודואדינאלי ומרוחקת ממנו. לתמונה הקלינית שלהם יש מאפיינים משלה ויש הרבה מן המשותף עם כיבים בתריסריון. הם מתרחשים בעיקר בחולים בגילאי 40-60 שנים. כיבים פוסטבולבריים הם חמורים ונוטים להחמרות תכופות, מלווה בדימום מסיבי. כאב הממוקם ברביע העליון הימני של הבטן, מקרין לגב או מתחת לכתף ימין, מופיע ב-100% מהמקרים. עוצמת הכאב, חומרת הכאב, ששוככת רק לאחר נטילת משככי כאבים נרקוטיים, מביאה את החולים לנוירסטניה חמורה. עונתיות של החמרות בכיבים חוץ-בולבוסיים נרשמת בכמעט 90% מהחולים. בחולים רבים, דימום במערכת העיכול הופך לתסמין קרדינלי. כיבים בתעלת הפילורי מאופיינים בתסביך סימפטומים הנקרא תסמונת הפילורי: כאבים אפיגסטריים, בחילות, הקאות וירידה משמעותית במשקל. החמרת המחלה ארוכה מאוד. על רקע טיפול אינטנסיבי נגד אולקוס, הכיב מצטלק תוך 3 חודשים. אספקת דם בשפע לתעלה הפילורית גורמת לדימום קיבה מסיבי. אבחון. במהלך הבלתי מסובך של כיב פפטי, אין שינויים בבדיקת הדם הכללית; תיתכן ירידה קלה ב-ESR ואריתרוציטוזה קלה. כאשר מתעוררים סיבוכים בבדיקות דם, מופיעה אנמיה, לויקוציטוזיס - כאשר הצפק מעורב בתהליך הפתולוגי. אין שינויים בניתוח הכללי של שתן. בניתוח ביוכימי של דם במקרים של מהלך מסובך של כיב פפטי, שינויים בפרמטרים של הבדיקה הסיאלית, חלבון C-reactive, תגובת DPA אפשריים. שיטת המחקר המסורתית בפתולוגיה של הקיבה היא קביעת החומציות של תוכן הקיבה. אינדיקטורים שונים אפשריים: גבוהים ונורמליים, במקרים מסוימים אף מופחתים. כיב בתריסריון מתרחש עם חומציות גבוהה של מיץ קיבה. בבדיקת רנטגן, כיב פפטי הוא "גומחה" - מחסן של תרחיף בריום. בנוסף לתסמין רדיוגרפי ישיר כזה, סימנים עקיפים של פגם פפטי חשובים באבחון: הפרשת יתר של תוכן הקיבה על קיבה ריקה, הפרעות פינוי, ריפלוקס תריסריון, הפרעות בתפקוד הלב, עוויתות מקומיות, התכנסות של קפלי רירית, עיוות ציטרי של הקיבה והתריסריון. Gastroduodenoscopy עם ביופסיה היא השיטה האמינה ביותר לאבחון כיב פפטי. זה מאפשר לך להעריך את אופי השינויים בקרום הרירי בשולי הכיב, באזור periulcerous ומבטיח את הדיוק של האבחנה ברמה המורפולוגית. במחקרים אנדוסקופיים ומורפולוגיים, נמצא כי רוב כיבי הקיבה ממוקמים באזור העקמומיות הפחותות והאנטרום, הרבה פחות לעתים קרובות - בקימור הגדול יותר ובאזור התעלה הפילורית. 90% מהכיבים בתריסריון ממוקמים באזור הבולברי. כיב פפטי הוא בדרך כלל עגול או סגלגל. החלק התחתון שלו מורכב ממסים נמקיים, שמתחתיהם יש רקמת גרנולציה. נוכחותם של כתמים כהים בתחתית מצביעה על דימום. שלב ריפוי הכיב מאופיין בירידה בהיפרמיה של הקרום הרירי ובפיר דלקתי באזור הפרי. הפגם הופך פחות עמוק, מתנקה בהדרגה מרובד סיבי. הצלקת נראית כמו אזור היפרמי של הקרום הרירי עם נסיגות ליניאריות או כוכביות של הקיר. בעתיד, במהלך בדיקה אנדוסקופית באתר הכיב לשעבר, נקבעות הפרות שונות של ההקלה של הקרום הרירי: דפורמציות, צלקות, היצרות. באנדוסקופיה, צלקת בוגרת עקב החלפת פגם ברקמת גרנולציה היא בעלת מראה לבנבן, אין סימנים לדלקת פעילה. מחקר מורפולוגי של דגימת ביופסיה המתקבלת מהתחתית והקצוות של הכיב מגלה דטריטוס תאי בצורה של הצטברות של ריר עם תערובת של לויקוציטים מתפוררים, אריתרוציטים ותאי אפיתל מפורקים עם סיבי קולגן הממוקמים מתחתיו. אבחון דיפרנציאלי. עם השימוש הנרחב באנדוסקופיה, האבחנה המבדלת של כיבים בקיבה ובתריסריון (כיבים סימפטומטיים, כיבים ספציפיים בשחפת, עגבת, מחלת קרוהן, סרטן כיב ראשוני, כיבים ממאירים שניוניים) הופכת חשובה במיוחד. לכיבים סימפטומטיים חייבת להיות סיבה שגרמה להם (חשיפה קיצונית, סימנים קליניים ומורפולוגיים של מחלות אנדוקריניות, הפרעות לב וכלי דם ונשימה, מחלות ראומטיות). יותר מאשר עבור כיב פפטי, הם מאופיינים בריבוי של נגעים, לוקליזציה דומיננטית בקיבה וגודל משמעותי. עם כיב פפטי, תסמונת הכאב שוררת, ועם דלקת קיבה כרונית - תופעות דיספפטיות. בדלקת קיבה כרונית, הכאב קל או נעדר, אין עונתיות של המחלה וכאב מוגבל במישוש; החמרה של המחלה תלויה לרוב באופי המזון. מצב תפקוד ההפרשה של הקיבה עם גסטריטיס יכול להיות שונה. יש חשיבות מכרעת לגסטרוסקופיה וגסטרוביופסיה, שבה מתגלים שינויים ברירית האופייניים לגסטריטיס וכיב בכיב פפטי. בקע היאטוס (HH) מלווה לעתים קרובות גם בכאב באפיגסטריום. עם זאת, בניגוד למחלת כיב פפטי, מחלה זו מאופיינת בעיקר בגיל המבוגר של החולים, קשר הכאב עם מנח הגוף (הכאב מתגבר בשכיבה, נחלש במצב זקוף). האבחנה של HH מאושרת על ידי תוצאות בדיקת רנטגן. דלקת כיס כיס כרונית מאופיינת בכאב בהיפוכונדריום ובאפיגסטריום הימני, לעיתים קרובות מקרינים לכתף הימנית, לכתף, לזווית הלסת התחתונה מימין. עם דלקת כיס המרה האקלקולוסית, יש להם אופי עמום, מונוטוני, לוחץ, ועם דלקת כיס המרה החשונית, הם רוכשים אופי של קוליק. בחילות, עצירות, גזים מצוינים. מצב תת-חום מתמשך אפשרי. עם חסימה ממושכת של דרכי המרה, צהבת עלולה להצטרף. האבחנה של פגיעה במערכת המרה מאומתת על ידי אולטרסאונד של חלל הבטן, בדיקת רנטגן (כולציסטוגרפיה), כוללבלב אנדוסקופי אנדוסקופי (ERCP), וכן תוצאות של צלילים בתריסריון, המצוינת רק לתהליך ללא אבנים. בדלקת לבלב חריפה והחמרה של כאב כרוני, הם ממוקמים בחצי השמאלי של האזור האפיגסטרי, הם שלבקת חוגרת בטבע, הנגרמים על ידי צריכת מזון כלשהו. באנמנזה - פתולוגיה של מערכת המרה, שימוש לרעה באלכוהול, שימוש ארוך טווח בתרופות לבלב. לחשוף באופן אובייקטיבי ירידה במשקל, פוליפאקל, סטאטוריה, קריאטורריאה. האבחנה מאושרת על ידי תוצאות בדיקת דם ביוכימית לאנזימי לבלב, צואה - לעיכול, כמו גם נתונים אינסטרומנטליים. טיפול. טיפול רציונלי בכיב פפטי צריך לכלול משטר, תזונה מתאימה, טיפול תרופתי, פסיכותרפיה, שיטות טיפול פיזיות וספא. במהלך תקופת ההחמרה של מחלת כיב פפטי, יש צורך להקפיד על דיאטה חלקית (מ 4 עד 6 פעמים ביום עם נפח קטן של כל מנת מזון שנלקחת בשעות מסוימות). מוצרי מזון חייבים להיות בעלי תכונות חציצה טובות ולהכיל כמות מספקת של חלבון (120-140 גרם). פסיכותרפיה חיונית להפסקה או הפחתת תגובות פסיכונוירוטיות הנובעות מתסמונת כאב מתמשכת והציפיות שלה. תרופות המשמשות לטיפול בכיב פפטי מחולקות ל-5 קבוצות: 1) תרופות המשפיעות על הגורם החומצתי-פפטי (נוגדי חומצה ו-H2חוסמי היסטמין, חומרים נוגדי הפרשה אחרים); 2) תרופות המשפרות את מחסום רירית הקיבה; 3) תרופות המגבירות את הסינתזה של פרוסטגלנדינים אנדוגניים; 4) חומרים אנטיבקטריאליים ואנטיספטיים; 5) תרופות המנרמלות הפרעות בפינוי מוטורי של הקיבה והתריסריון. סותרי חומצה: 1) מסיס (נספג) - ביקרבונט של סודה, סידן פחמתי (גיר) ותחמוצת מגנזיום (מגנזיה שרופה); 2) בלתי מסיס (לא נספג): מגנזיום טריסיליקט ואלומיניום הידרוקסיד. לסותרי חומצה מסיסים יש השפעה בסיסית מהירה, אנרגטית, אך קצרת טווח, אך לעיתים קרובות גורמות לתופעות לוואי, וזו הסיבה שהן אינן משמשות לטיפול בכיבים פפטי. נוגדי חומצה בלתי מסיסים על בסיס אלומיניום הידרוקסיד ומגנזיום הידרוקסיד (Almagel, Phosphalugel, Gelusillac, Topaal, Maalox וכו') מספקים נטרול ארוך טווח של חומצה הידרוכלורית, עוטפים את הקרום הרירי, מגנים עליה מפני ההשפעות המזיקות של חומצה ומזון. בנוסף לנטרול חומצה הידרוכלורית, הם עוזרים להפחית את הפעילות הפרוטאוליטית של מיץ הקיבה, קושרים ליזוליציטין וחומצות מרה, ויש להם אפקט ציטו-פרוטקטיבי אוניברסלי. יש ליטול נוגדי חומצה 1-2 שעות לאחר הארוחות ובלילה. Maalox נקבע בהשעיה (15 מ"ל 4 פעמים ביום) או טבליות (1-2 טבליות 4 פעמים ביום), פוספלוגל - בצורה של ג'ל (16 גרם 3-4 פעמים ביום). אחת מתופעות הלוואי העיקריות של נוגדי חומצה בלתי נספגים היא הפרעה בצואה. תכשירי אלומיניום הידרוקסיד גורמים לעצירות, ולתכשירי מגנזיום הידרוקסיד (מעלוקס) יש השפעה משלשלת תלוית מינון. עידן חדש בטיפול בכיב פפטי החל עם הופעתו של H2- חוסמי היסטמין. בתנאים פיזיולוגיים, היסטמין מתווך גירויים עצביים חוץ-גסטריים והומורליים הגורמים לייצור חומצה. גירוי ייצור חומצה הידרוכלורית על ידי היסטמין נובע מעלייה בפעילות ה-cAMP, הפועל על האנזים אדנילציקלאז המצוי באזור מייצר החומצה בקיבה, המגביר את הפרשת יוני המימן. הנתונים שהתקבלו היוו בסיס לסינתזה של תרופות הקוטעות את השתתפות ההיסטמין בתהליך ההפרשה ברמה התאית, כמו סימטידין, רניטידין, פמוטידין, ניזאטידין ועוד. בנוסף, אנטגוניסטים של H.2-קולטני היסטמין מונעים הפרעות מיקרו-סירקולציה ברירית הקיבה ובכך מונעים התפתחות כיבים. בנוסף, הם מפחיתים את ייצור הפפסין, מגבירים את הפרשת הביקרבונטים, מנרמלים את תנועתיות הקיבה התריסריון, מגדילים את מספר תאי האפיתל המסנתזים DNA, ממריצים תהליכי תיקון ומאיצים את הריפוי של כיבי קיבה ותריסריון כרוניים. עם זאת, תרופות דור 1 (סימטידין, סינמט, בלוממט, טאגמט) עלולות לגרום לשינויים במערכת העצבים, דלקת כבד רעילה, הפרעות קצב והולכה במערכת הלב וכלי הדם ושינויים באיברים ההמטופואטיים. H חוסמי2הדורות הבאים של קולטני היסטמין - ranitidine (zantac, ranisan, gistak), famotidine (kvamatel, lecedil, gastrosidin), nizatidine (roxatidine) שונים מסימטידין בסבילות טובה. Ranitidine נקבע במינון של 150 מ"ג 2 פעמים ביום, famotidine - 20 מ"ג 2 פעמים ביום למשך 4-6 שבועות. למניעת תסמונת גמילה לאחר ריפוי כיב, מומלץ להמשיך ליטול רניטידין (150 מ"ג) או פמוטידין (20 מ"ג) בלילה למשך 2-3 חודשים. בשנים האחרונות הופיעה תרופה נוגדת הפרשה חדשה אומפרזול (אומנול, אומז, לוסק), השייכת לנגזרות של בנזימידאזול. הוא חוסם את האנזים H + -K + -ATPase של משאבת הפרוטונים של התא הפריאטלי. זמן מחצית החיים הקצר (כשעה) ומשך הפעולה הארוך (1-18 שעות) מאפשרים ליטול תרופה זו פעם אחת. אומפרזול נקבעת 24 מ"ג בלילה פעם אחת ביום למשך 20-1 שבועות. אומפרזול מדורגת במקום הראשון מבחינת חומרת ההשפעה האנטי-הפרשה בקרב תרופות מודרניות נגד אולקוס.תופעות הלוואי של התרופה אינן בולטות במיוחד. שימוש נרחב בטיפול בכיבים פפטי מצא גסטרוצפין (נירנזפין, גסטרוזפין), השייך לתרופות אנטיכולינרגיות. התרופה חוסמת באופן סלקטיבי קולטנים מוסקריניים לאצטילכולין הנמצאים בתאי רירית הקיבה המייצרים חומצה הידרוכלורית ופפסין. לגסטרוצפין יש השפעה מעכבת על הפרשת קיבה בסיסית ומעוררת, מעכב את ייצור פפסין, מאט את הפינוי מהקיבה, גורם לעיכוב ייצור גסטרין, מפחית את רמת הפוליפפטיד הלבלב, בעל השפעה ציטופרוקטטיבית על ידי הגברת ייצור גליקופרוטאין ריר בקיבה. , כמו גם על ידי שיפור אספקת הדם לקרום הרירי של אזור הקיבה התריסריון. הקצה אותו ל-50 מ"ג 2 פעמים ביום 30 דקות לפני הארוחות. מהלך הטיפול הוא בממוצע 4 שבועות. תרופות המחזקות את המחסום הרירי של הקיבה כוללות תכשירים של ביסמוט קולואידי (דנול), היוצר סרט מגן על הקרום הרירי, מפחית את הפעילות הפפטית של הקיבה, יוצר תרכובת בלתי מסיסה עם פפסין, משפר את היווצרות הריר, בעל גורם ציטו-פרוטקטיבי. השפעה, הגדלת תכולת הפרוסטגלנדינים בדופן הקיבה. לדנול יש יכולת לעכב את הפעילות של HP ברירית הקיבה. התרופה נרשמה 2 טבליות (240 מ"ג) 2 פעמים ביום חצי שעה לפני הארוחות או שעתיים לאחר הארוחות. כדי למנוע הצטברות של מלחי ביסמוט בגוף, לא מומלץ לבצע טיפול בתרופות אלו במשך יותר מ-2 שבועות. לצורך טיפול אנטיבקטריאלי בכיבים בקיבה ובתריסריון משתמשים בטטרציקלין, אמוקסיצילין וקלריתרמיצין. הם משמשים בשילוב עם תרופות אחרות נגד אולקוס. הוצעו מספר תוכניות של טיפול משולב (שני, שלושה, ארבעה רכיבים). טיפול דו-רכיבי: אמוקסיצילין 1000 מ"ג 2 פעמים ביום למשך שבועיים; אומפרזול 2 מ"ג פעמיים ביום. ערכת שלושת המרכיבים כוללת הכנת ביסמוט קולואידי 40 מ"ג 2 פעמים ביום; טטרציקלין 120 מ"ג 4 פעמים ביום; מטרונידזול 250 מ"ג 4 פעמים ביום. מחזור הטיפול הוא 250 יום. ערכת ארבעת הרכיבים כוללת אומפרזול 20 מ"ג 2 פעמים ביום מהיום הראשון ליום העשירי; דה-נול 1 מ"ג 10 פעמים ביום מהיום הרביעי עד העשירי; טטרציקלין 120 מ"ג 4 פעמים ביום מהיום הרביעי עד העשירי; מטרונידזול 4 מ"ג 10 פעמים ביום מהיום הרביעי עד העשירי. ערכת ארבעת המרכיבים לטיפול בכיב פפטי של הקיבה והתריסריון מוכרת כיעילה ביותר. 500 שבועות לאחר ההליך, הריפוי של הפגם הפפטי נצפה ב-4-4% מהחולים. לאחר הצטלקות של כיב פפטי בקיבה ובתריסריון, משתמשים באופן מסורתי בשני סוגי טיפול. 1) טיפול תחזוקה מתמשך מתבצע עם תרופות נוגדות הפרשה במחצית המינון היומי לתקופה של עד שנה. 2) טיפול "על פי דרישה", כולל שימוש באחד מהתרופות נוגדות הפרשה במחצית המנה היומית למשך שבועיים כאשר מופיעים תסמינים של כיב פפטי. תחזית ומניעה. לצורות לא מסובכות של המחלה יש פרוגנוזה חיובית לחיים ולעבודה. במקרה של סיבוכים של מחלת כיב פפטי, הפרוגנוזה נקבעת על פי זמני הטיפול הכירורגי. מניעת הישנות כיב פפטי כולל ניטור דינמי עם בדיקות מעקב חובה על ידי רופא 2 פעמים בשנה. הבדיקות צריכות לכלול בדיקה קלינית ואנדוסקופית, ובמידת הצורך, בדיקה מורפולוגית. כאמצעי מניעה, מומלץ לנרמל את השינה והמנוחה, לוותר על הרגלים רעים, להגביל צריכת תרופות כיבית, רציונליות של חמש ארוחות ביום ולהשתמש בטיפול דו או שלושה מרכיבים במשך שבוע כל 3 חודשים. הרצאה מס' 12. מחלות במערכת העיכול. מחלות של המעיים. מחלות של המעי הדק. דלקת מעיים כרונית דלקת מעיים כרונית היא מחלה של המעי הדק, המאופיינת בהפרה של תפקודיה (עיכול וספיגה) על רקע שינויים דיסטרופיים ודיסרגנרטיביים, ששיאו בהתפתחות דלקת, ניוון וטרשת של הקרום הרירי של המעי הדק. אטיולוגיה ופתוגנזה. זוהי מחלה פוליאטיולוגית שיכולה להיות תוצאה של דלקת חריפה של המעי הדק או תהליך כרוני ראשוני. בשנים האחרונות, Yersinia, Helicobacteria, Proteus, Pseudomonas aeruginosa, rotaviruses, נציגים רבים של פרוטוזואה והלמינתים (גיארדיה, אסקריס, תולעי סרט, אופיסטורכיה, קריפטוספורידיום) קיבלו חשיבות רבה כגורם אטיולוגי בדלקת מעיים כרונית. חשיבות רבה בהתרחשות של דלקת מעיים כרונית הם גורמי מזון - אכילת יתר, אכילת מזון יבש, מזון לא מאוזן, בעיקר פחמימתי, שימוש לרעה בתבלינים. דלקת מעיים נגרמת מקרינה מייננת, חשיפה לחומרים רעילים ותרופות. בין המנגנונים הפתוגנטיים הנפוצים של מחלות כרוניות של המעי הדק, ישנם שינויים במיקרופלורה של המעי על רקע ירידה בחסינות המקומית והכללית. שינויים במצב החיסוני - ירידה בתכולת ה-IgA המופרשת, עלייה ברמת ה-IgE, ירידה בטרנספורמציה של הבלסט של לימפוציטים ועיכוב נדידת לויקוציטים - מובילים לקולוניזציה של המעי הדק על ידי נציגי מיקרופלורה אופורטוניסטית. ירידה בפלורה אנאירובית תקינה. התיישבות חיידקים של המעי הדק מגבירה את הפרשת המעי עקב הפעלת cAMP של תאי אפיתל, המגבירה את חדירות המעי, מגבירה את ייצור האלקטרוליטים והמים על ידי התאים. הפרשת מים ואלקטרוליטים מובילה להפרה של חילוף החומרים של מים-מלח. תחת השפעת הפלורה המיקרוביאלית, זרימת המרה האנטרו-הפטית מופרעת. חומצות שומן קושרות את יוני הסידן, ויוצרות סבונים מסיסים בקושי המופרשים בצואה. הפרה של חילוף החומרים של סידן מקודמת על ידי שינויים בחילוף החומרים של ויטמין D, אשר מפחית את ספיגת הסידן. בהשפעת הפרעות מטבוליות של ויטמינים מסיסים בשומן, תכולת המיקרו-אלמנטים בדם פוחתת. דיסביוזה ממושכת מקדמת רגישות לאנטיגנים מיקרוביאליים ומזון, גורמת לדלקת חיסונית של הקרום הרירי, מה שגורם להיווצרות אנטיגנים של רקמות. החדירות המוגברת של המחסום הרירי מלווה בספיגה של מקרומולקולות חלבון לא מפוצלות, שהופכות לאלרגנים, ותגובתיות אימונולוגית נפגעת. עם אלרגיות, חומרים פעילים ביולוגית משתחררים המגבירים את החדירות של דופן המעי, משנים את התכונות הפונקציונליות של enterocytes. הפרות של מבנה המיקרו של הממברנה הציטופלזמית האנטוציט מובילות תחילה לעיכוב פעילות הלקטאז, ולאחר מכן פעילות מלטאז וסוקראז. עם שינויים דיסטרופיים, דיסרגנרטיביים באפיתליוציטים, מופחתת הסינתזה של אנזימים וספיגתם על ממברנות האפיתליוציטים - דיסכרידאזות, פפטיזות, אנטרוקינאז, פוספטאז אלקליין - מה שגורם להפרעות בעיכול הממברנה והחלל. כל זה הופך לבסיס של תסמונת תת-הספיגה. בשלבים המוקדמים של המחלה מתפתחות הפרעות בחילוף החומרים של שומנים עקב ירידה בספיגת השומן, איבודו עם צואה ושינויים בשלב המעי של מחזור המרה האנטרוהפטית. הפרה של חילוף החומרים המרה, בתורו, מובילה להפרה של חילוף החומרים השומנים, המשפיעה על המבנה והתפקוד של קרומי התא. בקשר עם ספיגה לא מספקת של שומן, מתרחשת הפרה של סינתזה של סטרואידים, מה שגורם להפרה של הפונקציות של הבלוטות האנדוקריניות. מבחינה מורפולוגית, דלקת מעיים כרונית מתבטאת בשינויים דלקתיים ודיסרגנרטיביים בקרום הרירי של המעי הדק. אם התהליך מתקדם, נצפים ניוון וטרשת שלו. מיון (זלטקינה א.ר., פרולקיס א. ו., 1985). 1) אטיולוגיה: דלקות מעיים, פלישות הלמינתיות, גורמים מעיים, פיזיים וכימיים, מחלות קיבה, לבלב, דרכי המרה. 2) שלבי המחלה: החמרה; הֲפוּגָה. 3) דרגת חומרה: קלה; לְמַתֵן; כָּבֵד. 4) זרם: מונוטוני; חוזר ונשנה; חוזר ברציפות; חָבוּי. 5) אופי של שינויים מורפולוגיים: יחידה ללא ניוון; ג'וניטיס עם ניוון חלקי מתון; דלקת ג'וניטיס עם ניוון חלקי מעורפל; דלקת ג'וניטיס עם ניוון כושל מוחלט. 6) אופי הפרעות תפקודיות: הפרעות בעיכול הממברנה (מחסור בדיסכרידאז), תת ספיגה של מים, אלקטרוליטים, יסודות קורט, ויטמינים, חלבונים, שומנים, פחמימות. 7) סיבוכים: דלקת סולארית, מסאדניטיס לא ספציפית. תמונה קלינית. התמונה הקלינית של דלקת מעיים כרונית מורכבת מתסמונות מעיים מקומיות וכלליות. הראשון נגרם על ידי הפרה של תהליכי העיכול הקודקודית (קרום) וחלל (עיכול לקוי). מטופלים מתלוננים על גזים, כאבים באזור הפראומבילי, נפיחות בצורת כובע, רעמים חזקים, שלשולים, ובאופן פחות שכיח, עצירות. מישוש מגלה כאבים במזוגסטריום, כמו גם בצד שמאל ומעל לטבור (סימן חיובי של Porges), רעש התזה באזור המעי הגס (סימן אובראצטסוב). הצואה מקבלת מראה חרסי, וחומר פוליפאלי אופייני. תסמונת אנטרלית כללית קשורה לפגיעה בספיגה של מרכיבי מזון (חוסר ספיגה), וכתוצאה מכך להפרעות בכל סוגי חילוף החומרים, שינויים בהומאוסטזיס. מאופיין בהפרעות מטבוליות רב-גוניות, בעיקר חלבון, המתבטא בירידה מתקדמת במשקל הגוף. שינויים בחילוף החומרים של הפחמימות פחות בולטים, המתבטאים בנפיחות, רעש בבטן ושלשול מוגבר בזמן נטילת מוצרי חלב. במידה רבה, המחסור במשקל גוף בחולים נובע לא רק מחלבון, אלא גם מחוסר איזון שומנים. שינויים בחילוף החומרים של שומנים קשורים קשר הדוק להפרעות מטבוליות של ויטמינים ומינרלים מסיסים בשומן (סידן, מגנזיום, זרחן). הסימנים האופייניים למחסור בסידן הם סימפטום חיובי של גלגלת השריר, עוויתות, שברים חוזרים "חסרי מוטיבציה", אוסטאופורוזיס, אוסטאומלציה. יש גם נפיחות של הפנים, ציאנוזה של השפתיים, גלוסיטיס, עצבנות, שינה לקויה. הפרות של מאזן המים והאלקטרוליטים מתבטאות בחולשה כללית, חוסר פעילות גופנית, יתר לחץ דם בשרירים, בחילות, הקאות ושינויים במערכת העצבים המרכזית. תסמינים של polyhypovitaminosis הופכים אופייניים לדלקת מעיים כרונית בחומרה בינונית וחמורה. Hypovitaminosis C מתבטאת קלינית בדימום חניכיים, דימום חוזר באף, רחם, חבורות בעור. Hypovitaminosis B מלווה חיוורון של העור, glossitis, stomatitis זוויתי (cheilez). סימנים למחסור בויטמינים מסיסים בשומן (A,O,E,K): ראיית דמדומים לקויה, עור יבש וריריות, דימום מוגבר של החניכיים. צורות חמורות של דלקת מעיים כרונית מתרחשות עם תסמינים של הפרעה בתפקוד האנדוקריני (אי ספיקה פלוריגלנדולרית). היפוקורטיקה מתבטאת ביתר לחץ דם עורקי, הפרעות קצב לב, אנורקסיה ופיגמנטציה של העור. ירידה בפעילות הגונדות מלווה בהפרעות בתפקוד השחלות, הפרעות במחזור החודשי, אצל גברים - אימפוטנציה, גינקומסטיה, נשירת שיער. תפקוד לקוי של בלוטת התריס מאופיין בחולשה כללית, עור יבש, ברדיקרדיה, ירידה בביצועים והפרעות אינטלקטואליות-מנסטיות. אבחון ואבחון מבדל. בדיקת דם כללית מגלה אנמיה מיקרו- ומקרוציטית, עלייה ב-ESR ובמקרים חמורים - לימפה ואאוזינופניה. אם המחלה היא ממקור טפילי, ניתן להבחין בלימפוציטוזיס ואאוזינופיליה בדם. בדיקה סקאטולוגית מגלה סוג מעי של סטאטוריה עקב חומצות שומן וסבונים, קריאטורריאה, עמילוריה. התוכן של אנטרוקינאז ופוספטאז אלקליין בצואה עולה. המסה היומית של הצואה עולה באופן משמעותי. ניתוח בקטריולוגי של צואה מגלה דיסבקטריוזיס בדרגות שונות. יש ירידה בלקטו-וביפידובקטריות, enterococci, זנים של Escherichia coli עם תכונות אנזימטיות משתנות מופיעים. בניתוח הכללי של שתן בצורה חמורה של דלקת מעיים כרונית, מצוינים מיקרואלבומינוריה ומיגרוהמטוריה. בבדיקת דם ביוכימית, היפופרוטאינמיה, היפואלבומינמיה, היפוגלובלינמיה, היפוקלצמיה, ירידה ברמת המגנזיום, הזרחן ומיקרו-אלמנטים נוספים, מתגלות הפרעות במטבוליזם של אלקטרוליטים בצורה של ירידה ברמת הנתרן והאשלגן. הפרעות בחילוף החומרים של השומנים מלוות בשינויים בספקטרום השומנים: רמת הכולסטרול, הפוספוליפידים יורדת, וגם הספקטרום של חומצות המרה, הפוספוליפידים והטריגליצרידים משתנה. תוצאות בדיקת הרנטגן מאפשרות לנו להבהיר את התפקוד המוטורי של המעי הדק ואת ההקלה על הרירית, שינויים דיסטוניים ודיסקינטיים בצורה של האטה או האצה במעבר תרחיף של בריום סולפט דרך המעי הדק. , והקלה על שינויים ברירית בצורה של עיבוי לא אחיד, דפורמציה והחלקה של הקפלים. בדיקת גסטרודואודנוסקופיה חושפת גסטריטיס אטרופית ותריסריון. התמונה המורפולוגית של צורה קלה של דלקת מעיים כרונית מאופיינת בהתעבות של הווילי, דפורמציה שלהם, ירידה בעומק החריצים, ירידה בטונוס השרירים החלקים, בצקת תת-אפיתלית, שינויים ניווניים בפני השטח של האפיתל. , דילול גבול המברשת של תאים, ירידה במספר תאי הגביע באזור הווילי, עלייה במספר הקרפטות, חדירת רירית השכבה עצמה עם אלמנטים לימפופלסמטיים, ירידה בתאי Paneth באזור. של תחתית הקריפטים. עבור הצורה המתונה, אופייניים ניוון חלקי של ה-villi, ירידה במספר הקרפטות, דילול הקרום הרירי, ירידה בגבול המברשת וחדירת לימפו-פלסמציטית של השכבות התת-ריריות והשריריות. הצורה החמורה של המחלה מאופיינת בניוון פרוגרסיבי, המאובחן על פי קריטריונים היסטולוגיים, היסטוכימיים ומורפומטריים. תהליך התפשטות האנטוציטים גובר על ההתמיינות שלהם, מופיע שפע של תאים לא בשלים ופגומים. אבחנה מבדלת בדלקת מעיים כרונית מתבצעת עם מחלת צליאק, מחלת קרוהן, מחלת וויפל, עמילואידוזיס במעי, מחלת דיברטיקולרית, לימפומה, גידולים במעי הדק. המשותף לכל המצבים הללו הם תסמונות קליניות של הפרעות עיכול, ספיגה ודיסבקטריוזיס. האבחנה הסופית מאושרת על ידי בדיקה מורפולוגית של הקרום הרירי של המעי הדק. אז, עבור צליאק אנטרופתיה, אינדיקציה אנמנסטית לקשר של החמרות המחלה עם השימוש במוצרים המכילים גליאדין אופיינית. המרפאה של צליאק אנטרופתיה דומה לדלקת מעיים כרונית. לרוב, המעיים העליונים נפגעים ואין שינויים באילאום. האתר האופטימלי לנטילת דגימות ביופסיה הוא אזור הקרום הרירי ליד הרצועה של טריץ. בדיקה מורפולוגית חושפת ירידה במספר תאי הגביע ועלייה במספר הלימפוציטים הבין-אפיתליים, ניוון סבתא-טוטלי וחדירת תאים דלקתיים לשכבה משלו. עם צליאק אנטרופתיה, שינויים מורפולוגיים על רקע תזונה נטולת גלוטן הם הפיכים, בניגוד לדלקת מעיים כרונית בנאלית, שבה שינויים מורפולוגיים בלתי הפיכים. במחלת קרוהן מציינים פולימורפיזם קליני עקב היצירה האוטואימונית של המחלה והביטויים המערכתיים האופייניים לה (כגון דלקת בלוטת התריס האוטואימונית, פוליארתריטיס, דלקת העין, הפטיטיס, שילוב תכוף של דלקת מעיים וקוליטיס דיסטלי). לבדיקות אנדוסקופיות ומורפולוגיות יש רזולוציה גבוהה באימות מחלת קרוהן, החושפת את אופי הפסיפס של הנגע במעיים, שינויים אופייניים מסוג "ריצוף אבן", המתחלפים עם אזורים של רירית שלמה. צילום רנטגן, בדיקה אנדוסקופית יכולה לזהות היצרות מעיים, לעיתים נוצרות פיסטולות מעיים. אבחון מורפולוגי קובע חדירת תאי דלקת של כל שכבות דופן המעי עם פגיעה מקסימלית בשכבה התת-רירית ושינויים מינימליים ברירית. בשכבה התת-רירית, נמצאות גרנולומות דמויות סרקואיד לימפוציטי, פתוגנומוניות למחלה זו. מחלת וויפל, בנוסף לסימנים של דלקת מעיים, מאופיינת בביטויים מחוץ למעיים בצורה של חום, דלקת פרקים, לימפדנופתיה, יתר לחץ דם עורקי ופיגמנטציה של העור. הקריטריונים המורפולוגיים האינפורמטיביים ביותר של המחלה. דגימות ביופסיה שנלקחו מהמעי הדק חושפות הצטברות שומן תוך-תאית וחוץ-תאית ברירית המעי הדק ובלוטות הלימפה המזנטריות; חדירת שכבה משלו על ידי מיקרופגים גדולים המכילים גרגירים נטולי שומן חיוביים מסוג CHIC, ונוכחות של bacilli ברירית. טיפול. הטיפול בדלקת מעיים כרונית צריך להיות מקיף, כולל גורמים המשפיעים על גורמים אטיולוגיים, מנגנונים פתוגנטיים, כמו גם תסמינים מקומיים וכלליים של המחלה. הבסיס הוא תזונה תזונתית, המסייעת להפחית את הלחץ האוסמוטי המוגבר בחלל המעי, מפחיתה הפרשה ומנרמלת את מעבר תוכן המעי. אל תכלול מוצרים המכילים סיבים צמחיים גסים (ירקות חיים, פירות, לחם שיפון, אגוזים, מאפים, שימורים, תבלינים, מנות חריפות, חלב מלא, בירה, קוואס, משקאות מוגזים ואלכוהוליים). השימוש במלח שולחני מוגבל. יש צורך בארוחות חלקיות, עד 5-6 פעמים ביום. במהלך תקופת ההפוגה, כמה ירקות ופירות מוכנסים לתזונה, עד 100-200 גרם ליום. להקצות חסה, עגבניות קלופות בשלות, אגסים רכים, תפוחים מתוקים, תפוזים, קלמנטינות, פטל, תותים, תותי בר. מזון צריך להיות מבושל או מאודה. הטיפול התרופתי צריך להיות אטיוטרופי, פתוגנטי ותסמיני. טיפול אטיוטרופי: עבור דיסביוזיס דרגה II-IV, תרופות אנטיבקטריאליות נקבעות: מטרונידזול (0,5 גרם 3 פעמים ביום), קלינדמיצין (0,5 גרם 4 פעמים ביום), צפלקסין (0,5 גרם 2 פעמים ביום). יום), ביספטול ( 0,48 גרם 2 פעמים ביום), סולגין (1 גרם 3-4 פעמים ביום), furazolidon (0,1 גרם 4 פעמים ביום). לאחר שימוש בתרופות אנטיבקטריאליות, נרשמים יוביוטיקה - bifidumbacterin או bificol 5 מנות 3 פעמים ביום 30 דקות לפני הארוחות, coli-bacterin או lactobacterin 3 מנות 3 פעמים ביום לפני הארוחות, hilakforte 40 טיפות 3 פעמים ביום לפני הארוחות. הטיפול בתכשירים חיידקיים מתבצע לאורך זמן: 3 קורסים של 3 חודשים בכל שנה. עבור dysbacteriosis staphylococcal, בקטריופאג אנטי-סטפילוקוקלי נקבע (20 מ"ל 3 פעמים ביום למשך 15-20 ימים), עבור פרוטאוס דיסבקטריוזיס - קוליפרוטאוס בקטריופאג' דרך הפה, 20 מ"ל 3 פעמים ביום, מהלך הטיפול הוא 2-3 שבועות. כסוכן סימפטומטי נגד שלשולים, אימודיום (לופרמיד) נקבעת כמוסה אחת 1-2 פעמים ביום לפני הארוחות למשך 3-3 ימים. לשיפור תהליך העיכול מומלצים אנזימים: pancreatin, panzinorm forte, festal, digestal, pankurmen, mezim forte, trienzyme, שהמינונים שלהם נבחרים בנפרד (מ-1 טבליה 3 פעמים ביום ועד 3-4 טבליות 4 פעמים ביום ) ואשר נרשמים ישירות לפני או במהלך ארוחות למשך 2-3 חודשים. במידת הצורך, הטיפול באנזים חלופי נמשך זמן רב יותר. כדי לנרמל את המצב הכללי של חולים עם דלקת מעיים ולחסל הפרעות מטבוליות, יש לציין טיפול תחליף. על מנת לפצות על המחסור בויטמינים, ויטמינים B ו-B נקבעים למשך 4-5 שבועות.6 50 מ"ג כל אחד, PP - 10-30 מ"ג, C - 500 מ"ג כל אחד. עבור steatorrhea, מתן פרנטרלי של ויטמין B מצוין.2 (100-200 מק"ג) בשילוב עם ויטמינים מסיסים בשומן. ריבופלבין 0,02 גרם, חומצה פולית 0,003 גרם פעם ביום, ויטמין E 3300 IU 2 פעמים ביום נקבעים בפנים. בדלקת מעיים כרונית המתרחשת עם מחסור חמור בחלבונים, יחד עם דיאטה, מתן פרנטרלי של פלזמה, 150-200 מ"ל הידרוליזטים חלבונים ותערובות של חומצות אמינו (אמינופפטיד, אלבסין, פוליאמין, תוך-פוסין, 250-500 מ"ל תוך ורידי למשך 20 ימים) שילוב עם הורמונים אנבוליים (retabolil 2,0 מ"ל פעם אחת ב-1-7 ימים למשך 10-3 שבועות) ותערובות שומניות כגון intralipid. המינוי של סטרואידים מצוין רק עם מחסור משמעותי בחלבון, hypoproteinemia, נוכחות של אי ספיקת יותרת הכליה. לתיקון הפרעות מים ואלקטרוליטים, זריקות תוך ורידי של panangin 20-30 מ"ל, סידן גלוקונאט 10% 10-20 מ"ל ב-200-400 מ"ל של תמיסה איזוטונית או תמיסת גלוקוז, תמיסות פוליוניות "דיסול", "טריסול", "קוורטסול" מסומנים. תמיסות אלקטרוליטים ניתנות תוך ורידי למשך 10-20 ימים בשליטה של מצב חומצה-בסיס ורמת האלקטרוליטים בדם. תחזית ומניעה. הפרוגנוזה לחיים וליכולת לעבוד חיובית ברוב המקרים. סימנים לא חיוביים מבחינה פרוגנוסטית הם מהלך חוזר מתמשך של המחלה, ירידה פתאומית משמעותית במשקל, אנמיה, תסמונת הפרעה אנדוקרינית (ירידה בחשק המיני, דיסמנוריאה, אי פוריות). מניעה של דלקת מעיים כרונית מורכבת מטיפול בזמן של דלקות מעיים חריפות ומחלות נלוות של אזור הקיבה התריסריון, בהתאם לתזונה, בניהול מניעתי של תכשירים חיידקיים במהלך רנטגן והקרנות. הרצאה מס' 13. מחלות במערכת העיכול. מחלות של המעיים. מחלת קרוהן מחלת קרוהן היא מחלת מעי כרונית עם ביטויים מערכתיים; הבסיס המורפולוגי שלה הוא דלקת אוטואימונית גרנולומטית של מערכת העיכול. אטיולוגיה ופתוגנזה. האטיולוגיה ופתוגנזה של המחלה לא נחקרו מספיק. הפופולריים ביותר הם המושגים הזיהומיים והחיסוניים של התרחשות המחלה. בשנים האחרונות הופיעו דיווחים על תפקידם האטיולוגי של מיקרואורגניזמים מהסוג Yersinia. עם זאת, קשה לקבוע אם סוכנים מיקרוביאליים אלה הם פתוגנים או commensals. יחד עם זאת, לשינויים במיקרופלורה של המעיים תפקיד חשוב בפתוגנזה של המחלה. בדרך כלל, ירידה בחיידקים מסוג bifidum עם עליה בו זמנית של enterobacteria עם סימני פתוגניות. מנגנונים אוטואימוניים משחקים תפקיד בהתפתחות המחלה. במחלת קרוהן מופיעים נוגדנים עצמיים (IgC, IgM) כנגד רקמות המעי. המצע המורפולוגי של המחלה הוא תהליך דלקתי אוטואימוני המתרחש בתחילה בשכבת התת-רירית, משתרע לכל עובי דופן המעי ומאופיין בנוכחות של חדירות גרנולומטיות עם כיב לאחר מכן של הקרום הרירי, התפתחות מורסות ו פיסטולות שמתרפאות עם היווצרות צלקות והיצרות של לומן המעי. עם התגברות משך המחלה, היקף הנגע עולה ומופיעים תסמינים של הפרעות מחוץ למעיים. מיון. סיווג (F.I. Komarov, A.I. Kazanov, 1992). 1) קורס: חריף; כְּרוֹנִי. 2) מאפייני התהליך: נגע בתוך המעי הדק; נגע בתוך אזור ileocecal; נגע בתוך המעי הגס. 3) סיבוכים: היצרות של המעי; התרחבות רעילה של המעי הגס; פיסטולות; עמילואידוזיס; נפרוליתיאזיס, כולליתיאסיס; בְּ12-אנמיה של מחסור. תמונה קלינית. התמונה הקלינית של מחלת קרוהן מאופיינת בגיוון משמעותי, הנקבע לפי לוקליזציה והיקף התהליך הפתולוגי במעי, צורת המחלה ותוספת סיבוכים. הופעת המחלה יכולה להיות חריפה, כאשר המחלה מתקדמת כבר מההתחלה, וכרונית כאשר המחלה מתחילה בהדרגה. במקרה הראשון, האבחנה נעשית לעיתים קרובות במהלך לפרוטומיה המבוצעת עבור חשד לדלקת התוספתן, או חסימת מעיים שהתפתחה ללא סיבה נראית לעין בקרב צעירים. במקביל, נמצא אזור היפרמי של המעי הדק, בלוטות לימפה מוגדלות של השורש המזנטרי, האופייניים למחלת קרוהן. חולים מתלוננים על כאבים בבטן ללא לוקליזציה ספציפית, התרופפות של הצואה ללא זיהומים פתולוגיים גלויים, ירידה במשקל, טמפרטורת גוף בדרגה נמוכה. מחקר אובייקטיבי נותן תשומת לב לחיוורון של העור, המתאם עם חומרת האנמיה, נפיחות ברגליים עקב פגיעה בספיגה ומטבוליזם של חלבון. במישוש הבטן מציינים גזים ורעש. כאשר התהליך ממוקם במעי הגס, יש לסירוגין של עצירות עם שלשולים, כאבי בטן מתכווצים, צואה נוזלית או חצי צורה המכילה תערובת של דם. כאשר מערכת העיכול העליונה מושפעת, מופיעים תסמינים הדומים לדלקת ושט כרונית, דלקת קיבה כרונית ותריסריון כרוני. ייתכנו כאבים מאחורי עצם החזה במהלך מעבר המזון בוושט, כאבי לילה וכאבים "רעבים" באפיגסטריום, כאבים במישוש באזור הפילורדודנאלי. במהלך בדיקה גופנית של המטופל נקבעים חיוורון של העור, מצב תת-חום, חוסר במשקל הגוף, מישוש מגלה לולאות מעיים עוויתיות, כאבים באזור ה-paraumbilical, באזור הכסל הימני. במחלת קרוהן מציינים סימנים חוץ-מעיים של המחלה: אפטות סטומטיטיס, פלגמון ופיסטולות של חלל הפה, דלקת פרקים, הדומה לדלקת מפרקים שגרונית במרפאה, עם תסמינים אופייניים של נגעים סימטריים של מפרקים קטנים, נוקשות בבוקר. שינויים אופייניים בעיניים: דלקת קשתית, אירידוציקליטיס, מקולופתיה. העור עלול לפתח אריתמה נודוסה ו-pyoderma gangrenosum. שלשול מאופיין בעלייה בתדירות הצואה עד 10 פעמים ביום או יותר, חומר פוליפאלי. נפח הצואה נקבע על ידי לוקליזציה אנטומית של התהליך: עם פגיעה במעי הדק הפרוקסימלי, נפח הצואה גדול בהרבה מאשר עם פגיעה בחלקים הרחוקים. ירידה במשקל נצפתה בכל החולים. אבחון ואבחון מבדל. בדיקת דם קלינית במהלך החמרה מגלה לויקוציטוזיס, אנמיה ועלייה ב-ESR. שינויים בניתוח השתן הכללי מופיעים בצורות חמורות, המאופיינת בתוספת עמילואידוזיס כלייתית (פרוטאינוריה). בדיקת דם ביוכימית מגלה היפופרוטאינמיה, היפואלבומינמיה, עלייה ב-α-globulins, ירידה בתכולת הברזל, ויטמין B12, חומצה פולית, אבץ, מגנזיום ואשלגן. הנתונים של בדיקה סקאטולוגית מאפשרים להעריך בעקיפין את רמת הנגע. ב-coprogram עם לוקליזציה של המעי הדק של התהליך, חומר פוליפאלי, steatorrhea, creatorrhea נמצאים; עם המעי הגס - תערובת של ריר, לויקוציטים, אריתרוציטים. אבחון רנטגן מאפשר לך לקבוע את הלוקליזציה והשכיחות של התהליך הפתולוגי במעי. אזורים של המעי הפגוע מתחלפים עם אזורים של המעי ללא שינוי. הלולאות המשתנות הופכות נוקשות, התמונה היא פסיפס עם פגמי מילוי קטנים ועם חדירת ניגודיות מעבר לדופן המעי בצורת כיסים. המעי באזור הפגוע מקבל אופי של שוליים עדינים, עם היווצרות פסאודיברטיקולה. יכולת ההתכווצות של דופן המעי מופחתת או אובדת לחלוטין, פינוי הבריום מאט. נצפית היצרות לא אחידה של לומן המעי, כתוצאה מכך, הוא הופך להיות כל כך צר שהוא מקבל צורה של תחרה. מעל אזור ההיצרות, המעי מתרחב. לאבחון אנדוסקופי חשיבות מכרעת באימות האבחנה. עבור מחלת קרוהן, המאפיין ביותר הוא השינוי באנטרום הקיבה ובחתך הראשוני של התריסריון. מבחינה אנדוסקופית, ניתן לזהות היצרות מעגלית של האנטרום, הדומה להיצרות גידול. התקופה הראשונית של מחלת קרוהן מאופיינת בנתונים אנדוסקופיים גרועים: קרום רירי עמום, מולו נראות שחיקות מסוג אפטות, מוקף בגרגירים לבנבן. דפוס כלי הדם נעדר או מוחלק. בלומן של המעי ועל דפנות, ריר מוגלתי נקבע. בהפוגה קלינית, השינויים המתוארים עשויים להיעלם לחלוטין. ככל שהמחלה מתקדמת, הרירית מתעבה בצורה לא אחידה, יש לה צבע לבנבן, ומבחנים סדקים שטחיים או עמוקים. לומן המעי מצטמצם, מה שמקשה על התקדמות הקולונוסקופ. קולונוסקופיה מאפשרת לבצע ביופסיה ממוקדת של הקרום הרירי בכל חלק של המעי הגס ובאיליאום הטרמינל. במחלת קרוהן, התהליך הפתולוגי מתחיל בשכבה התת-רירית, ולכן יש לבצע את הביופסיה באופן שחלק מהשכבה התת-רירית ייכנס לחומר הביופסיה. בהקשר לאמור לעיל, ב-54% מהמקרים לא מתגלה המצע המורפולוגי של המחלה. יש צורך להבדיל בין מחלת קרוהן לבין קוליטיס כיבית לא ספציפית, שחפת במערכת העיכול, קוליטיס איסכמית, מחלת וויפל, מחלת דיברטיקולרית, קוליטיס פסאודוממברני, מחלת הודג'קין, עמילואידוזיס ראשוני של המעי הדק, דלקת מעיים כרונית. המשותף לכל המחלות הללו הן תסמונת דיספפסיה במעיים וכמה נגעים מערכתיים. עם זאת, קוליטיס כיבית מאופיינת בשינוי בחלקים הדיסטליים של המעי הגס תוך מעורבות חובה של פי הטבעת והסיגמואיד בתהליך. בקוליטיס כיבית לא ספציפית, אין פילוח של הנגע; בתדירות נמוכה יותר מאשר במחלת קרוהן, נקבעים ביטויים מערכתיים ותסמונת תת-ספיגה פחות בולטת. עם זאת, האבחנה המדויקת ביותר של מחלת קרוהן מאושרת על ידי אנדוסקופיה עם ביופסיה ממוקדת. צורת שחפת במערכת העיכול נבדלת ממחלת קרוהן על ידי לוקליזציה תכופה באילאום, ממצאים אנדוסקופיים המאפשרים זיהוי של כיבים עם קצוות מוגבהים ומפולפים מלאים בתוכן אפרפר. כיבים כאלה מתרפאים עם היווצרות צלקת קצרה, שאינה נצפית במחלת קרוהן. בקשישים יש צורך להבדיל בין מחלת קרוהן לבין קוליטיס איסכמית. עבור האחרונים, התקפי כאב עזים בבטן לאחר אכילה הם שינויים בקוליטיס אופייניים הניתנים לזיהוי איריגוסקופי בכיפוף הטחול, במעי הגס היורד והסיגמואידי. הסימן הרנטגני החשוב ביותר של קוליטיס איסכמית הוא סימפטום "טביעת אגודל". בדיקה אנדוסקופית ומורפולוגית מגלה אופיינית לתאים המכילים המוסידרין בקוליטיס איסכמית ופיברוזיס בחומר הביופסיה. האבחנה של לימפוגרנולומטוזיס ועמילואידוזיס ראשוני במעי נעשית על בסיס בדיקה היסטולוגית. במקרה הראשון, תאי ברזובסקי-שטרנברג נמצאים בדגימת הביופסיה מבלוטת הלימפה המזנטרית, במקרה השני, יש משקעים של עמילואיד ברירית פי הטבעת. טיפול. דיאטה עדינה מבחינה מכנית וכימית עם תכולה גבוהה של חלבונים, ויטמינים, מיקרו-אלמנטים, עם הרחקה של חלב אם הוא לא סובלני, והגבלה של סיבים צמחיים גסים. השימוש בהידרוליזטים אנטרליים נוזליים מסומן. Salazopreparations וקורטיקוסטרואידים מהווים את הבסיס לטיפול תרופתי פתוגנטי. המינון היומי של תרופות הוא 3-6 גרם. עם לוקליזציה של התהליך הפתולוגי במעי הגס, הפעילות של sulfasalazine עולה על הפעילות של פרדניזולון. בהיעדר השפעת השימוש בסולפסאלזין, עם נגעים בעיקר במעי הדק וסימנים בולטים של דלקת חיסונית, כמו גם בנוכחות ביטויים מערכתיים של המחלה, יש לציין שימוש בקורטיקוסטרואידים. השפעת השימוש בהם מצוינת ב-8 השבועות הראשונים מתחילת הטיפול. Prednisolone נקבע על פי התוכנית הבאה: בשיא החמרה, 60 מ"ג ליום, לאחר מכן המינון מופחת בהדרגה ובשבוע ה-6-10 מותאם למינון תחזוקה של 5-10 מ"ג ליום. עם הגעה להפוגה קלינית, התרופה מבוטלת בהדרגה. אם לא הושגה הפוגה, הטיפול בפרדניזולון נמשך על בסיס אשפוז עד 52 שבועות. במהלך חמור של המחלה, במקרה של סיבוכים בצורת פיסטולות רקטווגינליות, עור-אנטריות, enteroenteric, הזרם של 6-mercaptopurine דרך הפה ב-0,05 גרם 2-3 פעמים ביום מיועד לקורסים של 10 ימים עם מרווח של 3 ימים עד להשגת הפוגה קלינית. לאחר מכן, הם עוברים ליטול מנות תחזוקה של התרופה במהלך השנה. המינון של 6-מרקפטופורין במקרה זה הוא 75 מ"ג ליום. ניתן לקבוע את השפעת הטיפול בתרופות מדכאות לא לפני 3-4 חודשים. שימוש נרחב בטיפול במחלת קרוהן נמצא על ידי מטרונידזול, שההתוויות העיקריות עבורו הן פיסטולות וסדקים פריאנליים, חוסר השפעתם של סאלזופרפרפרס וגלוקוקורטיקואידים וכן הישנות של המחלה לאחר כריתת פרוקטקטומי. התרופה נקבעת במינון של 500-1000 מ"ג ליום. משך הקורס הרציף לא יעלה על 4 שבועות. טיפול סימפטומטי במחלת קרוהן מצטמצם למינוי קורסים קצרים (2-3 ימים כל אחד) של תרופות נגד שלשולים (מודיום, לופרמיד). המינונים נבחרים בנפרד בהתאם להשפעה הקלינית. אין לרשום תרופות נגד שלשולים במשך זמן רב (יותר מ-5 ימים). בהקשר לנוכחות של תסמונת תת-ספיגה במחלת קרוהן, משתמשים בתכשירי אנזימים שאינם מכילים חומצות מרה (פנקריאטין, מסימפורטה, סוליזים, סומילאז) במינון של 2 עד 6 טבליות בכל ארוחה. על פי האינדיקציות, אנמיה והיפואלבומינמיה מתוקנים על ידי רישום תכשירי ברזל (פרנטרלי) ומתן Alvezin, הידרוליזרי חלבון, aminopeptide, aminoblood. הקצה מולטי ויטמינים בכדורים, Essentiale בכמוסות. הטיפול בדיסבקטריוזיס מתבצע על פי כללים כלליים. תחזית ומניעה. עם מחלת קרוהן, הפרוגנוזה לחיים עם אבחון בזמן ומעקב יעיל היא חיובית, אך לגבי העבודה אין ודאות. בחולים עם מחלה קשה, בנוכחות סיבוכים וביטויים מערכתיים, נקבעת קבוצת מוגבלות I או II. מחלת קרוהן היא מחלה טרום סרטנית. יש להכיר את החולה בפירוט עם המאפיינים של מהלך המחלה ולהזהיר מפני סיבוכים אפשריים, תוך תיאור הביטויים הקליניים שלהם בצורה נגישה. הרצאה מס' 14. מחלות במערכת העיכול. מחלות של המעי הגס. קוליטיס כיבית לא ספציפי קוליטיס כיבית לא ספציפי היא מחלה דלקתית הפוגעת בקרום הרירי של המעי הגס בשינויים כיביים-הרסניים, שיש לה מהלך הישנות כרוני, המלווה לרוב בהתפתחות של סיבוכים מסכני חיים. אטיולוגיה ופתוגנזה. קוליטיס כיבית לא ספציפי היא מחלה אידיופטית. הסיבות להתרחשותו אינן ידועות. מבין התיאוריות הרבות המסבירות את מקור המחלה (זיהומית, אנזימטית, אלרגית, חיסונית, נוירוגנית וכו'), התיאוריה הזיהומית היא בעלת עניין רב, אך ניסיונות לבודד את הפתוגן מתוכן המעי הגס לא צלחו. התהליך הפתולוגי בקוליטיס כיבית כרונית מתחיל בפי הטבעת ומתפשט בכיוון הפרוקסימלי, לוכד את החלקים שמעל של המעי הגס. הדלקת יכולה להיות מוגבלת לרקטום (פרוקטיטיס), פי הטבעת וסיגמואיד (proctosigmoiditis), להתפשט לכל החלק השמאלי (קוליטיס צד שמאל), או להשפיע על המעי הגס כולו (קוליטיס מוחלט). במונחים תפקודיים, אורך המעי הגס בקוליטיס לא ספציפי מצטמצם בכ-1/3. במחקר של חומר פתולוגי גילה דלקת מפוזרת של הקרום הרירי של המעי הגס (בצקת בולטת ושפע, עיבוי של קפלים). כיבים בגדלים שונים נוצרים ברירית, בעלי צורה לא סדירה, שתחתיתם ממוקמת בקרום הרירי, לעתים רחוקות יותר בשכבה התת-רירית, בקרומים השריריים והסירוניים. מבחינה מורפולוגית, בתקופה הראשונית, נקבעת הסתננות בלמינה פרופריה של הקרום הרירי, המורכבת מלימפוציטים עם תערובת של לויקוציטים פולימורפו-גרעיניים, התרחבות של כלי דם ונפיחות של האנדותל של כלי אלה. הפרת microcirculation מלווה בהתפתחות של היפוקסיה, אשר מחמירה את ההפרות של המבנה והתפקוד של האפיתל הרירי. שלב הביטויים הקליניים המובהקים מלווה בחדירת לויקוציטים של שכבת פני השטח של האפיתל, התפתחות של קריפטיטיס, שבה מתרחשות הצטברויות של נויטרופילים בלומן של הקריפטים. החלקים המרוחקים של הקריפטים נמחקים, מופיעות מורסות קריפטה, שבהיווצרותן תפקיד חשוב בהתבגרות לקויה של אפיתליוציטים. עם נמק של האפיתל המרפד את הקריפטים, מורסות קריפטה נפתחות, נוצרים כיבים. במהלך תקופת ההפוגה, הקרום הרירי משוחזר, אך נותרו ניוון, דפורמציה של הקריפטים ועיבוי לא אחיד של lamina propria. מיון (Yu. V. Baltaitis et al., 1986). מאפיין קליני. 1. צורה קלינית: 1) חריף; 2) כרוני. 2. נוכחי: 1) מתקדם במהירות; 2) הישנות מתמשכת; 3) חוזרים; 4) סמוי. 3. דרגת פעילות: 1) החמרה; 2) החמרה דועכת; 3) הפוגה. 4. חומרה: 1) אור; 2) מתון; 3) כבד. מאפיין אנטומי. 1. מאפיין מקרוסקופי: 1) פרוקטיטיס: 2) proctosigmoiditis; 3) נגע תת-טוטלי; 4) תבוסה מוחלטת. 2. מאפיין מיקרוסקופי: 1) הדומיננטיות של תהליכים הרסניים-דלקתיים; 2) הפחתת תהליכים דלקתיים עם אלמנטים של תיקון; 3) השלכות התהליך הדלקתי.סיבוכים. 1. מקומי: 1) דימום מעיים; 2) ניקוב של המעי הגס; 3) היצרות של המעי הגס; 4) פסאודופוליפוזיס; 5) זיהום מעי משני; 6) היעלמות של הקרום הרירי; 7) התרחבות רעילה של המעי הגס; 8) ממאירות. 2. כללי: 1) היפוקורטיקה תפקודית; 2) אלח דם; 3) ביטויים סיסטמיים - דלקת פרקים, דלקת פרקים, נגעים בעור, דלקת קשתית, עמילואידוזיס, פלביטיס, דלקת חוליות טרשית, ניוון כבד. תמונה קלינית. התמונה הקלינית של קוליטיס כיבית היא פולימורפית ותלויה בחומרת המהלך ובחומרת התהליך. מהלך התהליך הדלקתי, הנחשב לרוב כרוני, במקרים מסוימים הופך חריף. גם מידת הנזק למעי הגס עשויה להשתנות. קוליטיס כיבית לא ספציפי מאופיינת ב-3 תסמינים מובילים: הפרשת דם ארגמן במהלך יציאות, תפקוד לקוי של המעיים וכאבי בטן. בידוד דם (מפסים על פני הצואה ועד 300 מ"ל או יותר) במהלך עשיית הצרכים הוא הסימן הראשון למחלה. בצורה החריפה של המחלה, הדם מופרש באמצעות סילון, מה שמוביל לירידה בלחץ הדם עד להתפתחות קריסה והלם דימומי. תפקוד לקוי של המעי מתבטא בצורה של תלונות על צואה בלתי יציבה חוזרת ונשנית, הנובעת מפגיעה נרחבת בקרום הרירי וירידה בספיגת מים ומלחים. לרוב, שלשול מתרחש עם קוליטיס כיבית חמורה. עם זאת, שלשול אינו אינדיקטור אמין לחומרת התהליך. חומרת השלשול בשילוב עם נוכחות של דם אדום בצואה חשובה. במספר לא מבוטל של חולים עם קוליטיס כיבית, דם וליחה נמצאים מעת לעת על פני הצואה שנוצרה, שלעתים קרובות רואים בטעות כביטוי של טחורים. מטופלים מתלוננים על כאבים בבטן התחתונה בעלי אופי מתכווץ או קבוע, הממוקם לעתים קרובות יותר בהיפוגסטריום או באזור הכסל השמאלי, מתגבר לפני פעולת עשיית הצרכים ונעלם לאחריו. לעתים קרובות מצוין טנסמוס. כאשר השכבות התת-ריריות, השריריות והסרוניות של המעי מעורבות בתהליך, הכאב מתגבר; מישוש של הבטן מופיע הגנה של השרירים של דופן הבטן הקדמית. המהלך הקל של קוליטיס כיבית לא ספציפי מאופיין במצב משביע רצון של החולים. הכאב בבטן הוא בינוני וקצר טווח. הכיסא מעוצב, מואץ, עד 2-3 פעמים ביום. דם וליחה נמצאים בצואה. התהליך הוא מקומי בתוך פי הטבעת והמעי הגס הסיגמואידי. הקורס הקליני חוזר על עצמו. השפעת הטיפול בתכשירי salazopreparations משביעת רצון. הישנות מתרחשות לא יותר מ-2 פעמים בשנה. ההפוגות יכולות להיות ארוכות (יותר מ-2-3 שנים). המהלך המתון של המחלה מאובחן אם למטופל יש שלשול. הכיסא תדיר (עד 6-8 פעמים ביום), בכל מנה נראית תערובת של דם וליחה. כאבי התכווצות בבטן חזקים יותר. יש חום לסירוגין עם עלייה בטמפרטורת הגוף עד 38 מעלות צלזיוס, חולשה כללית עזה. ייתכנו גם ביטויים מחוץ למעיים של המחלה (דלקת פרקים, דלקת אובאיטיס, אריתמה נודוסום). הקורס חוזר על עצמו ברציפות, ההשפעה של תכשירי סלאזו אינה יציבה, הורמונים נקבעים במהלך החמרה. הצורה החמורה של המחלה מאופיינת בהתפרצות חריפה. נגע כולל של המעי הגס מתפתח במהירות עם התפשטות התהליך הפתולוגי עמוק לתוך דופן המעי. מצבו של החולה מידרדר במהירות. המרפאה מתאפיינת בהתפרצות פתאומית, חום גבוה, שלשולים רבים עד 24 פעמים ביום, דימום רב במעיים ועלייה מהירה בהתייבשות. טכיקרדיה מופיעה, לחץ הדם יורד, עלייה בביטויים מחוץ למעיים של קוליטיס כיבית לא ספציפית. טיפול שמרני לא תמיד יעיל, ולעתים קרובות נדרש ניתוח חירום. אבחון ואבחון מבדל. בבדיקות דם קליניות בצורות קלות של המחלה, לוקוציטוזיס נויטרופילי קל, עלייה ב-ESR וספירת דם אדומים אינם משתנים. ככל שחומרת המהלך עולה ומשך ההחמרה עולה, מתרחשת אנמיה ממקור מעורב (B12-חסר וחסר ברזל), ESR מוגבר. בניתוח הביוכימי של דם בצורות מתונות וחמורות, צוינו דיספרוטינמיה, היפואלבומינמיה, היפרגמגלבולינמיה, חוסר איזון אלקטרוליטים ומצב חומצה-בסיס. בניתוח הכללי של שתן, שינויים מופיעים רק כאשר מתרחשים סיבוכים בצורה של תסמונת נפרוטית על רקע עמילואידוזיס, כאשר מציינים שינויים אופייניים בבדיקות שתן - פרוטאינוריה, משקעי שתן "מתים", יש גם עלייה בדם ורמת הקריאטינין, אוריאה. התפקיד העיקרי באבחון נרכש על ידי בדיקה אנדוסקופית עם ביופסיה ממוקדת, שכן בקוליטיס כיבית לא ספציפית, רירית המעי הגס מושפעת בעיקר. פי הטבעת מעורבת תמיד בתהליך הפתולוגי, כלומר, שינויים שחיקתיים וכיבים מתגלים במהלך אנדוסקופיה מיד מאחורי הסוגר האנאלי במהלך סיגמואידוסקופיה. בקוליטיס כיבית, לא תמיד ניתן להתגבר על העיקול הרקטוסיגמואידי עקב עווית חמורה. ניסיון להחזיק את הצינור של הפרוקטוסקופ מלווה בכאבים עזים. במצב זה יש להחדיר את הפרוקטוסקופ לעומק של לא יותר מ-12-15 ס"מ. קולונוסקופיה במהלך החמרה חמורה של קוליטיס כיבית לא ספציפית אינה בטוחה לביצוע. יש להשתמש בו בסיכון גבוה לממאירות. יש לציין את תכולת המידע הגבוהה של סיגמואידוסקופיה. התמונה האנדוסקופית תלויה בצורת המחלה. עם צורה קלה, נראים ריריות עמומות בצקת, שכבות לבנבות עבות של ריר על דפנות המעי ודימום מגע קל. דפוס כלי הדם של השכבה התת-רירית אינו נקבע חזותית. עם מהלך מתון של המחלה, מתגלים היפרמיה ובצקת של הקרום הרירי, דימום מגע חמור, שטפי דם, שחיקות וכיבים בצורת לא סדירה, שכבות עבות של ריר על דפנות המעי. במהלך חמור של המחלה, הקרום הרירי של המעי הגס נהרס במידה ניכרת. נמצא משטח פנימי גרגירי ומדמם, אזורים נרחבים של כיב עם משקעים פיבריניים, פסאודופוליפים בגדלים וצורות שונות, מוגלה ודם בלומן המעי. התוויות נגד לקולונוסקופיה וסיגמואידוסקופיה הן צורות חמורות של קוליטיס כיבית בשלב החריף של המחלה. בדיקת רנטגן מאפשרת לקבוע את היקף הנגע; להבהיר את האבחנה במקרה של נתוני אנדוסקופיה לא משכנעים מספיק; אבחנה מבדלת עם מחלת קרוהן, מחלת דיברטיקולרית, קוליטיס איסכמית; לזהות בזמן סימנים של ממאירות. צילומי רנטגן רגילים יכולים לחשוף קיצור של המעי, חוסר גזירה, התרחבות רעילה, גז חופשי מתחת לכיפת הסרעפת במהלך ניקוב. יש לבצע איריגוסקופיה בזהירות רבה. זה יכול לעורר הידרדרות במצבו של המטופל. במקרים מסוימים, יש להחליף את ההכנה של המטופל לחוקן בריום עם חוקן ומשלשלים בתזונה מיוחדת שנקבעה יומיים לפני המחקר. במקרים מסוימים, השימוש בחוקן ניגוד יכול להאיץ ניקוב או לגרום להתרחבות רעילה של המעי הגס. לכן, איריגוסקופיה מתבצעת לאחר שקיעה של תופעות חריפות. שיטה זו חושפת חוסר אחידות ו"גרעיניות" של הרירית, עיבוי דופן המעי, כיב, פסאודופוליפוזיס, חוסר גזירה. אבחנה מבדלת של קוליטיס כיבית לא ספציפית מתבצעת בעיקר עם דלקות מעיים חריפות. בנוכחות מגיפה של דלקות מעיים, האבחנה מתבססת בקלות. אך גם במקרה של תחלואה ספורדית בדלקות מעיים חריפות, תסמונת הקוליטיס זורמת ללא הישנות, בעוד שלקוליטיס כיבית יש מהלך חוזר. השיטות המדויקות ביותר לזיהוי זיהום מעי חריף כוללות בקטריולוגיות וסרולוגיות. לעתים קרובות, קוליטיס כיבית מובחן ממחלת קרוהן. במקרים טיפוסיים, מחלת קרוהן נבדלת מקוליטיס לא ספציפי בהיעדר נזק לפי הטבעת, מעורבות תכופה של האיילאום בתהליך הפתולוגי ונגעים מקטעים של דופן המעי. האבחנה הסופית יכולה להתבצע על ידי זיהוי גרנולומות לימפואידיות ספציפיות למחלת קרוהן בדגימות ביופסיה. עם קוליטיס גרנולומטי, paraproctitis ופיסטולות פאררקטליים מזוהים לעתים קרובות יותר מאשר עם קוליטיס כיבית לא ספציפית. במקרים מסוימים, יש צורך להבחין בין קוליטיס כיבית לבין שחפת מעיים. עבור שחפת מעיים, לוקליזציה מסוימת של התהליך אופיינית (אילאום, אזור אילוצקי), נזק מעי מגזרי. אבל לפעמים עם שחפת מעי, פי הטבעת וכל המעי הגס נפגעים. התמונה הקולונוסקופית של שחפת מעיים מאופיינת בנוכחות של כיבים עם קצוות מוגבהים מלאים בתוכן אפרפר. כיבים שחפתים נוטים להתפשט בכיוון רוחבי ולהשאיר מאחוריהם צלקות קצרות שבהן מופיעים שוב כיבים. עם קוליטיס כיבית לא ספציפית, צלקות אינן נוצרות באתר של כיבים לשעבר. בחולים מבוגרים וסניליים, יש להבדיל בין קוליטיס כיבית לבין קוליטיס איסכמית. האחרון מאופיין בכאבים עזים והתקפיים בבטן 20-30 דקות לאחר האכילה, בעוד שבקוליטיס כיבית מופיעים כאבים לפני פעולת עשיית הצרכים. הסימן הרדיולוגי החשוב ביותר הוא סימפטום "טביעת אגודל". התמונה האנדוסקופית של קוליטיס איסכמית מאופיינת בגבולות מוגדרים בחדות של הנגע, שטפי דם תת-ריריים, תצורות פסאודופוליפיות ציאנוטיות בולטות לתוך לומן המעי. בדיקה היסטולוגית מגלה תאים המכילים המוסידרין ופיברוזיס. היעדר דימום מגע בזמן הביופסיה מעיד גם יותר על קוליטיס איסכמית. טיפול. היעדר גורם אטיולוגי יחיד ומורכבות הפתוגנזה של קוליטיס כיבית לא ספציפית מקשים על הטיפול במחלה זו. נעשה שימוש בתרופות בעלות השפעות אנטי דלקתיות ואנטי בקטריאליות: salazopyridazine, sulfasalazine, salazodimethoxin, salofalk. Sulfasalazine נלקח דרך הפה, בהשתתפות מיקרופלורה של המעי, מתפרק לחומצה 5-אמינוסליצילית וסולפאפירידין. סולפאפירידין לא נספג מעכב את הצמיחה של מיקרופלורה אנאירובית במעי, כולל קלוסטרידיה ובקטריודים. ובזכות חומצה 5-אמינוסליצילית, התרופה לא רק גורמת לשינויים במיקרופלורה של המעיים, אלא גם מווסתת תגובות חיסוניות וחוסמת מתווכים של התהליך הדלקתי. התרופה נקבעת במינון של 2-6 גרם ליום למשך כל תקופת הדלקת הפעילה. כאשר התסמונת הקוליטית שוככת, המינון של sulfasalazine מופחת בהדרגה, ומביא אותו לתחזוקה (בממוצע 1-1,5 טבליות ליום). המינוי של נגזרות של חומצה 5-אמינוסליצילית (סאלופאלק, מסקול, סאלוסן, טידיקול) היא השיטה הבסיסית וניתן להשתמש בה כמונותרפיה לצורות קלות ובינוניות של קוליטיס כיבית. הטיפול מתבצע על רקע טיפול דיאטטי למעט מוצרי חלב, בנוכחות תכולה מאוזנת של חלבונים, שומנים, פחמימות וויטמינים בתזונה. רצוי לא לכלול פירות טריים, ירקות, מזון משומר. מזון צריך להיות עדין מבחינה מכנית וכימית. האכלה חלקית 4-5 פעמים ביום. חוסר איזון ויטמין משבש את תהליך הספיגה של מיקרו-אלמנטים ומפוצה על ידי מינוי תכשירים מורכבים בטבליות ("Duovit", "Oligovit", "Unicap"). בתסמונת שלשולים חמורים אצל אנשים עם מהלך קל ומתון של המחלה, יש לציין את מינויו של sandostatin, המעכב את הסינתזה של הורמוני מערכת העיכול ואמינים ביוגניים (פפטיד vasoactive מעיים, גסטרין, סרוטונין), הייצור שלהם מוגבר בחדות ב. קוליטיס כיבית ומחלת קרוהן. וגם התרופה מפחיתה הפרשה ומשפרת את הספיגה במעי, מעכבת את זרימת הדם הקרביים ומפחיתה את התנועתיות. בעת שימוש בסנדוסטטין (בתוך 7 ימים במינון של 0,1 מ"ג פעמיים, תת עורית), השלשול פוחת, הטנסמוס כמעט נעלם, והפרשת הדם עם הצואה פוחתת. בצורה חמורה של קוליטיס כיבית לא ספציפית, הטיפול מתבצע על רקע תזונה פרנטרלית. תכולת החלבון של תכשירים אלה צריכה להיות בערך 1,5-2,0 גרם/ק"ג ממשקל הגוף. קורטיקוסטרואידים, הניתנים באופן פרנטרלי, הם טיפול פתוגני לצורה חמורה של המחלה: במהלך היום הראשון, פרדניזולון ניתן לווריד במרווחים של 12 שעות (90-120 מ"ג או יותר), ב-5 הימים הבאים - תוך שרירית, הפחתת המינון בהדרגה. עם השפעה חיובית, הם עוברים לטיפול תרופתי דרך הפה (פרדניזולון 40 מ"ג ליום). מתן הורמונים לטווח ארוך במהלך תקופה של הפוגה יציבה אינו מעשי. בחולים עם מהלך חמור של המחלה, נצפתה השפעה חיובית של חמצון היפרברי (HBO). השימוש בקורס של HBO (7-10 הליכים) במהלך תקופת ההפוגה יכול להפחית את תדירות ההתקפים. אינדיקציות לטיפול כירורגי חירום: ניקוב מעי, התרחבות רעילה, דימום מעי רב, ממאירות. בצורה מתונה של מהלך של כיב כיב לא ספציפי, נדרשת דיאטה קפדנית עם הגבלה של סיבים, מוצרי חלב ותכולת חלבון גבוהה. פרדניזולון ניתן דרך הפה במינון ראשוני של 20-40 מ"ג ליום. ניתן להשלים את הטיפול עם sulfasalazine והאנלוגים שלו, הנלקחים דרך הפה או ניתנים במיקרוקליסטרים ונרות לתוך פי הטבעת. המינון הראשוני של sulfasalazine הוא 1 גרם ליום, ולאחר מכן הוא גדל ל 4-6 גרם. כשיטת טיפול עזר, ניתן להשתמש במרתח של עשבי תיבול עם השפעות אנטי דלקתיות והמוסטטיות (שורש שרוף, עלה סרפד, חזזית, קונוסים אלמון אפור, שורש ליקוריץ), רפואת צמחי מרפא מאפשרת לעתים קרובות להפחית את המינון של תכשירי סאלאזופ, להאריך הֲפוּגָה. תחזית ומניעה. במקרים חמורים ובנוכחות של סיבוכים מערכתיים ומקומיים, הפרוגנוזה חמורה. החולים אינם מסוגלים לעבוד לחלוטין. בצורות קלות ומתונות של המחלה, הפרוגנוזה לחיים חיובית. יש להעביר מטופלים לעבודה קלה. במהלך תקופת ההפוגה, מומלץ טיפול תחזוקתי עם תכשירי salazopreparations, חומרים חיידקיים, פסיכותרפיה וטיפול דיאטטי. חולים הסובלים מקוליטיס כיבית לא ספציפית במשך זמן רב (יותר מ-5-7 שנים) צריכים להיות מוקצים לקבוצת הסיכון להופעת סרטן המעי ולהכניס אותם לתיעוד. חולים אלו מוצגים אחת לשנה קולונוסקופיה עם ביופסיה ממוקדת. הרצאה מס' 15. מחלות כליות. גלומרולונפריטיס חריפה גלומרולונפריטיס חריפה (AGN) היא מחלת כליות מפוזרת חריפה בעלת אופי זיהומי-אלרגי, הממוקמת בגלומרולי. AGN יכולה להיות מחלה עצמאית (ראשונית) או להיות משנית כחלק ממחלה אחרת, מה שמסבך את התמונה הקלינית ואת האבחנה של האחרונה. AGN משפיע בדרך כלל על גברים צעירים ובני גיל העמידה. אטיולוגיה. AGN מתרחשת לרוב לאחר זיהום קוקי (שפעת, דלקת שקדים חריפה, דלקת הלוע הנגרמת על ידי מה שנקרא זנים נפריטוגניים של מיקרואורגניזמים). ב-60-80% מהחולים מתגלה סטרפטוקוקוס β-המוליטי מקבוצת A; ב-1/3 מהמקרים לא ניתן לקבוע את האטיולוגיה של AGN. היפותרמיה ממושכת, במיוחד בתנאים של לחות גבוהה, תורמת להתפתחות AGN. גם החיסון מהווה גורם להופעת המחלה, וב-75% מהמקרים הכליות נפגעות לאחר הזריקה השנייה או השלישית. פתוגנזה. לפתוגנזה של המחלה יש מנגנון חיסוני: כאשר אנטיגנים (סטרפטוקוקלים, חלבונים רפואיים, חלבונים זרים) חודרים לגוף, נוצרים בתגובה נוגדנים הקושרים אנטיגנים אלו ויחד עם השבר השלישי של המשלים יוצרים קומפלקסים חיסוניים שמסתובבים בכלי הדם. מיטה. הקומפלקסים מסוגלים להתמקם בצד החיצוני של קרום הבסיס של הנימים הגלומרולריים, ולגרום לנזק שלהם באמצעות שחרור תוצרי פירוק משלים, המגבירים את חדירות הנימים וגורמים לשינויים מקומיים בהם האחרונים. נויטרופילים ממהרים לאתרי השקיעה של קומפלקסים חיסוניים, שהאנזימים הליזוזומליים שלהם מחמירים את הפגיעה באנדותל ובממברנת הבסיס, ומפרידים אותם זה מזה. פירוק טסיות דם גורם לשחרור סרוטונין, מה שמוביל להמוקרישה ותצהיר פיברין על קרום הבסיס. חיסול קומפלקסים חיסוניים מהגוף מקל על ידי תגובה מקרופאג בצורה של התפשטות של תאי mesangial ואנדותל, עם היעילות של תהליך זה, החלמה מתרחשת. תמונה קלינית. התמונה הקלינית של המחלה מורכבת מהתסמונות הבאות. תסמונת השתן. 1. פרוטאינוריה הנובעת ממעבר מולקולות חלבון דרך מרווחי דופן הנימי של הגלומרולוס, הנוצרות בעת שקיעת קומפלקסים חיסוניים עליהן. פרוטאינוריה היא סלקטיבית בטבעה, שבה בעיקר אלבומינים עוברים דרך ה"פילטר" הגלומרולרי. 2. המטוריה על רקע מעורבות של מזנגיום נימי ורקמות אינטרסטיציאליות בתהליך הפתולוגי. אריתרוציטים חודרים דרך השברים הקטנים ביותר בקרום הבסיס, ומשנים את צורתם. 3. Cylindruria - הפרשת שתן של תאים גליליים של הצינוריות. במהלך תהליכים דיסטרופיים בצינוריות של התאים המפורקים של אפיתל הכליה, נוצרים גלילים גרגירים המורכבים ממסה גרגירית צפופה; לגלילים שעווה קווי מתאר חדים ומבנה הומוגני; יציקות היאליניות הן תצורות חלבוניות. תסמונת יתר לחץ דם נצפית עקב: 1) החזקת נתרן ומים; 2) הפעלה של מערכות רנין-אנגיוטנסין-אלדוסטרון והסימפטו-אדרנל; 3) ירידה בתפקוד המערכת המדכאת של הכליות. תסמונת בצקת קשורה לגורמים הבאים: 1) ירידה בסינון הגלומרולרי עקב תבוסתם; 2) ירידה במטען הסינון של נתרן ועלייה בספיגתו מחדש; 3) אגירת מים עקב אגירת נתרן בגוף; 4) עלייה ב-BCC; 5) היפראלדוסטרוניזם משני; 6) עלייה בהפרשת ADH ועלייה ברגישות הנפרון הדיסטלי אליו, המובילה לאגירת נוזלים; 7) עלייה בחדירות הדפנות הנימים ושחרור פלזמה לרקמות; 8) ירידה בלחץ האונקוטי בפלזמה עם פרוטאינוריה מסיבית. תלונות המוצגות ב-AGN אינן ספציפיות ומתרחשות במחלות שונות. חשוב מאוד לציין באנמנזה כאב גרון לאחרונה, החמרה של דלקת שקדים כרונית, היפותרמיה וכו'. חלק מהמטופלים מציינים ירידה בתפוקת השתן בשילוב עם קצת נפיחות (פסטו) של הפנים בבוקר. ב-1/3-3/4 חולים בימים הראשונים של המחלה, אין כאבים חזקים וכואבים במיוחד באזור המותני הקשורים לגידול בגודל הכליות. יש גם עייפות מוגברת, כאבי ראש, קוצר נשימה במהלך מאמץ גופני, עלייה קצרת טווח בטמפרטורת הגוף עד תת חום. יתר לחץ דם עורקי, המתגלה רק במחצית מהחולים, מאופיין בעלייה במספרים ל-140-160 / 85-90 מ"מ כספית. אומנות. (לעיתים רחוקות - עד 180/100 מ"מ כספית. אמנות). אבחון. ב-100% מהמקרים, בדיקת שתן מגלה פרוטאינוריה בדרגות חומרה שונות, צילינדרוריה ומה שהכי חשוב לאבחון, המטוריה בדרגות חומרה שונות - ממיקרוהמטוריה (עד 10 כדוריות דם אדומות בשדה הראייה) ועד למקרוהמטוריה (אם כי די נדירה). ). עם זאת, אם יש חשד ל-AGN, יש צורך לערוך סדרה של בדיקות שתן חוזרות או לבצע בדיקת Nechiporenko (קביעת מספר היסודות שנוצרו ב-1 μl), שכן ייתכן שלא יתגלו כדוריות דם אדומות בחלק אחד של שתן. כאשר בודקים את הדם, מתגלים אינדיקטורים לשלב חריף (עלייה בתכולת הפיברינוגן ו-α2-גלובולין, חלבון C-reactive, האצת ESR), מספר הלויקוציטים משתנה מעט, אנמיה מתונה. עם מהלך לא מסובך של AGN, תכולת החומרים החנקניים (קריאטינין, אינדיקן, אוריאה) בדם אינה משתנה. בשלב הראשוני של המחלה נצפה שינוי בבדיקת ריברג - ירידה בסינון הגלומרולרי ועלייה בספיגה חוזרת של הצינוריות, המתנרמלת עם התאוששותה. בדיקת רנטגן בחולים עם יתר לחץ דם עורקי חמור עשויה להראות עלייה מתונה בחדר השמאלי, המקבל את אותו גודל כמו שהמטופל מתאושש. ישנן 3 גרסאות קליניות של AGN. 1) וריאנט מונוסימפטומטי: תלונות קלות, היעדר בצקת ויתר לחץ דם עורקי, יש רק תסמונת שתן; הגרסה השכיחה ביותר של מהלך המחלה (86% מהמקרים). 2) וריאנט נפרוטי: בצקת, אוליגוריה בולטים, אפשר להעלות את לחץ הדם למספרים נמוכים יחסית, זה מתגלה ב-8% מהחולים. 3) גרסה מורחבת: יתר לחץ דם עורקי, מגיע למספרים גבוהים (180/100 מ"מ כספית), בצקת בולטת בינונית, כשל במחזור הדם, מופיע ב-6% מהמקרים. אבחון דיפרנציאלי. יש להבחין בין AGN לבין גלומרולונפריטיס כרונית, שאינה קשה עם הופעתה החריפה של AGN וההיפוך המוחלט של התסמינים לאחר מכן. עם זאת, בהיעדר הופעה חריפה, כמו גם בהתמדה ארוכת טווח של סימנים מסוימים של המחלה, האבחנה הופכת מסובכת משמעותית. אם קשה להבדיל, פונים לביופסיית נקב של הכליה. קשה להבדיל בין AGN לבין pyelonephritis עקב נוכחות של לויקוציטוריה בשתי המחלות. עם זאת, AGN מלווה בפרוטאינוריה מסיבית יותר, ובמקרים מסוימים, בצקת. אבחון דיפרנציאלי נעזר גם בסימפטומים הקליניים של פיאלונפריטיס בצורה של כאב בולט יותר בגב התחתון, המלווה בחום והפרעות דיסוריות. כמו כן, יש ערך אבחנתי להגדרה של בקטריוריה בפיאלונפריטיס, זיהוי של לויקוציטים "פעילים", וכן מחקרים ברנטגן (דפורמציה של הכוסות) ואיזוטופ-רנוגרפי (א-סימטריה של תפקוד הכליות). יש להבדיל את AGN כמחלה עצמאית ממחלות רקמת חיבור מפוזרות כרוניות, שבהן AGN הוא אחד מביטויי המחלה. מצב זה מתרחש בדרך כלל עם חומרת תסמונות שתן, יתר לחץ דם ובצקת וחוסר בהירות מספקת של תסמינים אחרים של המחלה, לעתים קרובות יותר עם SLE (זאבת אדמנתית מערכתית). האבחנה הנכונה ב-SLE יכולה להיעשות על ידי התחשבות בתסמונת המפרק, פגיעה בעור ובאיברים אחרים (לב), שינויים אימונולוגיים בולטים (זיהוי נוגדנים אנטי-איברים בטיטר גבוה, תאי לופוס אריתמטוזוס, נוגדנים ל-DNA ול-RNA ), כמו גם ניטור הדינמיקה של התמונה הקלינית. טיפול. הטיפול ב-AGN הוא מורכב וכולל את האמצעים הבאים. 1. מצב. אם יש חשד ל-AGN או מיד לאחר קביעת האבחנה, יש לאשפז את החולה מיד. יש להקפיד על מנוחה קפדנית במיטה במשך כ-2-4 שבועות עד להעלמת הבצקת ולנורמליזציה של לחץ הדם. השהייה במיטה מספקת התחממות אחידה של הגוף, מה שמוביל לירידה ב-vasospasm (ולכן, לירידה בלחץ הדם) ולעלייה בסינון הגלומרולרי ומשתן. לאחר השחרור מבית החולים, ניתן טיפול ביתי עד 4 חודשים ממועד הופעת המחלה, המהווה את המניעה הטובה ביותר של המעבר של AGN לשלב הכרוני. 2. דיאטה. בהתאם לחומרת התסמינים הקליניים, חשוב מאוד להגביל נוזלים ונתרן כלורי. עם צורה מורחבת ונפרוטית, מומלץ לצום מלא למשך 1-2 ימים עם צריכת נוזלים בכמות השווה לשתן. ביום 2-3 מוצגת צריכת מזון עשיר במלחי אשלגן (דייסת אורז, תפוחי אדמה). כמות המים הכוללת ששותים ליום צריכה להיות שווה לנפח השתן שהוקצה ליום הקודם בתוספת 300-500 מ"ל. לאחר 3-4 ימים, החולה מועבר לתזונה עם הגבלת חלבון (עד 60 גרם ליום), וכמות המלח הכוללת אינה עולה על 3-5 גרם ליום. דיאטה כזו מומלצת עד להעלמת כל התסמינים החוץ-כליים ולשיפור חד במשקעי השתן. 3. טיפול תרופתי כולל בעיקר טיפול אנטיביוטי, אשר, עם זאת, צריך להתבצע רק אם האופי הזיהומי של AGN מבוסס בצורה מהימנה (הפתוגן בודד ולא חלפו יותר מ-3 שבועות מאז הופעת המחלה). בדרך כלל רושמים פניצילין או אנלוגים חצי סינתטיים שלו במינונים קונבנציונליים. נוכחותם של מוקדים ברורים של זיהום כרוני (דלקת שקדים, סינוסיטיס וכו') היא גם אינדיקציה ישירה לטיפול אנטיביוטי. משתנים בטיפול ב-AGN ניתנים רק עם אצירת נוזלים, עלייה בלחץ הדם והופעת אי ספיקת לב. הפורוזמיד היעיל ביותר (40-80 מ"ג), בשימוש עד לחיסול בצקת ויתר לחץ דם. אין צורך במרשם ארוך טווח של תרופות אלו, מספיקות 3-4 מנות. בהיעדר בצקת, אך יתר לחץ דם מתמשך או עם השפעה לא מספקת של תרופות להורדת לחץ דם, תרופות להורדת לחץ דם (קלופלין, דופגיט) נקבעות עם משך מתן שתלוי בהתמדה של יתר לחץ דם עורקי. בצורה הנפרוטית של AGN, נקבע טיפול מדכא חיסון (קורטיקוסטרואידים - פרדניזון 60-120 מ"ג ליום, ואחריו ירידה הדרגתית במינון, משך השימוש למשך 4-8 שבועות). במקרה של AGN עם בצקת חמורה וירידה משמעותית בשתן, הפרין ניתן בקצב של 20-000 IU ליום במשך 30-000 שבועות, ומשיג עלייה של זמן קרישת הדם פי 4-6. עם פרוטאינוריה ממושכת, אינדומתצין או וולטרן נקבעים במינון של 75-150 מ"ג ליום (בהיעדר יתר לחץ דם ואוליגוריה). הפרוגנוזה חיובית, עם זאת, עם צורות ממושכות, קיימת אפשרות שהתהליך יהפוך לכרוני. מניעת AGN מסתכמת בטיפול יעיל בזיהום מוקד, התקשות רציונלית. על מנת לזהות בזמן את הופעת המחלה לאחר חיסון, הועבר SARS בכל החולים, יש צורך לבחון את השתן. הרצאה מס' 16. מחלות כליות. פיילונפריטיס פיילונפריטיס היא מחלה זיהומית שבה מעורבים בתהליך אגן הכליה, הגביעים שלו וחומר הכליות, עם נגע עיקרי של הרקמה הבין-סטילית. בהקשר זה, פיילונפריטיס היא דלקת כליות אינטרסטיציאלית (אינטרסטיציאלית). זהו מושג רחב יותר מפיאלונפריטיס. היא מציינת, ראשית, סוג של דלקת בכליות מכל אטיולוגיה עם מעורבות דומיננטית של האינטרסטיטיום, ושנית, מחלה מיוחדת שבה דלקת זו היא הביטוי היחיד והעיקרי שלה. קרוב לדלקת כליות אינטרסטיציאלית היא מה שנקרא tubulo-interstitial nephritis, שבה יש נגע ידידותי של הצינוריות והסטרומה של הכליות. מיון. בהתבסס על נתונים קליניים ומורפולוגיים, מובחנת פיאלונפריטיס חריפה וכרונית, שלרוב יש מהלך חוזר בצורה של התקפים של פיאלונפריטיס חריפה. כמו כן, פיילונפריטיס יכולה להיות חד צדדית. לפי צורת הקורס (לפיאלונפריטיס כרונית): צורה חוזרת, פיילונפריטיס כרונית סמויה, כליה מקומטת פיילונפרית. אטיולוגיה ופתוגנזה. פיילונפריטיס היא מחלה זיהומית. הגורמים הגורמים לו הם גורמים זיהומיים בעלי אופי לא ספציפי: E. coli, enterococcus, staphylococcus וחיידקים נוספים, אך ברוב המקרים אנו מדברים על E. coli (40%) ופלורה מעורבת (38%). תשומת הלב מופנית לצורות L של חיידקים, פרוטופלסטים (גופי חיידקים, נטולי ממברנות שיכולות לתמוך בזיהום), קנדידה, שעלולה לגרום לפיאלונפריטיס כרונית. מקורות הזיהום יכולים להיות שקדים, מחלות של איברי המין והמעי הגס, כלומר גורמים זיהומיים יכולים לחדור אל הכליה, כולל האגן, עם זרם הדם (המטוגנית יורד pyelonephritis), אשר נצפית במחלות זיהומיות רבות (קדחת טיפוס, שפעת , אנגינה, אלח דם). לעתים קרובות יותר, חיידקים מובאים לתוך הכליות בדרך עולה מהשופכים, שלפוחית השתן, השופכה (פיאלונפריטיס אורוגנית), אשר מסייעת על ידי דיסקינזיה של השופכנים והאגן, לחץ תוך-אגני מוגבר (ריפלוקס שלפוחית ופיאלורנלי), כמו גם ספיגה חוזרת של תוכן האגן לוורידים של מדולה הכלייתית (ריפלוקס pyelovenous). פיילונפריטיס עולה, ככלל, מסבכת את המחלות של מערכת גניטורינארית, שבהן יציאת השתן קשה (אבנים והיצרות של השופכנים, היצרות של השופכה, גידולים של מערכת גניטורינארית), ולכן היא מתפתחת לעתים קרובות במהלך ההריון. ייתכן גם זיהום לימפוגני בכליות (פיאלונפריטיס לימפוגנית), כאשר המעי הגס ואיברי המין הם מקור הזיהום. להתפתחות פיאלונפריטיס, בנוסף לחדירת זיהום לכליות, יש חשיבות רבה לתגובתיות הגוף ולמספר גורמים מקומיים הגורמים להפרה של יציאת השתן וקיפאון בשתן. אותן סיבות מסבירות את האפשרות של מהלך כרוני חוזר של המחלה. מיקרואורגניזמים נגועים עם שינויים תפקודיים ומורפולוגיים בדרכי השתן המובילים לקיפאון בשתן, הפרעה ביציאת הוורידים והלימפה מהכליה, התורמים לקיבוע הזיהום בכליות, גורמים לאזורים מוקדיים ופולימורפיים של חדירות דלקתיות וצפיחת האינטרסטיטיום של אחד מהם. או שתי הכליות. רקמת הביניים של הצינוריות מושפעת, ולאחר מכן הנפרונים. יש endarteritis פרודוקטיבי, היפרפלזיה של הקליפה האמצעית של הכלים, תופעות של hyalinosis, arteriolosclerosis להתפתח עד הכליה מקומטת משני. בשנים האחרונות, תפקיד מסוים בהתפתחות של פיאלונפריטיס כרונית מוקצה לתגובות אוטואימוניות: בהשפעת אנטיגנים חיידקיים, אימונוגלובולין G ומשלים מופקדים על קרום הבסיס של הנימים הגלומרולריים, וגורמים לנזק שלו. המעבר של פיאלונפריטיס חריפה לכרונית מקל על ידי: אבחון מאוחר של פיאלונפריטיס חריפה, אשפוז בטרם עת, נוכחות של זיהומים כרוניים, סוכרת, גאוט ושימוש לרעה במשככי כאבים - phenacetin. דלקת פיאלונפריטיס כרונית שכיחה יותר בנשים (50%), אשר מתאפשרת כתוצאה מהריונות, במיוחד חוזרים (אסטרוגנים גורמים לאטוניה של השרירים החלקים של דרכי השתן), בילדות אצל בנות, הקשורה למבנה של דרכי השתן. , החריגות שלהם. תמונה קלינית. כפי שצוין לעיל, גם מהלך חריף וגם כרוני של פיאלונפריטיס אפשרי. התמונה הקלינית של השלב החריף של המחלה מאופיינת בעלייה פתאומית וחדה בטמפרטורת הגוף עד 39-40 מעלות צלזיוס, עלולה להתרחש הופעת חולשה, כאבי ראש, צמרמורות, בשילוב עם הזעה מרובה, בחילות והקאות. יחד עם העלייה בטמפרטורת הגוף, מופיעים כאבים באזור המותני, אשר, ככלל, מצוינים בצד אחד. אופי הכאב עמום, עוצמתם שונה. במקרה של התפתחות המחלה על רקע אורוליתיאזיס, קדם להתקף של פיאלונפריטיס התקף של קוליק כליות. בהיעדר טיפול הולם, המחלה עלולה להפוך לכרונית, או שהדבר מוביל להתפתחות תהליכים ספוריטיביים בכליה, המתבטאים קלינית בהידרדרות במצב הכללי של החולה ובתנודות טמפרטורה פתאומיות (מ-35-36 מעלות C בבוקר עד 40-41 מעלות צלזיוס בערב). פיילונפריטיס כרונית היא, ככלל, תוצאה של פיילונפריטיס חריפה שאינה מטופלת בצורה לא נכונה, כאשר ניתן היה להסיר דלקת חריפה, אך לא ניתן היה להרוס באופן קיצוני את כל הפתוגנים בכליה או לשחזר את יציאת השתן הפיזיולוגית מהכליה. דלקת פיילונפריטיס כרונית מודאגת מכאבים קהים מתמידים של כאב באזור המותני, המחמירים במזג אוויר קר לח. כמו כן, פיילונפריטיס כרונית נוטה להחמרות תקופתיות, כאשר למטופל יש את כל הסימנים של תהליך חריף. אבחון. הבעיה באבחון המחלה נובעת מהעובדה שתסמיני הפיאלונפריטיס דומים לתסמינים של מחלות אחרות הנובעות מדלקת בדרכי השתן. תכנית הבדיקה האבחנתית כוללת בדיקות דם, בדיקות שתן וכן מחקרים המראים את מצב מערכת השתן: אולטרסאונד של הכליות, מחקרי רנטגן, ניתוח PCR לגורם זיהומי. כדי לאמת את סוג הסוכן הזיהומי, יש צורך לבצע תרבית בקטריולוגית של דגימת שתן, ושיטה של טומוגרפיה ממוחשבת משמשת כדי לא לכלול תהליכי גידול. לפיכך, לשיטות מעבדה ולשיטות מחקר מיוחדות חשיבות רבה להכרה במחלה. ובפיאלונפריטיס כרונית, הביטויים המכריעים, ולפעמים היחידים, הם שינויים בשתן, בדם ובדרכי השתן. יש צורך לנטר באופן דינמי את לחץ הדם ומשקל המטופל. לויקוציטוזיס, ESR מוגבר, שינוי נויטרופילי בדם, עלייה ברמת החנקן שיורית (בנורמה של 20-40 מ"ג), אוריאה (נורמה של 40-60 מ"ג), קריאטינין (נורמה של 53-106 מיקרומול) / ליטר), אינדיקן (נורמה של 1,41, 3,76-180 מיקרומול/ליטר), כולסטרול (נורמה 200-83 מ"ג), כלורידי דם (נורמה XNUMX ממול/ליטר). חשוב לאבחון שינויים בשתן: ירידה במשקל הסגולי, פרוטאינוריה (כולל יומית), המטוריה וצילינדוריה. עם זאת, שיטות לקביעה כמותית של היסודות הנוצרים של משקעי שתן מקבלים חשיבות אבחנתית גוברת: קאקובסקי-אדיס (לוקוציטים רגילים עד 4 מיליון תאי דם אדומים - עד מיליון, גלילים - עד 1 ב-2 שעות), אמבורגר (לוקוציטים רגילים עד 24, אריתרוציטים - עד 2000, צילינדרים - עד 1400 לדקה), Nechiporenko (בדרך כלל לויקוציטים עד 20, אריתרוציטים - עד 1, צילינדרים - עד 2500 ב-1000 מ"ל של שתן טרי) . היחס בין המספר המוחלט של אריתרוציטים וליקוציטים במשקע השתן בפיאלונפריטיס משתנה באופן דרמטי לקראת דומיננטיות משמעותית של לויקוציטים פי 10-20. בפיאלונפריטיס כרונית מופיעים תאי סטנהיימר-מלבין בשתן: לויקוציטים גדולים, עם תנועה בראונית של גרגירים ציטופלזמיים, המופיעים עם ירידה בתכונות האוסמוטיות של השתן (משקל סגולי מתחת ל-10-14), צבועים כחולים עם סגול ג'נטיאן וספרונין, לויקוציטים "פעילים": לויקוציטים משתנים, בעלי התנועה הבראונית של הפרוטופלסמה, מתגלים כשהם צובעים בתמיסה מימית של 1% של מתילן כחול בתוספת מים מזוקקים. הערך האבחוני של עלייה במספר הלויקוציטים ה"פעילים" ותאי סטנהיימר-מלבין (עד 40%), בקטריוריה (ספירת מיקרוביאלית יותר מ-100 אלף ל-1 מ"ל שתן), בדיקת ניטריט (עם ספירת חיידקים של יותר יותר מ-100 U, חיידקים מפרקים ניטריטים בשתן) מודגשים. , בתוספת של חומצה סולפנילית ו-L-naphthylamine, מופיע צבע אדום), בדיקת TTX קולורימטרית (בפעולה של דהידרוגנאזות מיקרוביאליות, טריפנילטטרזוליט כלוריד מצטמצם לאדום בלתי מסיס טריפנילפורמזן תוך 4-10 שעות בטמפרטורה של -37 מעלות צלזיוס), בדיקת פרדניזולון פרובוקטיבית (החולה נאסף בצלחת סטרילית, החלק האמצעי של השתן הוא השליטה, ואז 30 מ"ג של פרדניזולון ב-10 מ"ל של מי מלח הוא לאט מוזרק לווריד והחלק האמצעי של השתן נאסף שלוש פעמים במרווחים של שעה ואחרי 24 שעות; בפיאלונפריטיס כרונית, מספר הלויקוציטים, חיידקים מכפילים, מופיעים לויקוציטים "פעילים", לפחות בחלק אחד), אנטיביוגרמות. יש להקדיש תשומת לב מיוחדת למיקרוסקופיה של שחפת של הכליות (מיקרוסקופיה של מריחות מוכתמות על פי ציל, זריעת שתן על מדיה מיוחדת - השיטה של פריס ושקולניקובה, השיטה הביולוגית). אם יש חשד לתהליך חד צדדי, יש צורך לבצע בדיקת שתן, הנלקחת בנפרד מכל כליה עם צנתרים מיוחדים. תפקיד חשוב באבחון של דלקת פיאלונפריטיס כרונית ממלאים בשיטות מחקר רדיולוגיות: רדיוגרפיה סקר וטומוגרפיה (מאפיין את מיקומן, גודלן וצורתן של הכליות), פיאלוגרפיה הפרשה ורטרוגרדית (ירידה בריכוז וביכולת ההפרשה של הכליות, עוויתות , אנומליות, עיוותים של האגן, גבשושיות), פנאומופילוגרפיה (לזיהוי אבנים שאינן מנוגדות), אנגיוגרפיה כלייתית (חושפת הפרה של ארכיטקטוניקת כלי הדם - עורקים וורידים). כדי לקבוע את בטיחות התפקוד והפרנכימה של הכליות, במיוחד בתהליך חד צדדי, נעשה שימוש בשיטות רדיואינדיקטיביות - רנוגרפיה (היפורן יוד 131) וסקאנוגרפיה (באמצעות neohydride Hg 203). ביופסיה לנקב במקרה של פיילונפריטיס עקב מוקדי התהליך עשויה שלא לספק מידע. כרומוציסטוסקופיה עשויה להצביע על נזק לכליות. טיפול. לרוב, הטיפול בפיאלונפריטיס הוא שמרני, אולם אם דלקת פיאלונפריטיס חריפה היא מוגלתית, ייתכן שתידרש התערבות כירורגית. טיפול שמרני מורכב ממשטר, דיאטה, שימוש באנטיביוטיקה, וכן תרופות שונות המייצבות את תפקוד הכליות וגוף המטופל בכללותו. ב pyelonephritis חריפה, מנוחה קפדנית במיטה מסומנת. יש לצרוך את המזון מזונות המכילים את הכמות האופטימלית של חלבונים, שומנים ופחמימות. בתקופה החריפה, יש צורך להחליף חלבון ומזון צמחי. עם שיכרון חמור, אתה צריך לשתות הרבה מים. טיפול בפיאלונפריטיס כרוני מורכב מהשפעה על הזיהום (אטיוטרופי) בפיאלונפריטיס ראשוני וביטול סיבה כזו או אחרת בפיאלונפריטיס משנית, מנגנונים פתוגנטיים וטיפול בסיבוכים. הטיפול היעיל ביותר הוא לאחר קביעת האנטיביוגרמה. טיפול מתמשך (לפחות חודשיים) בתרופות אנטיבקטריאליות מתבצע. מיד עם הקבלה, תרופה אנטיביוטית, sulfanilamid או nitrofuran נקבעת. לאחר 1-10 ימים, התרופות מוחלפות, הטיפול מתבצע עד להיעלמות מתמשכת של לויקוציטוריה ובקטריוריה. ברגע שההחמרה מסולקת, מתבצע טיפול לסירוגין באחד מהתרופות האנטיבקטריאליות למשך 4-5 חודשים: התרופה ניתנת למשך 7 ימים, ולאחר מכן נלקחת הפסקה למשך 8-10 ימים, או התרופה ניתנת עבור 10 ימים עם מרווח של 15-20 ימים, או שהתרופה ניתנת למשך 15 ימים, המרווח נעשה למשך 15 ימים, ואז נקבע שוב טיפול אנטי-מיקרוביאלי. משך הטיפול והמרווחים נקבעים על פי תסמינים קליניים ובקרת מעבדה. יש לציין כי במקרה של דלקת פיאלונפריטיס שהתפתחה בחולה עם דלקת שקדים כרונית, אנטיביוטיקה מסדרת הפניצילין היא היעיל ביותר, במקרה של זיהומים באברי המין בגברים ובנשים משתמשים באנטיביוטיקה רחבת טווח (ראה טבלה 12). . בנוכחות פלורה גרם-שלילית, טיפול בחומצה נלידיקסית נותן תוצאות טובות (שחורים, איוויגרמון - 1,0 גרם 4 פעמים ביום למשך 7 ימים, אך יש לרשום את ההכנות שלה בתדירות נמוכה יותר מאשר תרופות אחרות (פעמיים)). מתכשירי sulfanilamide משתמשים ב-etazol (2 גרם 1,0 פעמים - 4 ימים), סולפור (10 גרם 0,1 פעמים), סולפונאמידים ארוכי טווח. כמו כן, קורסים מטופלים עם furazolidon, furadonin, furagin (3 גרם 0,1 פעמים ביום). יש להדגיש כי יש לקבוע את תפקוד הכליות לפני תחילת הטיפול. טיפול אנטיביוטי ארוך טווח צריך להתבצע עם קצב סינון גלומרולרי של לפחות 30 מ"ל לדקה או עם שארית תכולת חנקן בסרום הדם של לא יותר מ-70 מ"ג. אינדיקטור ליעילות התרופה לאחר שבוע של טיפול הוא ירידה בספירת החיידקים ל-10 ב-000 מ"ל שתן. ניתן להפחית את הארסיות של המיקרופלורה ולהגביר את היעילות של סוכנים אנטיבקטריאליים על ידי שינוי תגובת השתן כל 10-14 ימים. מזון בסיס, נתרן ציטראט (10 גרם ליום), מים מינרליים אלקליין עוזרים להפחית את תגובות ה-pH. פעילות אנטיבקטריאלית מסוימת מכילה נתרן בנזואט (4-6 גרם ליום), אשר מצוי בשפע בחמוציות ובדובי. טיפול פתוגנטי צריך להיות מכוון להגברת התגובתיות של הגוף, שיפור יציאת השתן ונורמליזציה של לחץ הדם. כדי להפעיל תגובתיות אימונוביולוגית, נעשה שימוש באלפא-גלובולין, אוטו-המותרפיה, עירוי דם, טיפול בחיסונים (טיפול חיסון אוטומטי מתבצע במשך 30-40 ימים, 0,1 מ"ל תת עורית או 0,2-0,3 מ"ל כל יומיים), טוקסואיד סטפילוקוקלי (2-0,1- 0,3-0,5-0,7-1,0-1,2-1,7 מ"ל כל 2,0 ימים). עשבי תיבול משתנים (דוב, גרגרי ערער, זנב סוס, עלה אורתוסיפון - תה כליות, עלה לינגונברי), נוגדי עוויתות (פפברין, נו-שפא וכו') עוזרים לנרמל את יציאת השתן. אם ישנה חסימה בזרימת השתן, יש לציין טיפול כירורגי. עם יתר לחץ דם נלווה, הכנות rauwolfia מסומנים - isobarine, dopegyt, hemiton, saluretics, אנטגוניסטים אלדוסטרון. מניעה ופרוגנוזה. מניעת פיילונפריטיס מורכבת מאמצעים ראשוניים ומשניים. מניעה ראשונית כוללת, קודם כל, טיפול במחלות שעלולות להוביל להתפתחות פיילונפריטיס: זיהומים מוקדיים, מחלות אורולוגיות (כגון אורוליתיאזיס, אדנומה של הערמונית, כמו גם כל מחלה המלווה בהפרה של יציאת השתן מהגוף. כליות), פעילויות פנאי. לוח 12 יעילות השוואתית של תרופות אנטיבקטריאליות בפיאלונפריטיס
מניעה משנית כוללת זיהוי של בקטריוריה במהלך בדיקות מונעות (לדוגמה, נשים בהריון צריכות לבצע ניתוח בקטריולוגי של שתן לפחות פעם בחודש), מינוי לטיפול נגד הישנות: בשבוע הראשון של כל חודש - הפסקה בטיפול: מרתח שושנים, השבוע השני, השלישי - משתנים וחיטוי צמחים, השבוע הרביעי - חומרים אנטיבקטריאליים (ניטרופורנים, אנטיביוטיקה, חיטוי, פעם בשנה - נוויגרמון 1 גרם 1 פעמים במהלך השבוע ו-1,0 גרם - במהלך השבוע השני, או 4 -NOC 2-5 מ"ג 100 פעמים ביום 150-4 ימים). טיפול נגד הישנות מתבצע במשך 2-3 שנים. יש לבצע בדיקות מרפא עם טיפול 3-4 פעמים בשנה או 4-6 פעמים. תחזית. הפרוגנוזה תלויה בשלב המחלה. טיפול בסנטוריום. טיפול בסנטוריום-נופש מתאים במהלך תקופת ההפוגה, במיוחד עבור חולים עם פיאלונפריטיס חשבונית משנית לאחר ניתוחים אורולוגיים (Truskavets, Sairme, Zheleznovodsk, Berezovsky מים מינרליים), שם חולים נוטלים מים במינרליים נמוך. טיפול בסנטוריום וספא אינו התווית במקרה של יתר לחץ דם גבוה, אנמיה חמורה ואי ספיקת כליות ברורה. סיבוכים של פיילונפריטיס הם מגוונים. בפיאלונפריטיס חריפה, התקדמות התהליך המוגלתי מובילה לאיחוי של מורסות גדולות ולהיווצרות קרבונקל של הכליה, תקשורת של חללים מוגלתיים עם האגן (pyonephrosis), מעבר התהליך לקפסולה סיבית (פרינפריטיס). ) ורקמה פרינפרית (פארנפריטיס). דלקת פיילונפריטיס חריפה יכולה להסתבך על ידי נמק של הפפילות של הפירמידות (papillonekrosis), המתפתחת כתוצאה מהשפעה רעילה ישירה של חיידקים במצבים של קיפאון שתן. סיבוך זה של פיאלונפריטיס מתרחש ברוב המקרים בחולי סוכרת. לעיתים רחוקות, פיאלונפריטיס הופכת למקור לאלח דם. עם הגבלת התהליך המוגלתי במהלך תקופת ההצטלקות, יכולות להיווצר מורסות המוקפות בממברנה פיוגנית (מורסה כליה כרונית). בפיאלונפריטיס כרונית, במיוחד חד צדדית, ניתן לפתח יתר לחץ דם נפרוגני וטרשת עורקים בכליה השנייה (שלמה). קמטים פיילונפריים דו-צדדיים של הכליות מובילים לאי ספיקת כליות כרונית. התוצאה של פיאלונפריטיס חריפה היא בדרך כלל החלמה, אך כתוצאה מסיבוכים (פיונפרוזיס, אלח דם, פפילונקרוזיס), עלול להתרחש מוות. פיילונפריטיס כרונית עם קמטים של הכליות מסתיימת לעתים קרובות עם אזוטמיה אורמיה. עם התפתחות יתר לחץ דם עורקי ממקור כליות, תוצאה קטלנית בפיאלונפריטיס כרונית קשורה לעיתים לסיבוכים המתרחשים ביתר לחץ דם (דימום מוחי, אוטם שריר הלב וכו'). מחבר: Mostovaya O.S.
עור מלאכותי לחיקוי מגע
15.04.2024 פסולת חתולים של Petgugu Global
15.04.2024 האטרקטיביות של גברים אכפתיים
14.04.2024
▪ Microchip LoRa RN2483 IoT אלחוטי מודול
▪ סעיף האתר סוללות, מטענים. בחירת מאמרים ▪ מאמר אנשים נוספים. ביטוי עממי ▪ מאמר מה מאפיין את גודל הכוכבים? תשובה מפורטת ▪ מאמר סוד (דיו סימפטי). מתכונים וטיפים פשוטים ▪ מאמר מסנן קוורץ פשוט. אנציקלופדיה של רדיו אלקטרוניקה והנדסת חשמל
בית | הספרייה | מאמרים | <font><font>מפת אתר</font></font> | ביקורות על האתר www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese








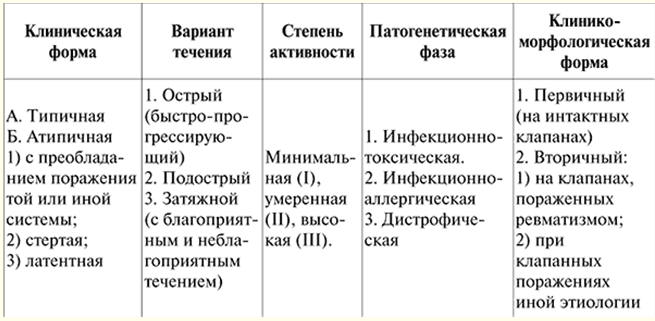








 ראה מאמרים אחרים סעיף
ראה מאמרים אחרים סעיף 