
|
|
אינציקלופדיה של רדיו אלקטרוניקה והנדסת חשמל מאפיינים השוואתיים של תאים גלווניים בגודל AA. אנציקלופדיה של רדיו אלקטרוניקה והנדסת חשמל
אנציקלופדיה של רדיו אלקטרוניקה והנדסת חשמל / מטענים, סוללות, תאים גלווניים כיום ניתן למצוא אלמנטים גלווניים רבים ושונים בחנויות ובשווקים. באילו לבחור? מאמר זה יעזור לך לקבל את ההחלטה הנכונה. תאים וסוללות גלווניים נמצאים בשימוש נרחב להפעלת ציוד אלקטרוני שונים. האלמנטים הנפוצים ביותר הם גודל AA. במדפי המכירות ניתן למצוא מוצרים דומים מחברות שונות, בעיקר של שתי מערכות אלקטרוכימיות: מלוחים ובסיסי. לאחרונה, אנרג'ייזר החלה לייצר תאי ליתיום בגודל AA בגודל 1,5 V. המאפיין החשוב ביותר של תא גלווני - קיבולת (כמות החשמל שהוא מסוגל לספק לעומס) - כמעט אף פעם לא מצוין על התווית. קונים יכולים להסתמך רק על פרסומות טלוויזיה על תאים ש"מחזיקים מעמד עד פי עשרה מתאי מלח רגילים", או לקחת את המילה של אנרג'ייזר שתאי הליתיום החדשים שלה בגודל AA e2 מחזיקים מעמד פי חמישה יותר מתאי אלקליין רגילים [1]. יתר על כן, לא לגמרי ברור אילו אלמנטים נקראים "רגילים". כדי להשוות כמותית את הפרמטרים של אלמנטים של מערכות אלקטרוכימיות שונות, יש צורך לבדוק אותם באותם תנאים. בדיקות כאלה בוצעו עם שלושה סוגים של אלמנטים: מלח Philips Long Life (EMF של אלמנט "טרי" - 1,65 V), Duracell Ultra MZ אלקליין (1,62 V) ו-Lithium Energizer e2 (1,8 V). כל אחד מהם הוטען בנגד של 15 אוהם, התואם לזרם פריקה ראשוני של כ-100 mA. עבור אלמנטים בגודל סטנדרטי AA, זרם עומס זה אופייני. הפריקה בוצעה במחזורים של מספר שעות ביום, התואם את תנאי ההפעלה האמיתיים. זה מסביר את "קוצים" במתח על עקומות הפריקה המוצגות באיור. 1. העקומה הכחולה מתאימה ליסוד המלח, אדום ליסוד הבסיסי וירוק ליסוד הליתיום. במהלך תקופת "המנוחה", המתח על אלמנט מכל סוג עלה מעט, אך לאחר חיבור העומס הוא ירד במהירות למינימום במחזור הקודם. הנקודות מסמנות את ערכי ה-EMF של האלמנטים - המתח עליהם ללא עומס.
אם ניקח כקריטריון לפריקה מלאה של תא ירידה במתח בעומס שלו ל-0,9 וולט, הקיבולת שנקבעה בניסוי של תא המלח הייתה 1 Ah, התא הבסיסי היה 2,9 Ah, ותא הליתיום היה 3,5 Ah . כתוצאה מכך, אין צורך לדבר על הבדלים של פי חמישה ועשר בקיבולת של אלמנטים ממערכות אלקטרוכימיות שונות. באיור. איור 2 מציג סדרה נוספת של עקומות.
הם מראים כיצד ההתנגדות הפנימית של האלמנטים השתנתה במהלך תהליך הפריקה. ההתאמה בין סוג האלמנט לצבע העקומה כאן זהה לזו באיור. 1. ערכי ההתנגדות הפנימית R חושבו באמצעות הנוסחה
כאשר E הוא EMF של היסוד; U - מתח תחת עומס; RH - התנגדות לעומס. ההתנגדות הפנימית של מלח ואלמנטים אלקליים עולה באופן מונוטוני ככל שהפריקה מתקדמת. והתנגדות הליתיום, לאחר ירידה חדה בתחילת הפריקה, נשארת כמעט ללא שינוי עד הסוף, ואז עולה באותה מידה. כמובן, הניסויים שבוצעו אינם יכולים להיקרא ממצים. הקיבולת של אלמנט אינה ערך קבוע לחלוטין, היא תלויה בגורמים חיצוניים רבים. עבור אלמנטים שונים, ניתן להשיג את המקסימום שלו בתנאי פריקה שונים באופן משמעותי. כדי לקחת את כל זה בחשבון, יהיה צורך לערוך סדרה גדולה מאוד של ניסויים, לא מציאותיים בתנאי חובבים. עם זאת, בואו ננסה לבדוק את התוצאות המתקבלות בחישוב. כדי להעריך את הקיבולת המקסימלית האפשרית תיאורטית של יסודות ממערכות אלקטרוכימיות שונות, עליך לדעת את ההרכב הכימי של האלקטרודות שלהם, האלקטרוליט והתגובה הכימית המתרחשת באלמנט. עבור תאים מלח ובסיסי, הקתודה היא אבץ והאנודה היא מנגן דו חמצני. מסיבה זו אלמנטים כאלה נקראים ביחד מנגן-אבץ. אבל האלקטרוליט שבהם שונה: מלח (בדרך כלל אמוניום כלוריד) או אלקלי (אשלגן הידרוקסיד). לפי [2], התגובה מתרחשת ביסוד מלח מנגן-אבץ
ובאלקליין
אין מידע אמין על חומר האלקטרודה והתגובה הכימית בתא הליתיום. אפשר רק להניח שהאלקטרודות הן ליתיום ומנגן דו חמצני, והאלקטרוליט הוא תמיסה של ליתיום פרכלורט בפרופילן קרבונט. אם הניחוש הזה נכון, לפי [2], מתרחשת תגובה בתא הליתיום
באמצעות חוק פאראדיי, אנו מקבלים ביטוי לקביעת הקיבולת של תא גלווני C, Ah:
כאשר m היא המסה של חומרים מגיבים F = 96,5-103 C/g-eq - מספר פאראדיי; n - ערכיות (עבור מלח ותאים גלווניים אלקליים - 2, עבור ליתיום - 1); M הוא המשקל המולקולרי הכולל של החומרים המגיבים. אנו שוקלים תאים גלווניים בגודל AA: מלח - 17 גרם, אלקליין - 24 גרם, ליתיום - 15 גרם נניח שבהשוואה למסה של החומרים המגיבים, מסת גוף התא וחומרים שאינם לוקחים חלק. בתגובה (אלקטרודת פחמן, אלקטרוליט בתאי אלקליין וליתיום), היא זניחה וניתן להזניח. אנו מחשבים את המשקל המולקולרי הכולל של החומרים המגיבים מהמשוואות לעיל של תגובות כימיות: עבור מלח - 346 גרם, עבור אלקליין - 257 גרם, עבור ליתיום - 94 גרם החלפת ערכים מספריים בנוסחה, אנו מקבלים את המקסימום האפשרי קיבולת תא המלח - 2,6 Ah, אלקליין - 5 Ah, ליתיום - 4,3 Ah. ניתן להסביר את ההבדלים בין ערכי הקיבול המחושבים לאלו הנמדדים על ידי הנחות גסות למדי שנעשו בחישובים. אז לא נמצאו הבדלים של פי חמישה או עשרה. הקיבולת התיאורטית של תא אלקליין היא כפולה מזו של תא מלח, ולליתיום אין יתרון על פני אלקליין בהקשר זה. זה תואם את תוצאות הניסוי. בהתבסס על התוצאות של כל העבודה שנעשתה, אנו יכולים להסיק את הדברים הבאים: 1. לתאים גלווניים של ליתיום יש את המתח היציב ביותר, ההתנגדות הפנימית הנמוכה ביותר, שלמעשה אינה תלויה במידת הפריקה, והקיבולת הגבוהה ביותר, אם כי לא בהרבה. רצוי להשתמש בהם להנעת ציוד עם צריכת זרם גבוהה, כמו גם במכשירים הנכבים אוטומטית כאשר מתח אספקת החשמל יורד (לדוגמה, מצלמות דיגיטליות). 2. לתאים אלקליים יש קיבולת דומה לזו של ליתיום והם גם מסוגלים לספק זרם גבוה לעומס, אך במתח נמוך יותר. הם משמשים בצורה הטובה ביותר במכשירים עם צריכת זרם ממוצעת ללא בקרת מתח אוטומטית. במקרים רבים, תאים אלקליין מועדפים על פני תאי ליתיום מכיוון שהם זולים פי שלושה עד ארבעה. 3. לתאי מלח יש את הקיבולת הקטנה ביותר ואת ההתנגדות הפנימית הגבוהה ביותר. רצוי להשתמש בהם בציוד עם צריכת זרם נמוכה. ספרות
מחבר: I.Podushkin, מוסקבה
עור מלאכותי לחיקוי מגע
15.04.2024 פסולת חתולים של Petgugu Global
15.04.2024 האטרקטיביות של גברים אכפתיים
14.04.2024
▪ סודות מתמטיים של איש השלג המושלם ▪ שבב להעברת נתונים מהירה במיוחד באמצעות אור
▪ חלק של האתר טכנולוגיית מפעל בבית. בחירת מאמרים ▪ סעיף משפט אזרחי. חלק מיוחד. עריסה ▪ מאמר כיצד אוכל לכבות את השריפה? תשובה מפורטת ▪ מאמר קצב תגובה - ניסויים עם סודה וחומץ. ניסיון כימי הערות על המאמר: אורח מאמר מעולה, תודה.
בית | הספרייה | מאמרים | <font><font>מפת אתר</font></font> | ביקורות על האתר www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese






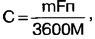
 השאר את תגובתך למאמר זה:
השאר את תגובתך למאמר זה: